Abwehr zwischen Angriff und Verteidigung
Damit das Immunsystem nicht aus dem Gleichgewicht gerät, dürfen die sogenannten MHC-Gene nicht zu variabel, aber auch nicht zu ähnlich sein
16. Oktober 2020
Evolutionsbiologie
Immunsystem
Alles hat seinen Preis – erst recht natürlich die Gesundheit. Am Max-Planck-Institut für Evolutionsbiologie in Plön erforscht Tobias Lenz mit seinem Team, was die evolutionären Kosten für eine perfekte Immunität wären und warum wir nicht gegen alle Krankheitserreger immun sind.
Text: Catarina Pietschmann
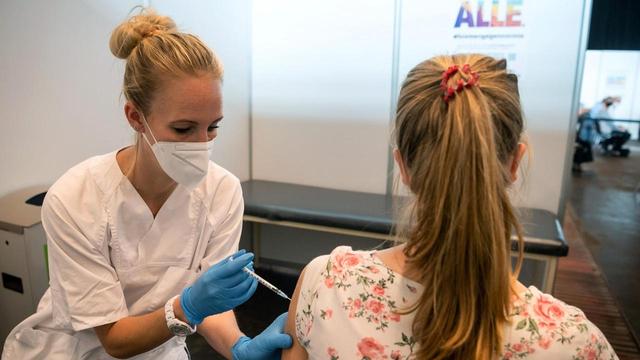
Schutzschirm Immunsystem: Ohne sein Abwehrsystem wäre unser Körper Bakterien und Viren hilflos ausgeliefert.
Schutzschirm Immunsystem: Ohne sein Abwehrsystem wäre unser Körper Bakterien und Viren hilflos ausgeliefert.
© MPG/ Alessandro Gottardo
Selten zuvor ist so viel über Krankheitserreger und Immunität gesprochen worden wie in diesen Tagen. Die Corona-Pandemie hat deutlich gemacht, wie wertvoll ein starkes Immunsystem ist. Aber warum gelingt es Viren, Bakterien und anderen Keimen immer wieder, unsere Körperabwehr zu überwinden? Könnte es nicht einen Rundum-Schutz geben, und was wäre der Preis dafür?
Tobias Lenz und sein Team analysieren den Wettstreit von Verteidigern und Angreifern. Am Computer berechnen sie, wie das Immunsystem auf Krankheitserreger wie Lepra-Bakterien oder HI-Viren reagiert. Ihr Untersuchungsobjekt: die sogenannten MHC-Gene.
MHC steht für „Haupt-Gewebeverträglichkeitskomplex“ („major histocompatibility complex“) und bezeichnet eine Gruppe von Genen, die bei allen Wirbeltieren vorkommen. Der Mensch besitzt sechs solcher Gene, die auch als „Humane Leukozyten Antigene (HLA)“ bezeichnet werden. Diese Gene sind mit dafür verantwortlich, dass das Immunsystem Eindringlinge überhaupt als solche erkennen kann. Die Proteine dieser Gene binden Molekülbruchstücke, die in Zellen eingedrungene Erreger hinterlassen haben, und stellen sie auf der Zelloberfläche wie in einem Schaufenster aus. Patrouillierende Immunzellen erkennen sie dort als Fremdmoleküle und versetzen das Immunsystem in Alarmbereitschaft.
Doch wie schaffen es so verhältnismäßig wenige Gene angesichts der schier unermesslichen Fülle von Viren, Bakterien, Pilzen und anderen Parasiten, dass ihnen kaum ein Eindringling entgeht? Der Schlüssel liegt in der extrem hohen Variabilität dieser Gene: Sie sind die variabelsten Gene im gesamten Erbgut. „Vom Gen HLA-B, einem der menschlichen MHC Gene zum Beispiel sind über 4.000 Varianten bekannt“, sagt Tobias Lenz.
Durch die hohe Variabilität der MHC-Gene ist sichergestellt, dass es zu fast jedem Eindringling ein passendes MHC-Protein gibt. Kursiert also ein bestimmter Erreger in einer Population, besitzen die Individuen mit der entsprechenden MHC-Variante einen evolutionären Vorteil. Ihre Träger erkranken nur leicht oder gar nicht. Folglich wird die Häufigkeit dieser Variante in der Population ansteigen. Will er auch künftig erfolgreich sein muss der Erreger darauf reagieren und sich so verändern, dass die MHC-Variante keinen Schutz mehr bietet. Zu dem mutierten Keim passt nun eine andere Genvariante, und der evolutionäre Wettlauf geht in die nächste Runde.
Die Evolution kann dabei immer wieder eine andere Richtung nehmen. Was heute einen Vorteil bietet, kann morgen schon nutzlos sein. Aber nicht nur, dass die Angreifer schnell mutieren und sich von Generation zu Generation verändern können, sie treten manchmal auch nur an bestimmten Orten oder zu bestimmten Zeiten auf. „Langfristig wird also nicht eine einzelne Variante in der Population dominieren, sondern es werden verschiedene nebeneinander existieren“, erklärt Tobias Lenz. Evolutionsbiologen sprechen in so einem Fall von einem „balancierten Polymorphismus“.
Evolution im Zeitraffer
Tobias Lenz im Fischkeller seines Instituts. Der Wissenschaftler erforscht nicht nur die MHC-Gene des Menschen, sondern auch die von Stichlingen. Die große Vielfalt der MHC-Varianten soll die Fische zum Beispiel vor Parasiten schützen.
© MPG/ Achim Multhaupt
Tobias Lenz im Fischkeller seines Instituts. Der Wissenschaftler erforscht nicht nur die MHC-Gene des Menschen, sondern auch die von Stichlingen. Die große Vielfalt der MHC-Varianten soll die Fische zum Beispiel vor Parasiten schützen.
© MPG/ Achim Multhaupt
Lenz und seine Kolleginnen und Kollegen simulieren das Wechselspiel zwischen MHC-Genen und Krankheitserregern am Computer. Mit speziellen Programmen lässt sich die Ko-Evolution der Kontrahenten wie im Zeitraffer verfolgen. Darüber hinaus vergleichen die Forschenden Erbgut aus der Vergangenheit mit heutigen Genomen und lernen daraus, wie sich die MHC-Varianten über die Zeit entwickelt haben.
Zum Beispiel in den Skeletten eines Friedhofs aus dem Mittelalter in Dänemark. Die Toten gehörten zu einer Leprakolonie, wie sie an vielen Orten bis in die Neuzeit errichtet wurden, um eine Ausbreitung der früher oft tödlich verlaufenden Krankheit zu verhindern. Heute ist sie dank Antibiotika in den meisten Fällen heilbar.
In Südostasien tritt Lepra vereinzelt heute noch auf. Manche Menschen dort besitzen eine HLA-Variante, die die Anfälligkeit dafür erhöht. Könnte es sein, dass auch in Europa vor allem Menschen mit dieser Variante der Erkrankung zum Opfer gefallen sind? „Zusammen mit Forschenden der Universität Kiel haben wir in den Knochen aus dem Mittelalter tatsächlich die HLA-Variante häufiger nachgewiesen, die für Lepra anfälliger macht“, erzählt Lenz.
Aber warum hat sich die Genvariante über all die Jahrhunderte gehalten und ist nicht der Selektion zum Opfer gefallen? „Wie wir inzwischen wissen, hat diese Variante nicht nur Nachteile: So schlecht sie vor Lepra schützt, sie bewahrt ihre Träger aber auch vor dem erblichen Typ-1-Diabetes“, erklärt Lenz. Der negativen Selektion durch Lepra steht also eine positive Selektion durch den Schutz vor Diabetes gegenüber. Dadurch bleibt vermutlich die HLA-Variante in der Population erhalten.
HIV ist ein weiteres Beispiel für balancierten Polymorphismus: Das Immunsystem kann das HI-Virus mit manchen HLA-Varianten besser in Schach halten als mit anderen. „Wir konnten zeigen, dass manche Varianten besonders viele unterschiedliche Antigene des HI-Virus präsentieren. So wird es für das Immunsystem besser sichtbar und kann effizienter bekämpft werden.“ Der Schutz dieser Varianten kann in seltenen Fällen sogar so weit gehen, dass sie gar nicht an Aids erkranken. Die weniger wirksamen Varianten bieten dagegen möglicherweise Schutz gegen einen anderen Erreger.
HLA-Varianten könnten auch daran beteiligt sein, dass das Sars-Co2-Virus nur bei einem kleinen Prozentsatz der Infizierten zu ernsthaften Symptomen führt. Da Corona-Viren schon seit langem unter uns Menschen kursieren, besitzen die meisten von uns Genvarianten, die die Viren erkennen können. „Wir sind zwar anfällig für Sars-CoV2, weil es verhältnismäßig neu ist, aber aufgrund der Jahrtausende langen Selektion ist das Immunsystem der meisten Menschen in der Lage, das Virus klein zu halten“, sagt Tobias Lenz. Zurzeit untersucht er mit Kolleginnen und Kollegen aus aller Welt, inwieweit HLA-Gene hierbei eine Rolle spielen.
Gefahr von Autoimmunkrankheiten
Die MHC-Gene beinhalten die Information zur Bildung von Proteinen auf der Oberfläche einer Immunzelle (links). Diese binden Molekülfragmente aus dem Innern der Zelle und präsentieren sie einer T-Zelle des Immunsystems (rechts), die dann eine Abwehrreaktion auslösen kann.
© GCO nach Tobias Lenz / MPI für Evolutionsbiologie
Die MHC-Gene beinhalten die Information zur Bildung von Proteinen auf der Oberfläche einer Immunzelle (links). Diese binden Molekülfragmente aus dem Innern der Zelle und präsentieren sie einer T-Zelle des Immunsystems (rechts), die dann eine Abwehrreaktion auslösen kann.
© GCO nach Tobias Lenz / MPI für Evolutionsbiologie
Obwohl beim Menschen Tausende verschiedene HLA-Varianten vorkommen, besitzt jeder einzelne von uns nur eine Handvoll davon. Die hohe Variabilität hat nämlich eine Schattenseite: die Autoimmunität.
Die MHC-Proteine sind dafür ausgelegt, Moleküle von Bakterien, Viren und anderen Parasiten zu binden und an der Zelloberfläche zu präsentieren. Dort werden die Fremdmoleküle von bestimmten Immunzellen erkannt, den sogenannten T-Zellen. Zwar werden schon im Embryo die T-Zellen ausgewählt, die ausschließlich körperfremde Moleküle erkennen, und alle anderen aussortiert. Allerdings ist dieser Korrekturprozess nicht perfekt, und so kommen auch immer wieder T-Zellen durch, die körpereigene Moleküle erkennen. „Je mehr HLA-Varianten ein Mensch besitzt, desto mehr Fremdmoleküle können sie präsentieren – im Fall von Erregern, die sich so rasch verändern können wie HIV, ein großer Vorteil! Leider sind aber auch mehr körpereigene Moleküle darunter. Das kann zur Folge haben, dass das Immunsystem sich gegen sich selbst richtet und Autoimmunkrankheiten entstehen können. Multiple Sklerose, Typ-1-Diabetes, Zöliakie, Psoriasis, Morbus Bechterev und viele mehr – sie alle hängen mit bestimmten HLA-Varianten zusammen.
HLA-Variabilität im Gleichgewicht
Optimum der Immunität: Je höher die Vielfalt an MHC-Varianten ist, desto besser ist der Körper gegen Krankheitserreger und Parasiten geschützt. Gleichzeitig sinkt aber auch die Toleranz des Immunsystems. Bei geringer Vielfalt ist diese Gefahr geringer, dafür wächst aber die Anfälligkeit für Krankheiten.
© GCO nach Tobias Lenz / MPI für Evolutionsbiologie
Optimum der Immunität: Je höher die Vielfalt an MHC-Varianten ist, desto besser ist der Körper gegen Krankheitserreger und Parasiten geschützt. Gleichzeitig sinkt aber auch die Toleranz des Immunsystems. Bei geringer Vielfalt ist diese Gefahr geringer, dafür wächst aber die Anfälligkeit für Krankheiten.
© GCO nach Tobias Lenz / MPI für Evolutionsbiologie
Im Laufe der Evolution scheint sich die Diversität der HLA-Gene auf ein optimales Niveau eingependelt zu haben. „So sind wir ausreichend vor Krankheitserregern geschützt, gleichzeitig wird das Risiko für Autoimmunkrankheiten niedrig gehalten“, sagt Tobias Lenz. Doch gilt dies in unseren heutigen auf Hygiene getrimmten Gesellschaft auch noch? In vielen Ländern nehmen Autoimmunkrankheiten zu – ein Hinweis, dass sich das Gleichgewicht zwischen Infektabwehr und Autoimmunerkrankung zugunsten des letzteren verschoben hat? „Es könnte durchaus sein, dass die Zahl unserer HLA-Gene für die heutige Zeit zu hoch ist.“
Die Diversität der Immun-Gene beeinflusst also die Anfälligkeit sowohl für Infektions- als auch für Autoimmunkrankheiten. Auch bei Krebs könnten das Immunsystem und die HLA-Gene eine Rolle spielen, denn Immunzellen können die sich unkontrolliert teilenden Zellen erkennen und eliminieren. Manche Tumore werden so schon im Anfangsstadium vernichtet. Manchmal beginnt ein Tumor aber auch im fortgeschrittenen Stadium auf scheinbar wundersame Weise zu schrumpfen. Dies kann der Fall sein, wenn eine der in Tumoren häufig auftretenden Mutationen dazu führt, dass das Immunsystem die Tumorzellen plötzlich als fremd erkennt und angreift.
Wirksame Krebstherapie
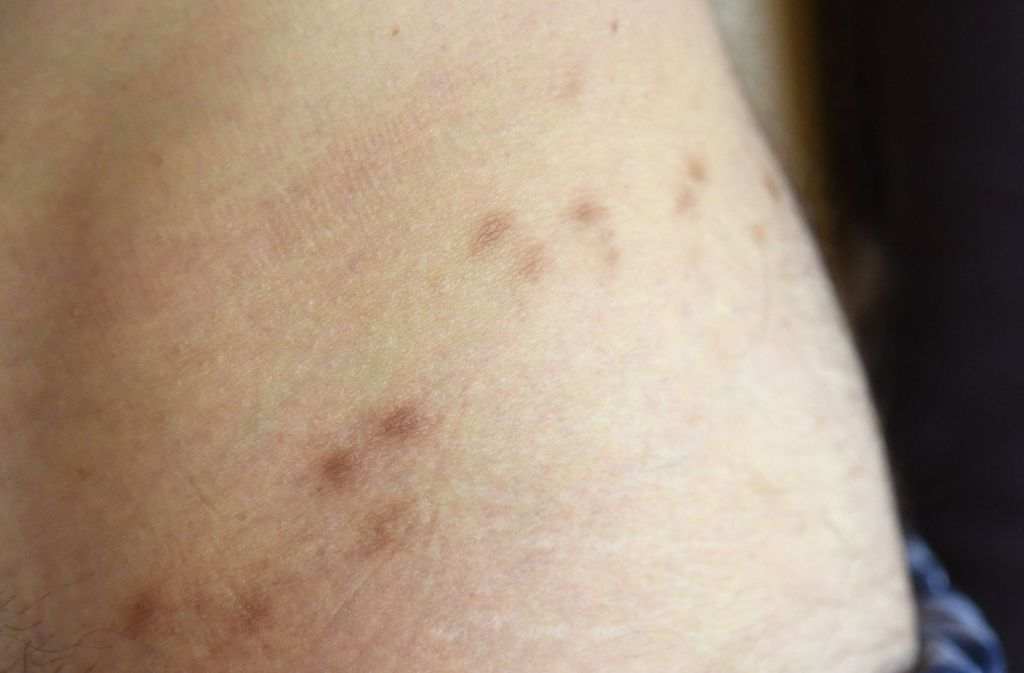
Entartete Pigmentzelle aus der Haut. Ein Immunsystem mit vielen HLA-Varianten kann Krebszellen wie diese leichter erkennen und bekämpfen. Entsprechend ist eine Immuntherapie bei Hautkrebspatienten mit hoher Variabilität dieser Gene effektiver, allerdings ruft die Behandlung bei solchen Patienten auch öfter Entzündungen hervor.
© Science Photo Library/ Steve Gschmeissner
Entartete Pigmentzelle aus der Haut. Ein Immunsystem mit vielen HLA-Varianten kann Krebszellen wie diese leichter erkennen und bekämpfen. Entsprechend ist eine Immuntherapie bei Hautkrebspatienten mit hoher Variabilität dieser Gene effektiver, allerdings ruft die Behandlung bei solchen Patienten auch öfter Entzündungen hervor.
© Science Photo Library/ Steve Gschmeissner
Zusammen mit Onkologen vom Memorial Sloan Kettering Cancer Center in New York haben Tobias Lenz und sein Team untersucht, welchen Einfluss die HLA-Ausstattung von Krebspatienten auf den Erfolg einer Immuntherapie hat. Durch eine solche Behandlung mit sogenannten Checkpoint-Inhibitoren sollen Immunzellen dazu gebracht werden, gegen körpereigene, sich unkontrolliert teilende Zellen vorzugehen. „Unsere Ergebnisse zeigen, dass eine Immuntherapie bei Patienten mit metastasiertem Hautkrebs besser wirkt, wenn sie eine hohe Vielfalt an HLA-Varianten besitzen“, sagt Lenz. Allerdings hängen auch häufige Nebenwirkungen einer Immuntherapie, etwa Entzündungsreaktionen wie Hautausschläge, Leber- und Darmentzündungen, mit den HLA-Genen zusammen.
Auch bei der Krebsabwehr gilt es für das Immunsystem also die Balance zu wahren, zwischen der Bekämpfung von Tumorzellen einerseits und der Vermeidung von Autoimmunerkrankungen andererseits. Wer ein lückenloses Abwehrsystem haben möchte, muss dafür in Kauf nehmen, dass sich dieses gegen den eigenen Körper richten könnte – ein Preis, der dann doch zu hoch wäre. Und so wird das Heer an Krankheitserregern auch künftig immer wieder Wege finden, unser Immunsystem zu überlisten.
Auf den Punkt gebracht:
MHC-Gene produzieren eine Fülle unterschiedlicher Proteine, mit deren Hilfe das Immunsystem Eindringlinge erkennen kann.
Manche MHC-Varianten schützen vor bestimmten Krankheitserregern, können aber auch Autoimmunerkrankungen auslösen.
Je mehr dieser Varianten ein Mensch besitzt, desto besser ist er gegen Erreger gewappnet. Der Preis dafür ist allerdings eine höhere Gefahr von Autoimmunerkrankungen. Jeder Mensch besitzt daher nur eine begrenzte Anzahl diese Gen-Varianten.