11. August
----------------------------------
SARS-CoV-2: Schwachstelle Spike-Protein
Österreichische Forschende haben möglicherweise eine Schwachstelle des SARS-CoV-2-Virus gefunden: Zwei kohlenhydratbindende Proteine könnten das Eindringen des Virus in die Wirtszelle verhindern.
Bei der Bekämpfung der Pandemie wird intensiv nach Möglichkeiten zur Eindämmung der Ausbreitung von SARS-CoV-2 geforscht. In diesem Zusammenhang ist das Spike-Protein von besonderem Interesse, da es der Haupteintrittsmechanismus des Virus in die Wirtszellen darstellt. So bestimmt die Interaktion des SARS-CoV-2-Spike-Proteins mit dem Angiotensin Converting Enzyme 2 (ACE2) der Wirtszellen die Infektiosität des Virus.
Österreichische Wissenschaftlerinnen und Wissenschaftler identifizierten zwei Säugetier-Lektine, die in Versuchen an das Spike-Protein von SARS-CoV-2 binden und so deren Funktionsfähigkeit einschränken konnten. Die Studienergebnisse wurden kürzlich im EMBO Journal veröffentlicht.
Lektine binden an Glykolisierungsstellen
Die Bedeutung des Spike-Proteins für das Überleben und die Ausbreitung des Virus erfordert einen Tarnmechanismus, um es vor der Immunantwort des Wirts zu verbergen. Dabei nutzt das Virus einen sogenannten Glykosylierungsmechanismus an bestimmten Stellen des S-Proteins, um eine Zuckerhülle zu bilden, die das antigene Protein vor der Immunreaktion des Wirts verbirgt. Die Glykosylierungsstellen des SARS-CoV-2-Spike-Proteins sind bei allen zirkulierenden Varianten hoch konserviert.
Hier die Beobachtung der Forschenden im Video
Die Forschenden stießen auf ihrer Suche nach einem Interaktionspartner für diese Glykolisierungsstellen auf Lektine. Lektine sind kohlenhydratbindende Proteine, dessen Bindung an das Spike-Protein dazu führte, dass das Virus nicht mehr in die Wirtszelle eindringen konnte.
Infektiosität von Lungenzellen konnte verringert werden
Das Team testete mehr als 140 Säugetier-Lektine und identifizierte zwei, die stark an die N-Glykanstelle N343 des Spike-Proteins binden: Clec4g und CD209c. Diese spezifische Stelle ist so essenziell für das Spike-Protein, dass sie bei keiner infektiösen Variante verloren gehen kann. Tatsächlich macht eine Deletion dieser Glykosylierungsstelle das Spike-Protein instabil. Darüber hinaus haben andere Gruppen gezeigt, dass Viren mit mutiertem N343 nicht infektiös sind.
Das österreichische Forschungsteam konnte zeigen, dass mit Hilfe der zwei identifizierten Lektine die SARS-CoV-2-Infektiosität von menschlichen Lungenzellen verringert werden konnte. „Der Ansatz ist vergleichbar mit dem Mechanismus des Medikamentenkandidaten 'APN01' [Apeiron Biologics], der sich in fortgeschrittenen klinischen Studien befindet. Dabei handelt es sich um ein biotechnologisch hergestelltes menschliches ACE2, das ebenfalls an das Spike-Protein bindet. Wenn das Spike-Protein von dem Medikament besetzt ist, wird der Zugang zur Zelle blockiert. Jetzt haben wir natürlich vorkommende Lektine von Säugetieren identifiziert, die genau das tun können”, sagt Professor Josef Penninger, Gruppenleiter der Studie. Aus Sicht des Forschungsteams sind diese Ergebnisse vielversprechend für variantenreiche therapeutische Interventionen gegen SARS-CoV-2.
Hoffmann D, Mereiter S, Jin Oh Y, et al. „Identification of lectin receptors for conserved SARS-CoV-2 glycosylation sites”. EMBO J. 2021 Aug 10:e108375. doi: 10.15252/embj.2021108375. Epub ahead of print. PMID: 34375000.
6. August
----------------------------------
Infektion erhöht Risiko für Herzinfarkt und Schlaganfall immens
Eine SARS-CoV-2-Infektion steigert das Herzinfarkt- und Schlaganfallrisiko temporär auf das mehr als Sechsfache, zeigt eine schwedische Studie. In Einzelfällen ist es sogar zwölffach erhöht.
Die Studie analysierte Daten von 86.742 schwedischen COVID-Patienten zwischen Februar und September 2020 und verglich diese mit Daten von 348.481 Kontrollpersonen. Die Forschenden untersuchten, welche Personen aufgrund von Herzinfarkten oder Schlaganfällen im Krankenhaus behandelt wurden. Andere Studien kamen bereits zu dem Ergebnis, dass COVID-19 wahrscheinlich ein Risikofaktor für akute kardiovaskuläre Komplikationen darstellt.
Ergebnis: Ohne Tag 0 betrug das Odds Ratio (OR) für einen akuten Myokardinfarkt 3,41 (Konfidenzintervall 95 Prozent, Spreizung 1,58 bis 7,36) und für einen Schlaganfall 3,63 (Konfidenzintervall 95 Prozent, Spreizung 1,69 bis 7,80) in den ersten zwei Wochen der Infektion. Als Tag 0 in die Auswertung eingeschlossen wurde, betrug das OR für akuten Myokardinfarkt 6,61 (Konfidenzintervall 95 Prozent, Spreizung 3,56 bis 12,20) und für ischämischen Schlaganfall 6,74 (Konfidenzintervall 95 Prozent, Spreizung 3,71 bis 12,20) in den ersten zwei Wochen der Infektion.
Die Ergebnisse deuten nach Ansicht der Autoren darauf hin, dass akuter Myokardinfarkt und ischämischer Schlaganfall einen Teil des klinischen Bildes von COVID-19 darstellen, und unterstreicht die Notwendigkeit einer Impfung gegen COVID-19.
Katsoularis, I. et al. „Risk of acute myocardial infarction and ischaemic stroke following COVID-19 in Sweden: a self-controlled case series and matched cohort study“ published in The Lancet on July 29, 2021. DOI:https://doi.org/10.1016/S0140-6736(21)00896-5
2. August
----------------------------------
Mundspülung reduziert Krankenhausaufenthalt
Antivirale Mundspülungen können auch als Therapeutikum verwendet werden. Eine Preprint-Studie zeigt, dass so die Schwere der COVID-Symptome und die Hospitalisierungsdauer gesenkt werden können.
Die bisher nur als Preprint erschienene Dreifachblind-Studie wurde vom 10. August bis 4. November 2020 in einer brasilianischen Klinik nahe Sao Paolo durchgeführt. Nachdem ein anionisches Phthalocyanin-Derivat (APD) in-vitro vielversprechende Wirkung zeigte, ließen die Forschenden 41 hospitalisierte, nicht intensivpflichtige COVID-Patienten zwischen 27 und 78 Jahre fünfmal am Tag (nach dem Aufwachen, Frühstück, Mittag- und Abendessen sowie vor dem Zubettgehen) für eine Minute mit 5 Millilitern APD-haltiger Mundspülung oder einem Placebo spülen und gurgeln.
Nach dem Zufallsprinzip waren dabei 20 Personen ausgewählt worden, die die eine Spülung mit Wirkstoff (active mouthwash, kurz „AM“) und 21, die eine ansonsten identische, aber wirkstofffreie Spülung (nonactive mouthwash, kurz „NAM“) erhielten.
Der Krankenhausaufenthalt sank auf fünf Tage
Ergebnis: Während die Dauer des Krankenhausaufenthalts für die NAM-Gruppe im Median 7 Tage betrug, lag der Vergleichswert der AM-Gruppe bei 4 Tagen. Die Autoren weisen zudem darauf hin, dass 75 Prozent der NAM-Patienten 12 Tagen im Krankenhaus verbleiben mussten, während der Wert in der AM-Gruppe bei 5 Tagen lag.
Weitere Ergebnisse: Sechs Probanden (26,8 Prozent) der NAM-Gruppe waren im weiteren Krankheitsverkauf auf Beatmung angewiesen und drei (14,3 Prozent) verstarben, in der AM-Gruppe gab es hingegen keine besonders schweren Verläufe.
Paulo Sérgio da Silva Santos et al. „Benefical effects of a mouthwash containing an antiviral phthalocyanine derivative on the length of hospital stay for COVID-19“, researchsquare.com, DOI: https://doi.org/10.21203/rs.3.rs-330173/v1
27. JULI
----------------------------------
Wie geht es schwer Erkrankten nach einem Jahr?
Wie geht es schwer an COVID-19 erkrankten Patienten nach einem Jahr? Chinesische Wissenschaftler untersuchten Lunge, Herz und Antikörper-Konzentration der mittlerweile Genesenen.
Von 56 zuvor schwer erkrankten COVID-Patienten zeigte ein Großteil auch ein Jahr nach der Infektion signifikante Einschränkungen beim Lungenfunktionstest. Geprüft wurden am Hospital of Chongqing Medical University unter anderem das Ausatemvolumen pro Sekunde sowie die Vitalkapazität, also die maximale Luftmenge, die nach tiefstmöglichem Einatmen ausgeatmet wird. Die CT-Aufnahmen des Brustkorbs zeigten, dass die Lungentrübung 3 und 10 Monate nach der Entlassung um 91,9 beziehungsweise 95,5 Prozent zurückgegangen war. Doch obwohl das Lungengewebe auf den CT-Bildern wieder merklich klarer erschien, war die Belastbarkeit des Organs weiterhin eingeschränkt.
Die durch die Infektion verursachten Lungenschäden hatten die meisten Patienten ohne Folgeschäden überstanden. Knapp 19 Prozent der Patienten hatte sich jedoch eine Lungenfibrose entwickelt, mehrheitlich bei den schwer erkrankten. Jeder fünfte hatte noch ein halbes Jahr nach Ende der Behandlung im Krankenhaus mit einer kardiopulmonaren Dysfunktion zu kämpfen, also mit Funktionsstörungen von Herz und Lunge. Etwa ein Fünftel der Patienten hatte 6 Monate nach der Entlassung eine kardiopulmonale Dysfunktion.
Die getesteten IgG-Antikörper waren bei allen Genesenen auch nach einem Jahr noch vorhanden. Zwar nahm die Konzentration im ersten halben Jahr um fast 69 Prozent ab, blieb aber die nächsten sechs Monate auf einem stabilen Niveau. Schwer Erkrankte hatten einen leicht höheren Antikörper-Titer als leichter Erkrankte. Bei zehn Patienten wurden nach zwölf Monaten keine Antikörper mehr festgestellt.
Xiao, K. et al: „Antibodies Can Last for More Than 1 Year After SARS-CoV-2 Infection: A Follow-Up Study From Survivors of COVID-19“ published in Front. Med. on July 16, 2021 DOI: https://doi.org/10.3389/fmed.2021.684864
22. JULI
----------------------------------
Delta-Variante erzeugt 1.260-mal höhere Viruslast
Eine Preprint-Studie liefert Hinweise, warum sich die Delta-Variante von SARS-CoV-2 so schnell verbreitet. Die Inkubationszeit ist 50 Prozent kürzer und die Viruslast Infizierter 1.260-mal höher.
Um herauszufinden, warum sich die Delta-Variante etwa doppelt so schnell überträgt wie der ursprüngliche Stamm von SARS-CoV-2, untersuchten chinesische Forschende 62 Probanden, die zu den ersten mit der Variante Infizierten auf dem chinesischen Festland gehörten. Sie wurden nach Kontakt mit dem Indexpatienten unter Quarantäne gestellt und anschließend kontinuierlich überwacht.
Das Team testete die Viruslast der Studienteilnehmer jeden Tag während des Infektionsverlaufs, um zu sehen, wie sie sich im Laufe der Zeit verändert. Die Forscher verglichen dann die Infektionsmuster mit denen von 63 Probanden, die sich 2020 mit dem ursprünglichen SARS-CoV-2-Stamm infiziert hatten.
Ergebnisse: Die durchschnittliche Inkubationszeit betrug bei der Deltavariante 4 Tage und war damit 50 Prozent kürzer als bei der Probandenstichprobe aus 2020 (6 Tage). Die Viruslast der Probanden war am ersten Tag mit einem positiven Testergebnis 1.260-mal höher.
Die Autoren schließen daraus, dass die Deltavariante des Virus im Wirt deutlich schneller repliziert als das Wildvirus. Die Annahme, dass die Variante damit auch in der präsymptomatischen Phase deutlich ansteckender sein könnte, unterstreicht nach Ansicht der Forschenden die Notwendigkeit einer rechtzeitigen Quarantäne für verdächtige Infektionsfälle oder enge Kontakte eines Infizierten – vor dem klinischen Beginn oder einem PCR-Screening.
Baisheng Li et al. "Viral infection and transmission in a large well-traced outbreak caused by the Delta SARS-CoV-2 variant", medRxiv 2021.07.07.21260122; doi: https://doi.org/10.1101/2021.07.07.21260122
Vakzin von Johnson & Johnson zeigt geringere Wirkung gegen Delta
An der Grossman School of Medicine in New York haben Forschende in Laborexperimenten analysiert, inwieweit die Seren von geimpften beziehungsweise rekonvaleszenten Personen fähig sind, der Bindung an SARS-CoV-2 zu widerstehen. Die Laborviren wiesen bei den Versuchen die Spike-Proteine verschiedener Virusvarianten auf – neben dem Wildtyp auch die Delta-Variante.
Dabei fiel auf, dass die mRNA-basierten Impfstoffe höhere Antikörper-Titer erzeugten als das Vakzin des US-Herstellers Johnson&Johnson. Das erzeugte im Laborversuch mit 220 eine ähnliche Titer-Höhe gegen den Wildtyp wie eigene Studiendaten bereits belegt hatten. Bei der Delta-Variante fiel der Titer bei geimpften Testpersonen jedoch signifikant ab und betrug nur 30. Zum Vergleich: Bei einer doppelten Impfung mit den mRNA-Vakzinen wurde ein Antikörper-Titer von rund 200 bei Delta festgestellt.
Sollten sich Durchbruchsinfektionen häufen, könnten die mit Johnson&Johnson geimpften Personen mit einem anderen Vakzin ein weiteres Mal geimpft werden.
Impfungen mit J&J in Deutschland
Bis zum 18. Juli 2021 wurden 3.957.030 Dosen des Impfstoffs von Johnson&Johnson nach Deutschland geliefert. Das entspricht 3,8 Prozent der mehr als 102 Millionen gelieferten COVID-Impfdosen. Zum Vergleich: Der Anteil des Herstellers BioNTech/Pfizer beträgt
68,6 Prozent
, der von Moderna
9,6 Prozent
und der von AstraZeneca
17,9 Prozent
.
Landau, N. R. et al: „Comparison of Neutralizing Antibody Titers Elicited by mRNA and Adenoviral Vector Vaccine against SARS-CoV-2 Variants“ published in bioRXiv on July 19, 2021. doi: https://www.biorxiv.org/content/10.1101/2021.07.19.452771v1
20. JULI
----------------------------------
Orale Ulzeration kann Frühwarnmarker für COVID 19 sein
In vielen Fallberichten werden orale Manifestationen von COVID-19 beschrieben. Ulzerationen gehören zu den häufigsten Befunden – sie könnten laut einer Meta-Analyse ein möglicher Frühwarnmarker bei asymptomatischen Patienten sein.
Forschende aus Taiwan sichteten für ihre Untersuchung die Fallberichte von 51 COVID 19-Patienten mit oralen ulzerierenden Läsionen. Das Alter der Patienten (28 Frauen, 23 Männer) reichte von 16 bis 83 Jahren, das Durchschnittsalter betrug 41,4 Jahre.
Ergebnis: Es gab 43 Fälle mit einer einzigen beteiligten Läsion und sechs Fälle mit mehr als einer Läsion in der Mundhöhle des Patienten (in zwei Fällen wurde die Anzahl der Läsionen nicht gemeldet). Die Läsionen zeigten sich am häufigsten an der Lippen- und Labialschleimhaut (28,6 Prozent), Zunge (25 Prozent), Gaumen- oder Wangenschleimhaut (jeweils 16,4 Prozent), Gingiva (8,9) oder den Mandeln (3,6 Prozent). Die Läsionsgrößen maßen zwischen 1 und 17 Millimetern, wobei der Großteil (88,9 Prozent) unter 10 Millimetern lag. Schmerzen beschrieben 40 Patienten.
Die Läsionen reichten von aphthösen Stomatitis-ähnlichen Läsionen bis hin zu weit verbreiteten Ulzerationen mit Nekrose oder Krusten. Wie bei der aphthösen Stomatitis zeigten die meisten Läsionen dabei solitäre oder mehrfach ausgestanzte Ulzerationen, die von einer gelblichen Membran bedeckt und von einem erythematösen Halo umgeben waren.
Andere der Läsionen zeigten ein herpetiformes Muster ähnlich einer Herpesinfektion, lieferten jedoch ein negatives Ergebnis für den Test auf Herpes-simplex-Virus. Manche ähnelten wiederkehrenden Herpesinfektionen, ohne dass die Patienten eine entsprechende Vorgeschichte hatten. Läsionen wie aphthöse Ulzerationen traten ebenfalls auf, ohne dass die Patienten eine Vorgeschichte wiederkehrender aphthösen Stomatitis (RAS), oral entzündlicher Erkrankungen oder Allergien hatten.
Die Schlussfolgerung der Autoren: Da die Latenz vom Beginn erster systemischer Infektionssymptome bis hin zu oralen Läsionen im Mittel 3,2 Tage betrug und damit deutlich unter der Inkubationszeit von COVID-19 liegt, könnte ihr Vorhandensein für eine frühzeitige Diagnose der zugrundeliegenden COVID 19-Infektion vor allem bei asymptomatischen Patienten hilfreich sein.
Yu-Hsueh Wu et al., „Review of oral ulcerative lesions in COVID-19 patients: a comprehensive study of 51 cases”, Journal of Dental Sciences, 2021, ISSN 1991-7902, https://doi.org/10.1016/j.jds.2021.07.001.
14. JULI
----------------------------------
Genschere stoppt Virus-Replikation
Australische Forscher haben herausgefunden, dass sich das Virus mittels Genschere Crispr in einer infizieren Zelle aufhalten lässt.
Wissenschaftler des australischen Peter Doherty Institute for Infection and Immunity (Doherty Institute) und des Peter MacCallum Cancer Centre in Melbourne haben eine Möglichkeit gefunden, die Vermehrung des SARS-CoV-2-Virus in infizierten menschlichen Zellen zu stoppen. Die Entdeckung baut auf Forschungen aus dem Jahr 2019 auf: Damals konnten Forscher zeigen, dass man mithilfe eines CRISPR-Gen-Editing-Tools abnormale RNAs, welche Krebs bei Kindern verursachen, eliminieren kann.
Nun fanden sie heraus: Derselbe Ansatz funktioniert auch bei SARS-CoV-2 und vor allem bei den bersorgniserregenden Varianten, um die Replikation zu stoppen.
Dabei setzten sie das Enzym Crispr/Cas13b ein. Es bindet bestimmte RNA-Sequenzen des Virus und schaltet denjenigen Teil aus, den es braucht, um sich in der infizierten Zelle zu vermehren.
Eine Replikation konnte zu über 98 Prozent verhindert werden
„Sobald das Virus erkannt wird, wird das Crispr-Enzym aktiviert und zerschneidet das Virus”, berichtete Prof. Sharon Lewin, Direktorin vom Doherty Institute. Eine Replikation von SARS-CoV-2 konnte demnach zu mehr als 98 Prozent verhindert werden. „Die Flexibilität von CRISPR-Cas13b - das nur die virale Sequenz benötigt - impliziert, dass wir schnell antivirale Mittel für COVID-19 und alle neu auftretenden Viren entwickeln können”, sagte Lewin.
Die Methode erwies sich auch bei Virusvarianten wie Alpha als wirksam. Bislang wurde sie jedoch nur unter Laborbedingungen getestet. Das Forscherteam will sie nun auch an Tieren erproben. Erst danach wären klinische Studien möglich. Bis die Geneschere bei der Behandlung von Menschen zum Einsatz kommen könnte, wird es daher wohl noch einige Jahre dauern.
Fareh, M., Zhao, W., Hu, W. et al. Reprogrammed CRISPR-Cas13b suppresses SARS-CoV-2 replication and circumvents its mutational escape through mismatch tolerance. Published in Nature Communications on 13. Juli 2021. DOI: doi.org/10.1038/s41467-021-24577-9
9. JULI
----------------------------------
Long-COVID: 77 Prozent hatten nach einem Jahr noch Symptome
Wissenschaftler vom Universitätsklinikum Heidelberg haben 96 Long-COVID-Patienten für ein Jahr lang begleitet, nur 23 Prozent von ihnen waren am Ende symptomfrei.
Nur 23 Prozent der Long-COVID-Patienten hatten zwölf Monate nach ihrer Erkrankung keine Symptome mehr. Die häufigsten Symptome waren verminderte körperliche Leistungsfähigkeit (56,3 Prozent), Müdigkeit (53,1 Prozent), Dyspnoe (37,5 Prozent), Konzentrationsprobleme (39,6 Prozent), Wortfindungsprobleme (32,3 Prozent) und Schlafprobleme (26,0 Prozent). Frauen zeigten signifikant mehr neurokognitive Symptome als Männer.
Alle Probanden waren vor mindestens fünf Monaten an COVID-19 erkrankt. 32,3 Prozent der Teilnehmenden waren hospitalisiert und mehr als 55 Prozent Frauen. Die Forscher untersuchten die antinukleären Antikörper (ANA), den Sars-CoV-2-Antikörperspiegel und die allgemeine Lebensqualität der Patienten. Bei ANA handelt es ich um Autoantikörper, die das Immunsystem gegen Kernbestandteile der eigenen Körperzelle bildet.
Im Vergleich zu symtomfreien Patienten unterschieden sich Patienten mit mindestens einem Long-COVID-Symptom nach zwölf Monaten nicht signifikant in Bezug auf ihre SARS-CoV-2-Antikörperspiegel, hatten aber eine signifikant reduzierte physische und psychische Lebensqualität.
Daher schlussfolgert das Forscherteam, dass neurokognitive Long-COVID-Symptome mindestens ein Jahr nach Beginn der COVID-19-Symptome andauern können und die Lebensqualität signifikant reduzieren. Mehrere neurokognitive Symptome waren mit ANA-Titererhöhungen assoziiert. Dies könnte auf Autoimmunität als Kofaktor in der Ätiologie von Long-COVID hinweisen.Seeßle, Jessica. et al: „Persistent symptoms in adult patients one year after COVID-19: a prospective cohorte Study" published in Oxford University Presse on Juli 2021: DOI: doi.org/10.1093/cid/ciab611
29. Juni 2021
------------------------------------------Ultraschall-Frequenz zerstört Coronaviren
Forschende aus den USA haben die mechanische Reaktion des Virus SARS-CoV-2 auf Ultraschall-Vibrationen geprüft und dabei die schädigende Wirkung auf dessen Hülle und Spike-Proteine entdeckt.Eine Studie am Massachusetts Institute of Technology (MIT) in Cambridge, USA, hat belegt, dass Ultraschallwellen das Coronavirus schädigen und zerstören können. Mithilfe von Computersimulationen haben die Forschenden die mechanische Reaktion des Virus auf Ultraschall-Vibrationen im Frequenzbereich medizinischer Bildgebung getestet. Innerhalb von Sekundenbruchteilen zerstörten die Vibrationen sowohl die Hülle als auch die charakteristischen Spike-Proteine des Coronavirus.Das Team des MIT fand heraus, dass das Virus bei Vibrationen zwischen 25 und 100 Megahertz innerhalb eines Bruchteils einer Millisekunde kollabiert und sich brechen lässt. Der Effekt wurde in Simulationen des Virus in Luft und in Wasser beobachtet. „Die Ergebnisse sind vorläufig und basieren auf begrenzten Daten bezüglich der physikalischen Eigenschaften des Virus“, schreiben die Autoren in ihrer Stellungnahme zur Studie. Dennoch seien die Ergebnisse ein erster Hinweis auf eine mögliche ultraschallbasierte Behandlung von Coronaviren, einschließlich des neuen SARS-CoV-2-Virus und dessen Varianten. Sie beschreiben außerdem die Vision, dass Miniatur-Ultraschallwandler, die in Telefone und andere tragbare Geräte eingebaut werden, Menschen vor dem Virus schützen könnten.
Bislang wurde Ultraschall in der Diagnostik bei COVID-Patienten eingesetzt. Zum Beispiel, um die Schädigungen des Lungengewebes zu erkennen. Außerdem soll ein Ultraschallbad mit der richtigen Reinigungssubstanz gegen Coronaviren wirksam sein.
Wierzbicki, T. et al: „Effect of receptors on the resonant and transient harmonic vibrations of Coronavirus“ published in Journal of the Mechanics and Physics of Solids on May 2021: DOI: doi.org/10.1016/j.jmps.2021.104369
23. Juni 2021
------------------------------------------
Sommer senkt Ansteckungsrisiko um 40 Prozent
Im Sommer ist Sars-CoV-2 bis zu 40 Prozent weniger ansteckend als im Winter. Zu diesem Ergebnis kommt ein Team der University of Oxford.
Um den Einfluss der Jahreszeiten auf das Infektionsgeschehen zu bestimmen, werteten die Forscher der University of Oxford in dem Projekt „EpidemicForecasting.org“ Daten aus 143 gemäßigten Regionen in Europa aus und ließen dabei Faktoren wie Maskenpflicht und Kontaktbeschränkungen außen vor.
Im Ergebnis liegt das Risiko einer Ansteckung im Winter um 40 Prozent höher als im Sommer. Das ist den Wissenschaftlern nach auch eine Erklärung für die heftige zweite Welle in Europa. Der saisonale Effekt ist demnach doppelt so stark zu bewerten, wie bislang angenommen; er ist vergleichbar mit den effektivsten Maßnahmen gegen die Virusausbreitung. Miteinander kombiniert haben die Maßnahmen allerdings einen größeren Effekt als die Jahreszeit.
Die Forscher weisen außerdem darauf hin, dass der Sommer allein nicht ausreiche, um die Pandemie in Schach zu halten. Vielmehr brauche es weiter die Kombination von Schutzmaßnahmen und Impfungen, um die Infektionszahlen einzudämmen. Andernfalls werde es auch weiter zu Ausbrüchen kommen, wie sie auch in wärmeren Region bis zu den Tropen stattfinden. Die Analyse umfasse jedoch ausschließlich europäische Daten und zeige nicht den unmittelbaren Zusammenhang zwischen der Virusverbreitung und dem Wetter.
Gavenčiak, T. et al: „Seasonal variation in SARS-CoV-2 transmission in temperate climates“ as Preprint on MedRxiv on June 13, 2021. https://www.medrxiv.org/content/10.1101/2021.06.10.21258647v1
22. Juni 2021
------------------------------------------
Bandwurmmittel gegen SARS-CoV-2?
Die Berliner Charité untersucht die Wirksamkeit des Bandwurmmittels Niclosamid bei Menschen. Die Wissenschaftler hatten zuvor entdeckt, dass der Wirkstoff die Vermehrung des Virus in den Zellen hemmt.
Am Deutschen Zentrums für Infektionsforschung (DZIF) an der Universitätsmedizin Berlin und der Universität Bonn haben Forschende den Stoffwechsel von SARS-CoV-2 in infizierten Zellen und im Lungengewebe von COVID-19-Patienten analysiert. Hierbei stellten sie fest, wie das Virus die Zellen zu seinem Vorteil umprogrammiert und sich so einfach vermehren kann.
Das neue Coronavirus drosselt das zelleigene Recycling
Für ihre Vermehrung sind Viren von der Maschinerie der Wirtszelle abhängig und nutzen deren molekulare Bausteine. Gleichzeitig müssen sie es schaffen, den zellurären Überwachungssensoren des Immunsystems zu entgehen, um nicht aufzufallen und sich ungehindert vervielfältigen zu können. Dafür manipulieren die Viren die Wirtszellen. Das neue Coronavirus drosselt dabei den zelleigenen Recycling-Mechanismus – die sogenannte Autophagie. Dieser Prozess der „Selbstverdauung“ dient dazu, molekulare Bausteine für neue Zellstrukturen zu produzieren, indem beschädigtes Zellmaterial und Abfallprodukte abgebaut werden.
Niclosamid zeigte den größten antiviralen Effekt
Im weiteren Schritt prüften die Forschenden daher, ob Substanzen, die das Zell-Recycling ankurbeln, die Vermehrung von SARS-CoV-2 in Wirtszellen bremsen können. Sie identifizierten vier Wirkstoffe: die körpereigenen Stoffe Spermin und Spermidin, das experimentelle Krebsmedikament MK-2206 und das Bandwurmmittel Niclosamid. Niclosamid zeigte den größten antiviralen Effekt und senkte die Produktion infektiöser Partikel um mehr als 99 Prozent. Das zugelassene Mittel gilt als gut verträglich.
Nun soll in der Phase II-Studie geprüft werden, ob das Präparat auch bei Menschen gegen das Virus wirkt. „Wir konnten in unserer Studie zeigen, dass SARS-CoV-2 zwar die Bausteine der Zellen für seine eigenen Zwecke nutzt, ihnen gleichzeitig aber auch Nahrungsreichtum vortäuscht und damit das zelluläre Recycling bremst“, berichtet der Erstautor der Studie Dr. Nils Gassen.
Gassen NC et al. „SARS-CoV-2-mediated dysregulation of metabolism and autophagy uncovers host-targeting antivirals“ published in Nature Communications on June 21, 2021. doi: 10.1038/s41467-021-24007-w
16. Juni 2021
------------------------------------------
SARS-CoV-2 schädigt körpereigene Bakterien in Darm und Lunge
Eine schwere COVID-Erkrankung kann zu einer Veränderung des Mikrobioms führen und die Darmflora so aus dem Gleichgewicht bringen. Welche Faktoren das begünstigen und welche Auswirkungen das auf die Immunabwehr der Patienten hat, erklären Wissenschaftler in einem Review aus der Intensivmedizin.
Bei rund einem Drittel der an COVID-19 erkrankten Patienten ist eine intensivmedizinische Behandlung notwendig. Sie weisen häufig eine durch den hyperinflammatorischen Zustand gesteigerte Immunreaktion auf, welche im Zusammenhang mit dem stark veränderten Mikrobiom, der sogenannten Dysbiose, stehen kann. Da der Darm mit der Lunge in einer bidirektionalen Verbindung steht, können sich die Stoffwechselprodukte hier gegenseitig beeinflussen. Die Bakterien im Darm regulieren dabei sowohl das hier ansässige Immunsystem als auch das im Lungengewebe. Intakt fungiert das Mikrobiom somit als direkte Abwehr von SARS-CoV-2.
Bei einer schweren COVID-Erkrankung kann die Darmflora jedoch empfindlich aus dem Gleichgewicht geraten und das bereits nach wenigen Tagen der Infektion, stellten Studien zuvor fest. Kommen Medikamente wie Antibiotika oder Sedativa hinzu, kann dies noch verstärkt werden. Nun veröffentlichten Forschende aus Brasilien ihre Erkenntnisse zur Schädigung der körpereigenen Bakterien durch das Virus aus einer Literaturstudie. Als Intensiv- und Ernährungsmediziner empfehlen sie im Anschluss an eine schwere Infektion eine Mikrobiom-fokussierte Ernährung sowie Prä- und Probiotika.
US-Studie zu COVID-19 und Ernährung
Ernährung beeinflusst den Krankheitsverlauf
Eine vorwiegend pflanzenbasierte Ernährung kann vor einem schweren Verlauf einer COVID-19-Infektion schützen, fanden US-amerikanische Wissenschaftlerinnen und Wissenschaftler heraus.
Weitere Aspekte, die zur Veränderung des Mikrobioms bei schweren COVID-Erkrankungen führen, sehen die Autoren in der Medikamenteneinnahme, der Körperposition während einer intensivmedizinischen Behandlung sowie der invasiven mechanischen Beatmung und der künstlichen Ernährung der Patienten im Krankenhaus. Hinzu kommen die häufig vorliegenden Vorerkrankungen wie Diabetes und starkes Übergewicht, die selbst bereits eine Veränderung des Mikrobioms mit sich bringen. Ist das Gleichgewicht gestört, ist auch die Immunabwehr beeinträchtig, warnen die Autoren.
Battaglini, D. et al.: „The Role of Dysbiosis in Critically Ill Patients With COVID-19 and Acute Respiratory Distress Syndrome“ published in Front. Med. on June 4, 2021. https://www.frontiersin.org/articles/10.3389/fmed.2021.671714/full
14. Juni 2021
------------------------------------------
Profitieren Kinder von den Impfungen der Erwachsenen?
Aktuelle Daten aus mehreren Ländern zeigen, dass der Impfeffekt der Erwachsenen auch Kindern nutzen kann. Denn die Infektionen unter der jungen Bevölkerungsgruppe gehen ebenfalls signifikant zurück, auch wenn diese selbst noch nicht geimpft ist.Da Kinder und Jugendliche bislang noch nicht Teil der weltweiten Impfkampagne sind, schauen Wissenschaftler gespannt auf das Ansteckungsgeschehen bei ihnen. Trifft sie nun häufiger eine Infektion, weil sie anders als viele Erwachsene noch nicht immunisiert sind? Oder haben auch sie einen Vorteil von der entstehenden Herdenimmunität? Erste Datenauswertungen dazu haben Epidemiologen im Fachmagazin Nature zusammengetragen. Doch die Schlussfolgerungen fallen unterschiedlich aus.In der brasilianischen Kleinstadt Serrana im Bundesstaat São Paulo, in der 98 Prozent der Erwachsenen mit CoronaVac von Sinovac geimpft wurden, sahen die Forschenden auch bei ungeimpften Kindern einen auffälligen Rückgang der symptomatischen Infektionen. Ähnlich verhält sich das Infektionsgeschehen unter Kindern und Jugendlichen in Ländern wie Israel und den USA, wo die Impfquote unter den Erwachsenen hoch ist. In den USA ging die Infektionsquote bei unter 18-Jährigen zwischen den Monaten Januar und Mai 2021 um 84 Prozent zurück. Rund 50 Prozent der erwachsenen US-Amerikaner sind geimpft.
"Eine unserer Befürchtungen war, dass, wenn man alle anderen impft, sich die Krankheit wahrscheinlich auf die Kinder und Jugendlichen konzentrieren wird", erklärt der Epidemiologe Ricardo Palacios im Beitrag. Aber diese bestätigte sich bislang nicht. Der Effekt der Herdenimmunität könnte also auch für nicht geimpfte Kinder von Bedeutung sein - und könnte darauf hindeuten, dass Kinder meistens von Erwachsenen angesteckt werden, schreiben die Experten.
Anderes zeigen allerdings die Auswertungen von Daten aus Großbritannien. Dort liegt die Impfrate bei rund 60 Prozent unter den Erwachsenen. Kinder spielen hier als Verteiler des Virus jedoch weiterhin eine Rolle. So gab es im Mai 2021 erneut 100 Infektionsausbrüche in den 25.000 Grund- und Sekundarschulen in England, nachdem die Infektionen zuvor stark zurückgegangen waren. Allerdings sind auch die Daten nicht vollumfänglich repräsentativ und beleuchten nur einen Teil der Bevölkerungsgruppe. In jedem Fall spielen die Erkenntnisse eine Rolle bei der Entwicklung der Pandemie und der Entscheidung, ob Kinder auch zügig gegen COVID-19 geimpft werden sollten.
„Does vaccinating adults stop kids from spreading COVID too?“ published in Nature on June 10, 2021. doi: https://doi.org/10.1038/d41586-021-01549-z
11. Juni 2021
------------------------------------------
Chronisch obstruktive Lungenerkrankung (COPD) und COVID-19
Hat die chronisch obstruktive Lungenerkrankung (COPD) Einfluss auf die Mortalität von COVID-Patienten und begünstigt das Homeoffice die Erkrankung? In zwei Studien wurde das untersucht.
Für eine retrospektive Vergleichsstudie analysierten Wissenschaftler aus der Türkei die Daten von rund 1.000 Patienten mit einer gesicherten SARS-CoV-2-Infektion und untersuchten, wie viele davon zusätzlich an der chronischen obstruktiven Lungenerkrankung (COPD) litten. Die knapp fünf Prozent der COVID-19-Patienten, die auch eine COPD aufwiesen, zeigten einige prognostisch ungünstige Faktoren, jedoch war die Mortalität unter ihnen nicht signifikant erhöht. Weitere signifikante Vohersagefaktoren für die Mortalität von COVID-19-Patienten waren der Studie nach ein höheres Alter, Lymphopenie, Hypoxämie und Lungenentzündung.Ob die Heimarbeit, die viele Arbeitnehmer während der Pandemie aufnahmen, einen Einfluss auf COPD hat, untersuchten Wissenschaftler anhand von Daten einer umfangreichen Querschnittsstudie aus der chinesischen Provinz Sichuan. Darin gaben die Teilnehmer Auskunft über ihr sitzendes Verhalten und ihre chronischen Erkrankungen. Die Forschenden interessierten sich für einen möglichen Zusammenhang zwischen der chronischen Erkrankung und dem zunehmenden Sitzen. Dabei fanden sie heraus, dass Personen, die länger als sieben Stunden am Tag saßen, ein etwa doppelt so hohes Risiko hatten, an COPD zu erkranken, als Personen, die weniger als drei Stunden am Tag im Sitzen verbrachten.
Turan, O. et al: „Clinical characteristics and outcomes of hospitalized COVID-19 patients with COPD“. Expert Rev Respir Med. 2021 May 4. doi: 10.1080/17476348.2021.1923484
Lei Y, Z. et al.: „Sedentary behavior is associated with chronic obstructive pulmonary disease: A generalized propensity score-weighted analysis“. Medicine (Baltimore). 2021 May 7. doi: 10.1097/MD.0000000000025336. PMID: 33950922.
8. Juni 2021
------------------------------------------
Kinder und Jugendliche mit Grunderkrankungen neigen zu schwerem Verlauf
Eine aktuelle US-Studie zeigt, dass Kinder mit Typ-1-Diabetes, angeborenen Herz- und Kreislaufanomalien, Adipositas, Bluthochdruck, Epilepsie, neuropsychiatrischen Störungen und Asthma sowie chronischen Erkrankungen ein erhöhtes Risiko für eine Hospitalisierung oder einen schwere Verlauf bei COVID-19 haben.
Forschende des US-amerikanischen Centers for Disease Control (CDC) haben mittels einer Querschnittstudie die Daten von etwa 43.465 COVID-Patienten im Alter von 18 Jahren oder jünger analysiert, die während März 2020 und Januar 2021 in die Notaufnahme von US-Kliniken eingeliefert wurden. Die Daten stammen aus der Premier Healthcare-Datenbank (PHD) von mehr als 800 US-Krankenhäusern. 28,7 Prozent der Kinder und Jugendlichen wiesen eine Grunderkrankung auf. Zu den am häufigsten diagnostizierten Erkrankungen gehörte hierbei Asthma mit 10,2 Prozent gefolgt von neurologischen Entwicklungsstörungen bei 3,9 Prozent sowie Angststörungen bei 3,2 Prozent. Bei weiteren 2,8 Prozent lang eine diagnostizierte depressive Störungen vor, bei 2,5 Prozent Adipositas. Die bedeutendsten Risikofaktoren für einen Krankenhausaufenthalt waren laut der Datenauswertung ein Diabetes Typ 1 (bereinigtes Risikoverhältnis [aRR]: 4,60) und Adipositas (aRR: 3,07). Weiter zählen zu den Risikofaktoren für eine schwere COVID-Erkrankung angeborene Herz- und Kreislaufanomalien (aRR: 1,72). Unter Kindern, die jünger als zwei Jahre waren, hatten Frühgeburten ein höheres Risiko für COVID-19 (aRR: 1,83). Vor allem Kinder mit chronischen und komplexen chronischen Erkrankungen hatten ein 2,91- beziehungsweise 7,86-faches erhöhtes Risiko für einen Krankenhausaufenthalt. Bereits hospitalisierte Kinder mit chronischen Erkrankungen hatten eine bis zu 2,86-fache höhere Wahrscheinlichkeit für einen schweren COVID-19-Verlauf im Vergleich zu Kindern und Jugendlichen ohne Vorerkrankungen. Die Studie fand im Ergebnis ein höheres Risiko für eine schwere COVID-Erkrankung bei Kindern und Jugendlichen mit bestimmten Grunderkrankungen zu denen beispielsweise Diabetes Typ 1, angeborenen Herz- und Kreislaufanomalien und Adipositas zählen. Diese Erkenntnisse können Ärzte für das klinische Management von Kindern mit COVID-19 in Betracht ziehen.
Kompaniyets, L. et al. „Underlying Medical Conditions Associated With Severe CO-VID-19 Illness Among Children.“ published in Jama Network Open on June 7, 2021. doi:10.1001/jamanetworkopen.2021.11182
7. Juni 2021
------------------------------------------
Antikörper-Nasenspray schützt im Mäuseversuch gegen COVID-19
US-Wissenschaftler entwickelten einen hybriden Antikörper, der per Nasenspray verabreicht in der Lunge von Mäusen wirksam SARS-CoV-2 bekämpfen kann.
Das Forscherteam kombinierte Fragmente von IgG- und IgM-Antikörpern, die als schnelle Ersthelfer für eine breite Palette von Infektionen fungieren. Die entwickelten IgMs hatten gegenüber mehr als 20 Varianten von SARS-CoV-2 eine viel stärkere „neutralisierende“ Wirkung als die IgGs allein.
Das Nasenspray wurde den Mäusen sechs Stunden vor der Infektion in fünf unterschiedlichen Dosierungen (3,5; 1,2; 0,4; 0,13 und 0,044 mg/kg) oder sechs Stunden nach der Infektion in drei Dosierungen (3,5; 1,2 und 0,4 mg/kg) verabreicht. Zwei Tage nach der Infektion wurde dann die Virusmenge in der Lunge der Nagetiere untersucht.Ergebnis: Bei den Tests zur prophylaktischen Behandlung wurde die Viruslast in der Lunge in den Gruppen
3,5mg/kg bei 90 Prozent der Mäuse auf ein nicht nachweisbares Maß reduziert.
1,2 mg/kg bei 70 Prozent der Mäuse auf ein nicht nachweisbares Maß reduziert.
0,4 mg/kg bei 90 Prozent der Mäuse auf ein nicht nachweisbares Maß reduziert.
0,13 mg/kg bei 60 Prozent der Mäuse auf ein nicht nachweisbares Maß reduziert.
Bei der Dosis von 0,044 mg/kg war die mediane Viruslast noch signifikant (etwa fünffach) gegenüber der Vergleichsgruppe reduziert.Bei den Tests der therapeutischen Leistungsfähigkeit des Sprays war die mediane Viruslast um das 13.6-fache (Dosen 3,5 mg/kg und 1,2 mg/kg) beziehungsweise um das 56-fache (0,4 mg/kg) gegenüber der Vergleichsgruppe reduziert. Fazit der Autoren: Die Daten zeigen, dass das Nasenspray bereits bei Dosen von nur 0,044 mg/kg zur prophylaktischen und 0,4 mg/kg zur therapeutischen Behandlung von COVID-19 geeignet sei. Ku, Z., Xie, X., Hinton, P.R. et al. „Nasal delivery of an IgM offers broad protection from SARS-CoV-2 variants.“ Nature (2021). https://doi.org/10.1038/s41586-021-03673-2
3. Juni 2021
------------------------------------------
Vitamin C könnte bei COVID-Fatique helfen
Eine Studie zeigt, dass hochdosiertes Vitamin C bei Krebs-, Allergie- und OP-Patienten chronische Müdigkeit reduziert – und legt nahe, dass es auch bei Long COVID-Patienten hilft.
Mit einer systematischen Literaturrecherche untersuchten Forschende der Universität Rostock die Wirksamkeit von hochdosiertem Vitamin C bei postviraler Fatigue, insbesondere als Symptom von Long COVID. Ausgewertet wurden neun klinische Studien mit insgesamt 720 Teilnehmern.
In den meisten Studien wurde der Effekt von Vitamin C auf Fatigue bei Krebspatienten beobachtet. Eine Studie untersuchte den Effekt auf Fatigue nach einer Herpes zoster-Infektion, eine bei Allergie, eine nach Operationen und eine bei gesunden Angestellten. Dabei wurde Vitamin C jeweils intravenös in Dosierungen von 3,5 g bis zu mehr als 75 g pro Tag verabreicht.
Ergebnis: Drei der vier kontrollierten Studien beobachteten eine signifikante Abnahme der Ermüdungswerte in der Vitamin-C-Gruppe im Vergleich zur Kontrollgruppe. Vier der fünf Beobachtungs- oder Vorher-Nachher-Studien belegen eine signifikante Verringerung der Ermüdungserscheinungen. Auch Begleiterscheinungen der Müdigkeit wie Schlafstörungen, Konzentrationsmangel, Depressionen und Schmerzen wurden häufig gelindert.
Schlussfolgerung der Autoren: Da oxidativer Stress, Entzündungen und Durchblutungsstörungen – die wichtige Faktoren für Müdigkeit sind – ebenfalls mit Fatigue als Long COVID-Symptom in Verbindung gebracht werden, könnte eine hochdosierte Vitamin C-Gabe eine geeignete Behandlungsoption sein. Ihre Empfehlung: Klinischen Studien sollten die Auswirkungen von hochdosiertem IV-Vitamin C auf mit Long COVID assoziierte Müdigkeit untersuchen.
Vollbracht C, Kraft K. Feasibility of Vitamin C in the Treatment of Post Viral Fatigue with Focus on Long COVID, Based on a Systematic Review of IV Vitamin C on Fatigue. Nutrients. 2021;13(4):1154. Published 2021 Mar 31. doi:10.3390/nu13041154
2. Juni 2021
------------------------------------------
Covid-19 kann Diabetes auslösen
Diabetes gilt als Risikofaktor für einen schweren COVID-19-Verlauf. Dass eine Infektion mit SARS-CoV-2 umgekehrt auch Diabetes auslösen kann, zeigt eine Studie der Stanford University School of Medicine.
Etwa 15 Prozent Covid-19-Patienten entwickeln im Zuge der Infektion einen Diabetes. Eine internationale Studie der Stanford University School of Medicine mit Beteiligung der Universität Basel hat entschlüsselt, wie das Coronavirus die insulinproduzierenden Beta-Zellen der Bauchspeicheldrüse befällt und zerstört. Beta-Zellen produzieren das Hormon Insulin, das Gewebezellen dazu anregt, Zucker aus dem Blut aufzunehmen - und dadurch den Blutzucker zu senken.
Das Virus wählt eine alternative Eintrittspforte
Im Lungengewebe nutzt Coronavirus vor allem das Protein ACE2 als Eintrittspforte in die Zellen. Da die Beta-Zellen der Bauchspeicheldrüse aber nur geringe Mengen an ACE2 aufweisen, war bisher unklar, ob und wie das Virus in diese Zellen eindringt.
Die Forscher untersuchten deshalb Gewebeproben sieben verstorbener Covid-19-Patientinnen und -Patienten aus Basel
–
und konnten in den Beta-Zellen der Bauchspeicheldrüse der Verstorbenen SARS-CoV-2 nachweisen. Sie entdeckten dabei, dass diese Zellen große Mengen eines Proteins enthielten, das das Virus alternativ zu ACE2 als Eintrittspforte nutzen kann: Neuropilin 1 (NRP1).
Wird das Protein blockiert, hat es das Virus schwerer
Laborversuche mit kultivierten Beta-Zellen zeigten zudem, dass infizierte Zellen weniger Insulin produzierten und Zeichen des Absterbens aufwiesen. Wurde Neuropilin 1 mit einem Hemmstoff blockiert, gelang es dem Virus viel schlechter, in die Zellen einzudringen. Da sich die Infektion der Beta-Zellen zumindest im Laborversuch so reduzieren ließ, könnte man diese Zellen womöglich auch bei Patienten mit schwerem Covid-19-Verlauf schützen, folgern die Autoren.
Ob sich der Zuckerstoffwechsel wieder normalisiert, ist offen
"Ob sich der Zuckerstoffwechsel nach einer überstandenen Infektion bei allen Covid-19-Patientinnen und -Patienten wieder normalisiert und ob und wie häufig ein bleibender Diabetes entstehen kann, lässt sich nach derzeitiger Studienlage nicht mit Sicherheit sagen", erklärt Pathologe PD Dr. Matthias Matter von der Universität Basel und vom Universitätsspital Basel, Leiter der Anteile der Studie, die in Basel durchgeführt wurden.
Es gebe Hinweise, dass bei Betroffenen mit Long-Covid auch mehrere Wochen bis Monate danach noch ein Diabetes feststellbar sei. Eine Möglichkeit zu entwickeln, bleibende Schäden der Bauchspeicheldrüse zu verhindern, sei daher sinnvoll.
Chien Ting-Wu et al., SARS-CoV-2 infects human pancreatic β-cells and elicits β-cell impairment, Cell Metabolism (2021), doi: 10.1016/j.cmet.2021.05.013
1. Juni 2021
------------------------------------------
Indische Umfrage mit 4.400 Zahnärzten zeigt: Die Impfung schützt
Einer Studie zufolge infizierten sich 9 Prozent aller geimpften indischen Zahnärzte in der zweiten Infektionswelle mit SARS-CoV-2. Der Schutz war unabhängig vom Vakzin und von der Anzahl der Impfdosen.
An der bisher nur als Preprint erschienenen Studie beteiligten sich vom 29. April bis 2. Mai 2021 insgesamt 4.493 indische Zahnärzte. 74,4 Prozent der Befragten waren unter 45 Jahre alt, 51,5 Prozent Frauen. Im Befragungsraum waren 88,1 Prozent der Probanden mindestens einmal mit „Covishield”(Vektorimpfstoff von AstraZeneca) oder „Covaxin” (Todimpfstoff von Bharat Biotech) geimpft. 92,4 Prozent hatten den Impfstoff von AstraZeneca erhalten, während 7,5 Prozent das Vakzin von Bharat Biotech verimpft bekamen.
Ergebnis: Von den Befragten hatten sich 9,1 Prozent (n=364) der Geimpften und 14,6 Prozent (n = 78) der Ungeimpften in der zweiten Infektionswelle in Indien mit SARS-CoV-2 angesteckt. Zum Umfragezeitpunkt hatten 60,2 Prozent der Befragten beide Impfstoffdosen erhalten. Von Ihnen infizierten sich 9,2 Prozent derjenigen, die Covishield und 8,3 Prozent, die Covaxin erhalten hatten. Der Unterschied zwischen der Schutzfähigkeit war statistisch nicht signifikant.
Die Autoren kommen zu dem Schluss, dass Impfungen in der zweiten indischen Infektionswelle über alle Altersgruppen hinweg eine entscheidende Rolle bei der Verringerung der Positivitätsrate in der Zahnärzteschaft spielten.
Sie schreiben: „Eine einzelne Impfdosis scheint hinsichtlich der Infektionvorbeugung mit SARS-CoV-2 genauso wirksam zu sein wie zwei Impfdosen.” Weiteres Detail: Mit ihrer Impfquote von mehr als 88 Prozent (bei den über 45-Jährigen mehr als 95 Prozent) seien indische Zahnärzte außergewöhnlich starke Impfbefürworter. Bis zum 19. April 2021 waren dagegen weniger als 50 Prozent aller besonders exponierten Mitarbeiter des indischen Gesundheitswesens geimpft.
Sanjeev Kumar et al. „Effectiveness of the Covid-19 vaccine in preventing infection in dental practitioners – results of a cross-sectional ‘questionnaire-based’ survey“ medRxiv 2021.05.28.21257967; doi: https://doi.org/10.1101/2021.05.28.21257967
26. Mai 2021
------------------------------------------
Kinder weisen eine ähnlich hohe Viruslast im Rachen wie Erwachsene und sind somit genauso ansteckend. Die überarbeitete Studie von Prof. Christian Drosten bestätigt seine Ergebnisse von 2020 zur Infektiosität von Kindern.
Im vergangenen Frühjahr löste die Studie unter der Leitung von Drosten, Direktor des Instituts für Virologie der Charité, eine Kontroverse aus. Sie hatte offengelegt, dass Kinder ähnlich ansteckend sind wie Erwachsene und wurde als Entscheidungshilfe für die Schul- und Kitaschließungen verwendet. Kritisiert wurde damals, dass wegen einer zu groben statistischen Methodik die Studie nicht vollständig repräsentativ sei.
Die Jüngsten sind nicht so ansteckend
Nun erschien die Studie überarbeitet und deutlich umfangreicher im Fachmagazin Science. Drosten und sein Team bleiben darin bei ihren bisherigen Ergebnissen. Zur Infektiosität von Kindern heißt es: "Die am wenigsten infektiösen, jüngsten Kinder im Alter von 0 bis fünf Jahren haben 78 Prozent der Spitzenkulturwahrscheinlichkeit von Erwachsenen im Alter von 45 bis 55 Jahren. Die Jüngsten weisen im Durchschnitt mit 800.000 Erbgutkopien eine geringere Viruslast auf. Kinder im Schulalter und Jugendliche weisen Werte auf, die mit denen der Erwachsenen vergleichbar sind."
In den Altersgruppen zwischen 20 und 65 Jahren gibt es demnach keinen signifikanten Unterschied bei der festgestellten Viruslast. Den höchsten Wert weisen im Durchschnitt Infizierte der Altersgruppe ab 65 Jahren auf. Die Viruslast liegt hier bei etwa 2,5 Millionen Kopien.
Alle Altersgruppen sind gleich infektiös
Um festzustellen, ob es einen Zusammenhang zwischen der Viruslast in Proben
und damit eine mögliche Varianz in der Infektiosität gibt, werteten die Wissenschaftler am Virologischen Institut der Charité 25.000 positive PCR-Proben aus. Hierbei wurden die Erbgutkopien gezählt, die näherungsweise die Virusmenge im Rachen der Patienten repräsentieren und somit Voraussagen über deren potenzielle Infektiosität zulassen. „Mein anfänglicher Eindruck einer ungefähr gleich großen Infektiosität aller Altersgruppen hat sich bestätigt, nicht nur hier, sondern auch in anderen Studien“, teilte Drosten mit.
Der Virologe weist aber auch drauf hin, dass die Proben von Kindern nicht vollständig mit denen von Erwachsenen vergleichbar sind. Die Stäbchen für die Abstriche sind oft kleiner und werden eher im Rachen denn über den unangenehmeren Weg durch die Nase eingeführt. Deshalb enthalten sie von vornherein weniger Probenmaterial und damit auch weniger Viruslast. Vergleiche zwischen den Viruslasten von Erwachsenen und Kindern und den relativen Infektionsrisiken, die sie darstellen, sind aufgrund nicht-viraler Faktoren schwierig, schreiben die Studienautoren.
Eine Minderheit verursacht größtenteils die Übertragungen
In rund 9 Prozent der untersuchten Proben fiel eine außergewöhnlich hohe Viruslast von einer Milliarde Erbgutkopien oder mehr auf. Dabei zeigten mehr als ein Drittel dieser potenziell hochinfektiösen Personen keine oder nur leichte Symptome. „Diese Daten liefern eine virologische Grundlage für die Beobachtung, dass nur eine Minderheit der Infizierten den größten Teil aller Übertragungen verursacht“, erklärt Drosten.
Unter den Proben befanden sich auch 1.500 Fälle, die die neue Mutation B.1.1.7 aufwiesen. Diese hatten eine zehnfach höhere Viruslast und gelten daher als 2,6-Fach so ansteckend.
Jones, T. C. et al. „Estimating infectiousness throughout SARS-CoV-2 infection course.“ Published in Science on May 25, 2021. doi: 10.1126/science.abi5273
20. Mai 2021
------------------------------------------
BioNTech: Längeres Impfintervall stärkt Antikörperreaktion
Hat die Streckung des Impfintervalls beim Impfstoff von BioNTech/Pfizer Einfluss auf die Qualität der Immunantwort? Eine britische Studie zeigt in ersten Ergebnissen: ja, und zwar einen positiven.
Weil der Impfstoff knapp ist, wurde hat man den Zeitraum zwischen der ersten und der zweiten Dosis des BioNTech/Pfizer-Impfstoffs gestreckt. Der Aufbau der Schutzwirkung wurde davon nicht weiter beeinträchtigt. Doch wie steht es um die Qualität der Immunantwort? Eine Kohorten-Studie aus Birmingham legt nun Ergebnisse vor. Sie zeigen, das längere Dosierungsintervall verstärkt die Antikörperreaktion auf den Impfstoff sogar.
Dafür verglichen die Wissenschaftler des „UK Coronavirus Immunology Consortium“ an der Universität Birmingham die Immunantworten von 172 Probanden über 80 Jahren: Die eine Gruppe mit 99 Personen erhielt die zweite Impfdosis in einem Abstand von drei Wochen, die andere mit 73 Teilnehmer nach elf bis zwölf Wochen. Allen Testpersonen wurden zwei Blutproben jeweils nach fünf bis sechs Wochen und noch einmal nach 13 bis 14 Wochen genommen. DAnn lag der Zeitpunkt der zweiten Impfung entweder bereits zehn bis elf Wochen oder erst zwei Wochen zurück.
Kommt der Boost nach 13 Wochen, fällt er stärker aus
Überraschende Feststellung der Untersuchung: Der Antikörper-Titer der später geimpften Probanden stieg stärkeran (4.030 U/ml), als der der zügig Nachgeimpften (1.138 U/ml). Dieser stärkere Boost könnte die Schutzwirkung zusätzlich verlängern, so die Einschätzung der Wissenschaftler. Denn bei den früher Geimpften sank der Antikörper-Titer bereits wieder um den Faktor 2,6.
Nachteil eines gestreckten Impfintervalls ist allerdings, dass sich der vollständige Impfschutz erst später ausbildet. Die Antikörper-Titer war bei allen Senioren nach der ersten Impfung noch relativ niedrig, ebenso die T-Zellen-Antwort, die mit dem ELISpot-Assay gemessen wurde. Insgesamt war sie nicht deutlich ausgeprägter nach dem längeren Impfintervall.
Die Ergebnisse entkräften die Befürchtung, dass eine späte zweite Dosis den Anstieg der Antikörper-Titer verringern könnte und der gewünschte Boost ausbleibt. Sie stützen Erkenntnisse von Forschern der Universität Oxford einher, die auch einen stärkeren Anstieg der Antikörperreaktion beim Impfstoff von AstraZeneca festgestellt hatten.
Die Aussagekraft der Studie ist dahingehend eingeschränkt, dass bisher noch nicht klar ist, wie viele Antikörper ein Infizierter benötigt, um eine SARS-CoV-2-Infektion abzuwehren beziehungsweise nicht an COVID-19 zu erkranken.
Helen M Parry, H. M. et al: „Extended interval BNT162b2 vaccination enhances peak antibody generation in older people“ published on medRxiv on May 71, 2021. DOI: https://www.medrxiv.org/content/10.1101/2021.05.15.21257017v1
19. Mai 2021
------------------------------------------
Antivirale Nasentropfen können COVID-19-Schutz erhöhen
Interferon-Alpha-Nasentropfen können zusätzlich zu Schutzausrüstung und Hygienevorkehrungen effektiv den COVID-19-Schutz für medizinisches Personal erhöhen. Dazu genügen zwei bis drei Tropfen 4-mal täglich.
Die prospektive klinische Studie mit paralleler Interventionszuweisung wurde in einer frühen Phase der Pandemie (21. Januar 2020 bis 30. Juli 2020) mit Ärztinnen und Ärzten sowie Pflegepersonal des Taihe Hospital, Provinz Hubei, China, durchgeführt. Die 2.944 Probanden wurden in zwei Gruppen mit geringem (n=2.415) und hohem Infektionsrisiko (n=529) entsprechend ihrem Grad der direkten Exposition gegenüber COVID-19-Patienten einteilt.
Die Personen der Niedrigrisiko-Gruppe erhielten 4-mal täglich Nasentropfen (zwei bis drei Tropfen pro Nasenloch) mit antiviral wirksamen, körpereigenen Interferon-Alpha (IFN-α) zusätzlich zu OP-Masken und Handhygiene. Die Hochrisiko-Gruppe erhielt eine Kombination von IFN-α-Nasentropfen mit wöchentlich einer subkutanen Injektion von Thymosin-α1 (1,6 mg) zusätzlich zu Schutzkleidung mit Sicherheitsbrille oder Gesichtsschild, Atemschutzmaske und Handschuhen.
Alle Teilnehmer wurden 30 Tage beobachtet und nach Abschluss der Testphase mittels Computertomografie (CT) auf Anzeichen einer COVID-19-Pneumonie untersucht. Außerdem dokumentierten die Forscher mögliche Nebenwirkungen.
Blick auf die Studienlage
Welches Potenzial haben Nasensprays gegen SARS-CoV-2?
Für ausgewählte Mundwasser ist erwiesen, dass sie temporär die Viruslast im Mund-Rachen-Raum wirksam reduzieren können. Nun rückt das Potenzial von Nasensprays verstärkt in den Fokus.
Ergebnis: Im Beobachtungszeitraum trat in keiner Gruppe eine COVID-19-Pneumonie auf, die Lungen-CT-Scans waren negativ. Sämtliche Probanden blieben ohne klinische Symptome. Es wurde kein schwerwiegendes unerwünschtes Ereignis beobachtet.
Schlussfolgerung: Zusammen mit den Standard-Schutzmaßnahmen können rhIFN-α Nasentropfen auch stark exponiertes medizinische Personal effektiv vor COVID-19-Lungenentzündung schützen. Die Studie hatte keine Kontrollgruppe, konnte also keinen direkten Wirksamkeitsnachweis erbringen. Die Autoren verweisen jedoch darauf, dass im Beobachtungszeitraum in derselben Region insgesamt 2.035 medizinische Angestellte an COVID-19 erkrankten, die keine zusätzlichen Nasentropfen oder Nasentropfen plus Injektion erhielten.
Zhongji Meng et al. „The effect of recombinant human interferon alpha nasal drops to prevent COVID-19 pneumonia for medical staff in an epidemic area”. Curr Top Med Chem. 2021 Apr 28. doi: 10.2174/1568026621666210429083050.
17. Mai 2021
------------------------------------------
Kombination von zwei Impfstoffen erhöht Impfreaktionen
Fieber, Schüttelfrost, Müdigkeit – wer bei Erst- und Zweitimpfung verschiedene Vakzine bekommt, erleidet verstärkt Impfreaktionen. Das zeigt eine multizentrische Studie aus Großbritannien.
Die Prime-Boost COVID-19-Impfstudie vergleicht alle vier Impfstoff-Kombinationen von Vaxzevria (AstraZeneca) und Comirnaty (BioNTech/Pfizer) in Impfabständen von 28 und 84 Tagen. Die 830 Probanden waren 50 Jahre und älter ohne oder leicht bis mäßig, gut kontrollierte Komorbiditäten. Sie wurden von Mitte bis Ende Februar 2021 an acht Standorten in Großbritannien rekrutiert.
Kombination aus AstraZeneca und BioNTtech/Pfizer erzielt höhere Wirksamkeit
Erste Zwischenergebnisse einer klinischen Phase-II-Studie zu kombinierten Impfungen des spanischen Gesundheitsministeriums zufolge soll die Kombination aus Erstimpfung mit AstraZeneca und Zweitimpfung mit BioNTech/Pfizer eine höhere Wirksamkeit aufweisen. Bisher gibt es kaum ausreichend Daten zur Wirksamkeit dieser Kombination.
An dieser Studie haben 679 Freiwilligen im Alter von 18 bis 59 Jahren teilgenommen, die als Erstimpfung AstraZeneca erhielten. Etwa 450 Personen davon bekamen als zweite Dosis BioNTtech/Pfizer geimpft. Laut den Zwischenergebnissen, war das Antikörperniveau bei der zweiten Dosis mit dem Biontech-Impfstoff zwischen 30- und 40-mal höher war als bei einer Kontrollgruppe, der nur mit einer Dosis von AstraZeneca geimpft wurde. Infolge der Kombination der beiden Impfstoffe stiege laut dem spanischen Gesundheitsministerium nicht nur die Wirksamkeit, sondern auch das Niveau neutralisierender Antikörper.
Nach der zweiten Dosis mit dem BioNTech/Pfizer-Impfstoff war es um mehr als das Siebenfache angestiegen. Nach der zweiten Impfdosis mit AstraZeneca lag nur eine Verdoppelung vor. Nur 1,7 Prozent der Probanden berichteten von Nebenwirkungen, die im Zusammenhang mit den Impfungen auftraten. Die häufigsten Nebenwirkungen waren Kopfschmerzen, Unwohlsein, Schüttelfrost, leichte Übelkeit und Fieber.
In die Zwischenauswertung flossen nur Daten nach 28-tägigem Impfintervall ein: In Gruppen mit homologen Impfplänen war die Reaktogenität in der AstraZeneca-Gruppe nach der ersten Dosis größer, in der BioNTech-Gruppe nach der Boost-Dosis. Beide heterologen Impfpläne induzierten eine größere Reaktogenität nach der Boost-Dosis als ihre homologen Pendants. So wurde etwa Fieber berichtet von:
41 Prozent der BioNTech/AstraZeneca-Gruppe,
21 Prozent der BioNTech/BioNTech-Gruppe,
34 Prozent der AstraZeneca/BioNTech-Gruppe,
10 Prozent der AstraZeneca/AstraZeneca-Gruppe.
Ähnliche Zunahmen wurden bei Schüttelfrost, Müdigkeit, Kopfschmerzen, Gelenkschmerzen, Unwohlsein und Muskelschmerzen beobachtet, schreiben die Autoren. Der größte Teil der Impfreaktionen trat in den ersten 48 Stunden nach der Verabreichung der Vakzine auf.
Robert H Shaw et al., „Heterologous prime-boost COVID-19 vaccination: initial reactogenicity data“, The Lancet, online first, May 12, 2021, DOI:https://doi.org/10.1016/S0140-6736(21)01115-6 a
STIKO: Auffrischimpfung für COVID-19 spätestens 2022 notwendig
Der Ständigen Impfkommission (STIKO) zufolge müssen sich die Deutschen spätestens im nächsten Jahr erneut gegen COVID-19 impfen lassen. „Das Virus wird uns nicht wieder verlassen. Die aktuellen Corona-Impfungen werden deswegen nicht die letzten sein”, prognostiziert Thomas Mertens, Vorsitzender der STIKO. „Grundsätzlich müssen wir uns darauf einstellen, dass möglicherweise im nächsten Jahr alle ihren Impfschutz auffrischen müssen."
Noch sei anhand der aktuellen Datenlage unklar, wann genau eine Auffrischung des Impfschutzes nötig sei. „Wir müssen sicherlich noch einige Monate warten, um zu sehen, ob möglicherweise bei einzelnen Gruppen der Impfschutz bereits wieder nachlässt oder generell zu schwach war", betont Mertens.
14. Mai 2021
------------------------------------------
Warum bei Genesenen der Test weiterhin positiv ausfällt
Forschende vermuten, dass sich einzelne Virusgene in die menschliche DNA eingefügt haben können und es deshalb nach einer überstandenen Infektion weiter zu einem positiven Testergebnis kommt.
Es gibt Fälle von ehemals mit SARS-CoV-2 infizierten Personen, deren PCR-Tests lange nach der Genesung weiter positiv ausfallen. Eine Erklärung dafür könnte sein, dass Virusgene ins menschliche Erbgut übergehen, wodurch das Virus bei PCR-Tests nachweisbar bleibt. Diese Personen fallen damit durchs Raster: Sie sind weder akut infiziert oder erkrankt, noch können sie als Genesene sicher ein negatives Ergebnis vorweisen. Den Vorgang haben Wissenschaftler in den USA im Experiment bestätigt.
Konkret sind einige Viren fähig, nach der Infektion des Menschen in dessen DNA überzugehen. Im Laufe der Zeit können sich so Fremdkörper im menschlichen Genom ansammeln. Dazu gehören auch die sogenannten LINE-1-Elemente (Long Interspersed Nuclear Elements), die als Transposone ihre Position im Genom verändern können (daher werden sie auch springende Gene genannt). Die meisten davon sind stumm, andere können allerdings aktiviert werden.
Wird bei der Aktivierung auch das Gen für die reverse Transkriptase produziert, können RNA-Viren, die gerade zufällig die Zellen infiziert haben, ins menschliche Erbgut eingebaut werden. Passiert dieser Vorgang zufällig an der Stelle, die registriert wird, so können auch nach einer überstandenen Infektion einzelne Virusgene gebildet werden. Diese sind dann für das positive PCR-Testergebnis verantwortlich.
Das vermuten auch Molekularbiologen vom Whitehead Institute in Cambridge, Massachusetts, und greifen das seltene, aber mögliche Phänomen für SARS-CoV-2 auf. Sie konnten Spuren des Virusgens in der DNA nachweisen - und zwar laut Studienbericht mit drei verschiedenen Techniken der DNA-Sequenzierung.
Als die Ergebnisse der Studie im Dezember veröffentlich wurden, kritisierten einige Wissenschaftler diese besorgt. Sie fürchteten, die Annahme, dass RNA-basierte Impfstoffe das menschliche Erbgut verändern könnten, werde damit untermauert. Inzwischen ist diese Kritik aber mit einem weiteren Experiment entkräftet worden: Die Gene bauen sich nach dem Zufallsprinzip nur zu 50 Prozent in die richtige Richtung ablesbar ein.
Zhang, L. et al., „Reverse-transcribed SARS-CoV-2 RNA can integrate into the genome of cultured human cells and can be expressed in patient-derived tissues.“ on Proceedings of the National Academy of Sciences on May 2021. DOI: 10.1073/pnas.2105968118.
COVID-19-Patienten weisen auch nach acht Monaten noch Antikörper auf
Zu diesem Ergebnis kommt eine aktuelle italienische Studie der Mailänder Forschungsklinik San Raffaele und des obersten italienischen Gesundheitsinstituts (ISS). Die Antikörper seien unabhängig von der Schwere der Erkrankung, vom Alter der Patienten oder von Vorerkrankungen im Blut nachweisbar.
Die Forscher untersuchten 162 Patienten mit symptomatischer SARS-CoV-2-Infektion, die während der ersten Infektionswelle in Italien im vergangenen Jahr in die Notaufnahme eingeliefert wurden. Denjenigen, die die Erkrankung überstanden haben, wurden im März und im April 2020 und erneut Ende November vergangenen Jahres Blutproben entnommen. Etwa 29 Patienten starben. Zwei Drittel der untersuchten Patienten waren Männer, das Durchschnittsalter lag bei 63 Jahren. Etwa 57 Prozent von ihnen hatten eine Vorerkrankung, Bluthochdruck und Diabetes waren am häufigsten vertreten.
"Das Vorhandensein von neutralisierenden Antikörpern nahm zwar im Laufe der Zeit ab, war aber sehr hartnäckig - acht Monate nach der Diagnose gab es nur drei Patienten, die nicht mehr positiv auf den Test reagierten", berichtet das ISS in einer gemeinsamen Erklärung mit der Mailänder Forschungsklinik. Diejenigen, die es nicht geschafft haben, Antikörper innerhalb der ersten 15 Tage nach der Infektion zu produzieren, haben ein größeres Risiko, schwere Formen von COVID-19 zu entwickeln und sollten frühzeitig identifiziert und behandelt werden, resümieren die Forscher.
Stefania Dispinseri et. al. „Neutralizing antibody responses to SARS-CoV-2 in symptomatic COVID-19 is persistent and critical for survival“ Nature Communications. Published on May, 11 2021. Doi: https://www.nature.com/articles/s41467-021-22958-8
12. Mai 2021
------------------------------------------
Teilpopulation hat geringes Risiko für Herzschäden nach mildem COVID
Studien aus Großbritannien untersuchten, ob Mitarbeiter des Nationalen Gesundheitsdienstes 6 Monate nach milden COVID-Verläufen signifikante Unterschiede in der Herzstruktur zeigen. Mit überraschendem Ergebnis.
Seit Pandemiebeginn gibt es Hinweise auf eine Multiorganbeteiligung bei COVID. Zu den beobachteten Auswirkungen auf das Herz gehören akutes koronares Syndrom, Verschlimmerung bereits bestehender Herz-Kreislauf-Erkrankungen, Arrhythmie, Myokarditis und mikroangiopathische Thrombose. Jüngste CMR-Studien haben sogar über Herzanomalien nach COVID-19 bei bis zu 78 Prozent der Patienten berichtet, mit Hinweisen auf eine anhaltende Myokardentzündung bei 60 Prozent auch nach einer leichten, nicht hospitalisierungspflichtigen Erkrankung.
Zwei britische Studien kommen zu anderen Ergebnisse. Aus 731 Mitarbeitern dreier Londoner Krankenhäuser, die 16 Wochen lang einer wöchentlichen Polymerase-Kettenreaktion (PCR) und Serologietests unterzogen wurden, rekrutierten sie dazu 149 Probanden: 74 seropositive und 75 seronegative.
Die Stichprobe
Die Komorbiditäten der Stichprobe waren relativ gering (18 Prozent Raucher, 13 Prozent Body-Mass-Index >30 kg/m2, 11 Prozent Asthma, 7 Prozent Bluthochdruck, 2 Prozent Diabetes, 1 Prozent rheumatologische Erkrankung, 1 Prozent Krebs). Das Medianalter betrug 37 Jahre [Bereich 18 bis 63 Jahre], insgesamt waren 42 Prozent Männer, 38 Prozent nicht weiß, darunter 6 Prozent der schwarzen Ethnien. Die Krankheit war bei 99 Prozent mild, bei 25 Prozent mit asymptomatischen Verläufen, nur zwei Probanden mussten jeweils für zwei Tage im Krankenhaus behandelt werden. Alle Infektionen traten vor dem 1. Mai 2020 auf.
Ergebnis: Kardiovaskuläre Phänotypisierungen zeigten 6 Monate nach Infektionsbeginn zwar Anomalien, jedoch bei Seropositiven nicht häufiger als bei Seronegativen. Der milde COVID-19-Verlauf hatte also keine messbaren kardiovaskulären Auswirkungen auf Struktur, Funktion und Narbenbelastung des Herzens sowie Aortensteifigkeit oder Serum-Biomarker, führen die Autoren aus. Ein Screening bei asymptomatischen Patienten nach nicht hospitalisiertem COVID-19 – wie es zwischenzeitlich diskutiert wurden – halten sie deshalb für nicht indiziert.
Auch bei der kardiovaskulären Magnetresonanztomografie (CMR) der Probanden gab es keine klinisch bedeutsamen Unterschiede in den Befunden zwischen Seropositiven und Seronegativen. Insgesamt waren beobachtete Anomalien sehr selten und gleichmäßig in beiden Probandengruppen verteilt, schreiben die Autoren.
Auch wenn die Ergebnisse für Beschäftigte des Gesundheitswesens Entwarnung geben, weisen die Autoren darauf hin, dass die Studienpopulation nicht repräsentativ für die Allgemeinbevölkerung ist.
Berry C, Mangion K, Cardiovascular complications are very uncommon in healthcare workers with mild or asymptomatic COVID-19 infection, JACC: Cardiovascular Imaging (2021), doi: https://doi.org/10.1016/j.jcmg.2021.04.022.
George Joy et al. "Prospective Case-Control Study of Cardiovascular Abnormalities 6 Months Following Mild COVID-19 in Healthcare Workers, JACC: Cardiovascular Imaging", 2021, ISSN 1936-878X, https://doi.org/10.1016/j.jcmg.2021.04.011.
10. Mai 2021
------------------------------------------
Warum schützt die Grippe-Impfung vor COVID?
Wer gegen Grippe geimpft ist, ist weniger anfällig für COVID und hat, wenn doch, einen viel milderen Verlauf. Das belegen Studien schon länger. Woran das liegt, ist aber nach wie vor nicht geklärt.
Kann eine Grippeschutzimpfung vor COVID-19 schützen? Eine Studie aus Michigan bündelt die Ergebnisse zweier Analysen: Die eine umfasst die Krankendaten von mehr als 92.000 Probanden aus Brasilien. Sie belegt: Bei Personen, die gegen das saisonale Influenza-Virus geimpft waren, sank das Risiko an COVID zu erkranken erheblich, die Todesrate fiel um 17 Prozent. Die Patienten benötigten in 8 Prozent der Fälle weniger Intensivpflege und in 18 Prozent weniger invasive Beatmung als nicht gegen Grippe geimpfte Patienten. Diese Ergebnisse stützen andere epidemiologische Studien.
Die zweite Analyse mit 27.000 Patienten brachte hervor, dass sich die Grippe-Geimpften knapp um 24 Prozent weniger häufig mit SARS-CoV-2 infizierten. Die positiv getesteten Geimpften wurden dabei seltener in die Klinik eingewiesen (32 zu 46 Prozent) und mussten nur halb so häufig beatmet werden (10 Prozent zu 20 Prozent). Ihr stationärer Aufenthalt war kürzer (12 zu 16 Tage) und sie mussten seltener intensiv gepflegt werden (19 zu 25 Prozent).
Kreuzreaktion oder Healthy User-Effekt?
Noch wird derzeit allerdings diskutiert, womit das reduzierte Risiko für einen schweren COVID-Verlauf durch eine Grippeschutzimpfung konkret zusammenhängt. Es gibt die Annahme, dass eine unspezifische Kreuzreaktion dafür verantwortlich sein kann. Danach würden bei der Impfung biologische Mechanismen angeregt, die nicht nur die eigentlichen Krankheitserreger bekämpfen, sondern auch andere.
„Der Schutzeffekt lässt sich durchaus mit Eigenschaften, Verhalten und Lebensumständen jener Menschen erklären, die sich um Prävention bemühen. Zum Beispiel wäre möglich, dass sie sozioökonomisch begünstigt sind“, widerspricht Prof. Dr. Thomas Mertens, Vorsitzender der STIKO und Sprecher der Arbeitsgruppe Influenza am Robert Koch-Institut (RKI).
Diese Personengruppe habe besseren Zugang zur Gesundheitsversorgung und lebe in großzügigeren Wohnungen, könne häufiger im Homeoffice arbeiten. Wer sich gegen die Grippe impfen lässt, achte also mehr auf seine Gesundheit und die Hygienevorschriften und in der Folge zeige sich die Gesundheit als widerstandsfähiger („Healthy User-Effekt“).
Die Daten der Analyse wurden retrospektiv ausgewertet. Somit ist nicht klar, ob die Gruppen der Geimpften und Nicht-Geimpften vergleichbar sind. Nichtsdestotrotz bietet die Studie nennenswerte Anhaltspunket, die für den positiven Effekt sprechen. Als Durchbruch wird sie von der STIKO jedoch nicht bewertet. Es sei nicht eindeutig klar, ob der Schutz auf die Grippeschutzimpfung selbst oder auf dden "Healthy User-Effekt" (siehe Kasten) zurückzuführen sind. Weitere prospektive Studien müssten das untersuchen - dann könne auch die Empfehlung zur Grippeschutzimpfung, wie sie die STIKO ausspricht, auch weiter unterfüttert werden.
Conlon, A. et al.: „Impact of the influenza vaccine on COVID-19 infection rates and severity“ published in American Journal of Infection Control on Feb, 21, 2021. DOI:https://doi.org/10.1016/j.ajic.2021.02.012
7. Mai 2021
------------------------------------------
BioNTech-Impfstoff auch gegen Virusvariante B.1.351 wirksam
Forscher aus Katar liefern erste Beweise dafür, dass der Impfstoff von BioNTech/Pfizer auch vor Virusvarianten wie B.1.1.7 und B.1.351 schützt.
Am 21. Dezember 2020 startete Katar seine Impfkampagne mit dem Vakzin von BioNTech/Pfizer. Bis zum 31. März 2021 haben insgesamt 385.853 Personen mindestens eine Impfstoffdosis und 265.410 beide Dosen erhalten.
Ab Mitte Januar 2021 wurde die Verbreitung der Virus-Variante B.1.1.7 beobachtet, ab Mitte Februar 2021 die der Variante B.1.351. Eine vom 23. Februar bis zum 18. März durchgeführte Genomsequenzierung ergab, dass 50,0 Prozent der COVID-Fälle in Katar durch B.1.351 und 44,5 Prozent durch B.1.1.7 verursacht wurden. Fast alle Fälle, in denen das Virus nach dem 7. März sequenziert wurde, wurden entweder durch B.1.351 oder B.1.1.7 verursacht.
Für die Arbeit wurden Daten über Impfungen, Polymerase-Kettenreaktionstests und klinische Merkmale aus den nationalen COVID-Datenbanken ausgewertet, die alle SARS-CoV-2-bezogenen Daten seit Beginn der Epidemie erfassen. Die Wirksamkeit des Impfstoffs wurde anschließend mit einem testnegativen Fall-Kontroll-Studiendesign geschätzt, einem bevorzugten Entwurf zur Bewertung der Wirksamkeit von Impfstoffen gegen Influenza.
Die geschätzte Wirksamkeit des Impfstoffs (14 oder mehr Tage nach der zweiten Dosis) gegen jede dokumentierte Infektion betrug
mit der Variante B.1.1.7 89,5 Prozent (95 Prozent Konfidenzintervall, Schwankungsbreite 85,9 bis 92,3 Prozent).
mit der Variante B.1.351 75,0 Prozent (95 Prozent Konfidenzintervall, Schwankungsbreite 70,5 bis 78,9 Prozent).
Die Wirksamkeit des Impfstoffs gegen schwere, kritische oder tödliche Krankheitsverläufe aufgrund einer Infektion mit SARS-CoV-2 (wobei die Varianten B.1.1.7 und B.1.351 in Katar vorherrschen) betrug 97,4 Prozent (95 Prozent Konfidenzintervall, Schwankungsbreite 92,2 bis 99,5 Prozent).
Sensitivitätsanalysen bestätigten diese Ergebnisse. Die Wirksamkeit des Impfstoffs wurde auch mithilfe einer Kohortenstudie bewertet, indem die Inzidenz von Infektionen bei geimpften Personen mit der Inzidenz von Antikörper-negativen Personen in der nationalen Kohorte verglichen wurde. Die Wirksamkeit wurde auf 87,0 Prozent (95 Prozent Konfidenzintervall, Schwankungsbreite 81,8 bis 90,7 Prozent) gegenüber der Variante B.1.1.7 und auf 72,1% (95 Prozent Konfidenzintervall, Schwankungsbreite 66,4 bis 76,8 Prozent) gegenüber der Variante B.1.351 geschätzt - Ergebnisse, die die oben genannten Ergebnisse bestätigen, schreiben die Autoren.
Bis zum Ende des Beobachtungszeitraums wurden bei 6.689 Personen, die eine Dosis des Impfstoffs erhalten hatten, und bei 1.616 Personen, die zwei Dosen erhalten hatten, Infektionen festgestellt. Sieben COVID-bedingte Todesfälle wurden bei geimpften Personen registriert: fünf nach der ersten Dosis und zwei nach der zweiten Dosis.
Laith J Abu-Raddad et al. „Effectiveness of the BNT162b2 Covid-19 Vaccine against the B.1.1.7 and B.1.351 Variants.“, N Engl J Med. 2021 May 5. doi: 10.1056/NEJMc2104974. Epub ahead of print. PMID: 33951357.
6. Mai 2021
------------------------------------------
So gut schützt der BioNTech-Impfstoff
Eine Beobachtungsstudie aus Israel zeigt: Mit BNT162b2 vollständig Geimpfte sind zu mehr als 95 Prozent vor einer Infektion und einem schwerem Verlauf geschützt. Das gilt auch für die Virusvariante B.1.1.7.
Im Analysezeitraum vom 24. Januar bis 3. April 2021 gab es in Israel 232.268 SARS-CoV-2-Infektionen, 7.694 COVID-19-Krankenhausaufenthalte, 4.481 schwere oder kritische COVID-19-Krankenhausaufenthalte und 1.113 COVID-19-Todesfälle bei Menschen ab 16 Jahren. Bis zum 3. April waren in Israel 4,7 Millionen (72,1 Prozent) der rund 6,5 Millionen Einwohner im Alter ab 16 Jahren mit zwei Dosen BNT162b2 vollständig geimpft.
Die in der Studie beobachtete Wirksamkeit des Impfstoffs 7 Tage oder länger nach der zweiten Dosis lag bei 95 Prozent. Die Inzidenzrate für Ungeimpfte lag bei 91,5 pro 100.000 Personentage verglichen mit 3,1 pro 100.000 Personentage bei vollständig geimpften Personen.
Laut Studie schützt die Impfung zu
97 Prozent gegen symptomatische COVID-Verläufe,
91,5 Prozent gegen asymptomatische Verläufe,
97,2 Prozent gegen COVID-19-bezogene Krankenhausaufenthalte,
97,5 Prozent gegen schwere oder kritische COVID-19-Verläufe und
96,7 Prozent gegen den COVID-19-bedingten Tod.
Fazit der Autoren: Nach der Zweitimpfung ist der COVID-Impfstoff von BioNTech/Pfizer in allen Altersgruppen (≥16 Jahre bis ≥ 85 Jahre) hochwirksam bei der Prävention symptomatischer und asymptomatischer SARS-CoV-2-Infektionen und COVID-19-bedingter Krankenhausaufenthalte, schwerer Krankheitsverläufe und Todesfälle. Das gilt auch für die Virusvariante B.1.1.7.
Eric J. Haas et al. „Impact and effectiveness of mRNA BNT162b2 vaccine against SARS-CoV-2 infections and COVID-19 cases, hospitalisations, and deaths following a nationwide vaccination campaign in Israel: an observational study using national surveillance data”, The Lancet, Published:May 05, 2021, DOI:https://doi.org/10.1016/S0140-6736(21)00947-8
5. Mai 2021
------------------------------------------
Schutzmaßnahmen in Pflegeheimen bleiben trotz Impfung zwingend
Eine Studie zeigt für einen COVID-19-Ausbruch in einem US-Pflegeheim, dass der mRNA-Impfstoff von BioNTech/Pfizer zu 87 Prozent vor symptomatischen Verläufen schützt. Insgesamt kam es zu vier Reinfektionen.
Bislang liegen nur begrenzte Daten zur Wirksamkeit der gängigen Impfstoffe in Pflegeeinrichtungen sowie gegenüber neuen Virusvarianten vor. Das Kentucky Department for Public Health (KDPH) und ein lokales Gesundheitsministerium untersuchten darum einen COVID-19-Ausbruch in einem US-Pflegeheim, der auftrat, nachdem allen Bewohnern und dem Gesundheitspersonal eine Impfung angeboten worden war.
Von den 83 Einwohnern erhielten bis zum Ausbruch 75 (90,4 Prozent), von 116 Mitarbeitern 61 (52,6 Prozent) zwei Dosen des mRNA-Impfstoffs von BioNTech/Pfizer. 26 Bewohner und 20 Mitarbeiter erhielten positive Testergebnisse für SARS-CoV-2, darunter auch 18 Bewohner und 4 Mitarbeiter, die ihre zweite Impfstoffdosis mehr als 14 Tage vor dem Ausbruch bekommen hatten.
Die Genomsequenzierung wies eine R.1-Virusvariante mit mehreren Mutationen des Spike-Proteins nach. Trotzdem war es für die geimpften Bewohner und Mitarbeiter 87 Prozent weniger wahrscheinlich als für Ungeimpfte, einen symptomatischen COVID-Verlauf zu erleiden. Während sich 75 Prozent der ungeimpften Bewohner infizierten, waren es bei den geimpften Bewohnern nur 25,4 Prozent – bei den Mitarbeitern infizierten sich 29,6 Prozent der ungeimpften und nur 7,1 Prozent der Geimpften.
Der geschätzte Schutz gegen eine SARS-CoV-2-Infektion betrug
unter den geimpften Bewohnern 66,2 Prozent (95 Prozent Konfidenzintervall, Spreizung 40,5 bis 80,8 Prozent)
und unter geimpften Mitarbeitern 75,9 Prozent (95 Prozent Konfidenzintervall, Spreizung 32,5 bis 91,4 Prozent).
Der geschätzte Schutz gegen einen symptomatischen COVID-Verlauf betrug
unter den geimpften Bewohnern 86,5 Prozent (95 Prozent Konfidenzintervall, Spreizung 65,6 bis 94,7 Prozent)
und unter geimpften Mitarbeitern 87,1 Prozent (95 Prozent Konfidenzintervall, Spreizung 46,4 bis 96,9 Prozent)
Es wurden vier Reinfektionen bei einem Bewohner und drei Mitarbeitern festgestellt, wobei einer der Mitarbeiter geimpft war. Alle vier Personen erlitten eine symptomatische Erkrankung. Ein Bewohner war 300 Tage zuvor infiziert gewesen, musste ins Krankenhaus eingeliefert werden und verstarb dort.
Die Autoren betonen, dass die Impfung zwar mit einer verminderten Infektionswahrscheinlichkeit und einem geringeren Risiko für einen symptomatischen Verlauf verbunden war, es aber bei 25,4 Prozent der geimpften Bewohner und 7,1 Prozent der geimpften Mitarbeiter zu Infektionen kam. Deshalb müsste von einer verringerten Wirksamkeit gegenüber der der R1-Virusvariante ausgegangen werden. Auch schütze eine natürliche Immunität offensichtlich nicht vor einer Reinfektion.
Fazit der Autoren: Die Impfung von Pflegeheimbewohnern und -mitarbeitern ist entscheidend, um das Risiko für die Übertragung von SARS-CoV-2 und schwere COVID-Verläufe in Einrichtungen zu verringern. Trotz Impfung bleibt ein kontinuierlicher Fokus auf Infektionspräventions- und -kontrollpraktiken ebenfalls von wesentlicher Bedeutung.
Alyson M. Cavanaugh et al. „COVID-19 Outbreak Associated with a SARS-CoV-2 R.1 Lineage Variant in a Skilled Nursing Facility After Vaccination Program - Kentucky”, March 2021. MMWR Morb Mortal Wkly Rep. 2021 Apr 30;70(17):639-643. doi: 10.15585/mmwr.mm7017e2
3. Mai 2021
------------------------------------------
An Tag eins kommt die große Müdigkeit
Müdigkeit, Husten, Kopfschmerzen: Eine neue Studie hat die tägliche Prävalenz der Symptome von 313 ambulanten COVID-Patienten für die ersten 20 Krankheitstage retrospektiv bewertet – und gibt eine dringende Empfehlung.
Bereits im März 2020 startete das Universitätsklinikum Münster einen Aufruf, um Personen zu identifizieren, die sich von einer SARS-CoV-2-Infektion erholt und während der Erkrankung ein Symptomtagebuch geführt hatten. 736 Teilnehmende erhielten daraufhin einen detaillierten Online-Bogen, der die Prävalenz, Schwere, Dauer und den Zeitpunkt von COVID-19-Symptomen abfragte. 313 Teilnehmer füllten den Online-Fragebogen vollständig aus.
Ergebnisse der Statistischen Auswertung: Müdigkeit (91,1 Prozent), Husten (85,0 Prozent) und Kopfschmerzen (78,0 Prozent) waren die häufigsten Symptome und traten innerhalb eines Medians von einem Tag nach Symptombeginn auf. Weitere häufige allgemeine Symptome waren Myalgie (73,2 Prozent), Rhinitis (70,3 Prozent) und Halsschmerzen (65,2 Prozent), die innerhalb eines Medians von einem Tag auftraten. Fieber wurde von 61 Prozent der Studienteilnehmer innerhalb eines Medians von zwei Tagen nach Symptombeginn berichtet.
Neurologische Symptome stellen sich meist erst an Tag drei ein
Symptome der unteren Atemwege (Dyspnoe) wurden von 51,1 Prozent aller Teilnehmer berichtet und traten innerhalb eines Medians von drei Tagen nach Symptombeginn auf. Das erste Auftreten neurologischer Symptome wie Geschmacksverlust (66,5 Prozent), Dysgeusie (51,8 Prozent) und Geruchsverlust (62,3 Prozent) wurde innerhalb eines Medians von drei bis vier Tagen nach Symptombeginn berichtet, auch deutlich später als die meisten anderen Symptome. Magen-Darm-Symptome wie Übelkeit (31,9 Prozent), Erbrechen (3,2 Prozent) und Durchfall (32,6 Prozent) traten ebenfalls deutlich später auf, innerhalb eines Medians von drei bis fünf Tagen.
Außerdem wurde die Symptomintensität in Schweregraden 0 bis 4 abgefragt. Müdigkeit (57,2 Prozent), Kopfschmerzen (54,0 Prozent), Geschmacksverlust (45,3 Prozent), Geruchsverlust (41,9 Prozent) und Myalgie (41,9 Prozent) wurden am häufigsten mit den Schweregraden 3 und 4 gemeldet.
Fazit: Um Infizierte früh im Krankheitsverlauf zu identifizieren, ist genaue Kenntnis der Symptomprävalenz sehr wichtig, schreiben die Autoren und sehen in ihren Ergebnissen wichtige Hinweise, die die Frühdiagnose von COVID-19 wesentlich verbessern könnten.
Besonders in Zeiträumen saisonaler Erkältungskrankheiten sei bei der Früherkennung von Patienten, die mit SARS-CoV-2 infiziert sind, äußerste Vorsicht und damit auch verstärkte Testungen geboten, da die Symptome einer milden COVID-Erkrankung stark denen von gewöhnlichen Atemwegsinfekten ähneln.
Patricia Nicole Wiegele et al., „Symptom Diary–Based Analysis of Disease Course among Patients with Mild Coronavirus Disease, Germany, 2020”, Emerg Infect Dis. 2021;27(5):1353-1361. https://doi.org/10.3201/eid2705.204507
29. April 2021
------------------------------------------
Schon eine Impfung kann das Risiko, Personen im eigenen Haushalt anzustecken, halbieren. Das geht aus einer umfangreichen Datenauswertung der Gesundheitsbehörde Public Health England hervor. Eine Impfung gegen COVID-10 verhindert mit sehr hoher Wahrscheinlichkeit einen schweren oder tödlichen Krankheitsverlauf. Noch immer ist aber nicht ganz klar, ob geimpfte Personen sich weiterhin mit dem Virus infizieren und so möglicherweise durch einen nur noch milden und asymptomatischen Verlauf die Infektion unbemerkt weitertragen können. Dabei ist diese Frage zentral für die weitere Pandemie-Entwicklung.
Britische Wissenschaftler analysierten nun Daten der Gesundheitsbehörde aus 365.447 Haushalten und stellten einen Vergleich auf: Wie häufig kam es zu gesicherten Infektionen in den Familien und Haushalten von nicht geimpften Personen in Relation zu denen, die in Haushalten von bereits einmal geimpften Personen stattfanden. Im Ergebnis zeigte sich, das bereits die erste Impfung das Risiko einer Ansteckung in den privaten Haushalten um bis zu 50 Prozent reduzierte.Von 960.765 Haushaltsmitgliedern der nicht-geimpften Indexfälle erkrankten 10,1 Prozent, also 96.898 Personen an COVID-19. In Haushalten hingegen, in denen der Indexpatient bereits die erste Dosis des Impfstoffs Vaxzevria von AstraZeneca erhalten hatte, erkrankten mit 196 von 3.424 Mitbewohnern nur 5,72 Prozent. In den Haushalten mit einem Indexfall nach der ersten Dosis Tozinameran von BioNTech/Pfizer kam es unter 5.939 Mitgliedern zu 371 Erkrankungen und somit zu 6,25 Prozent der Ansteckungen.Somit hat die erste Impfung das Übertragungsrisiko in den Haushalten um 38 bis 49 Prozent gesenkt und somit nahezu halbiert.Harris, Ross J. et al: „Impact of vaccination on household transmission of SARS-COV-2 in England“ published in khub.net on Arpil 28, 2021. Server-PDF.
28. April 2021
------------------------------------------
Nasenspray mit Carragelose senkt Infektionsrisiko um 80 Prozent
Nasensprays mit dem Wirkstoff Carragelose aus der Rotalge weisen eine effektive Schutzwirkung gegen SARS-CoV-2 auf – sowohl bei in vitro-Tests als auch bei Probanden.
Der natürliche Wirkstoff Carragelose aus der Rotalgenträgt zur Bildung eines Schutzfilms als physikalische Barriere der Nasenschleimhaut bei und verhindert so, dass die Viren ihre Erbinformationen in die Zellen einschleusen und sich dort replizieren. Der Mechanismus war zuvor auch schon bei anderen Erkältungsviren erfolgreich. Untersuchungen an verschiedenen humanen Zellsystemen im Labor am Universitätsklinikum Erlangen belegen die antivirale Wirkung des Carragelose-Sprays. Klinische Studien bestätigten zuvor die gute Verträglichkeit hinsichtlich anderer Erkältungsviren. Ergänzt werden die Erkenntnisse nun durch Studiendaten aus Argentinien. Dort wurden 400 Krankenhausmitarbeiter, die regelmäßigen direkten Kontakt zu infizierten Patienten hatten, in zwei Gruppen aufgeteilt. Die eine Gruppe wurde um die Anwendung des Nasensprays 4-mal pro Tag gebeten, die andere erhielt ein Placebo. Der Test dauerte drei Wochen. Der Einsatz des Sprays erwies sich als effektiv und konnte das Infektionsrisiko bei der regelmäßigen Verwendung deutlich verringern. „Ein Carragelose-haltiges Nasenspray bewirkt eine 80-prozentige relative Risikoreduktion für eine Infektion mit SARS CoV-2“, ordnet Prof. Dr. Ulrich Schubert, Forscher am Virologischen Institut für Klinische und Molekulare Virologie des UK Erlangen die neuen Studienergebnisse ein. Das Spray könnte seiner Einschätzung nach als präventive Maßnahme eingesetzt werden. Seit Dezember 2020 empfiehlt die Deutsche Gesellschaft für Krankenhaushygiene bereits den Mitarbeitern auf COVID-Stationen die Anwendung von Carragelose-Nasensprays. „Aber auch die Allgemeinbevölkerung kann damit ihre persönlichen Schutzmaßnahmen zur Vorbeugung erweitern“, betont Schubert.Das gelte auch für Virusmutanten: „Carragelose ist ein Polymer, das das Virus durch eine elektrostatische Wechselwirkung umhüllt und es dabei neutralisiert. Deshalb sollte es für die Wirksamkeit auch keinen Unterschied machen, welche Virusvariante vorliegt“, so der Virologe.Wirksamkeit und Verträglichkeit von Carragelose-Nasenspray, -Inhalationslösung und -Lutschpastillen in Bezug auf die Vorbeugung und Therapie von SARS-CoV-2-Infektionen werden derzeit in drei weiteren klinischen Studien in Erlangen untersucht.Figueroa, Juan M. et al: „Efficacy of a nasal spray containing Iota-Carrageenan in the prophylaxis of COVID-19 in hospital personnel dedicated to patients care with COVID-19 disease A pragmatic multicenter, randomized, double-blind, placebo-controlled trial (CARR-COV-02)“ published in medRxiv on April 15, 2021. doi: https://doi.org/10.1101/2021.04.13.21255409
26. April 2021
------------------------------------------
Bisher gab es noch wenige Erkenntnisse über die Folgen einer Infektion mit SARS-CoV-2 für schwangere Frauen und deren ungeborene Kinder. Eine internationale Studie legt nun Ergebnisse vor.
Die Vermutung, Schwangere würden vor einer Infektion eher verschont, weil sie zur jüngeren Bevölkerungsgruppe gehören, konnte bereits eine US-Studie aus dem vergangenen Jahr nicht bestätigen. Ähnlich wie bei der saisonalen Influenza, der Spanischen Grippe und der Schweinegrippe waren Morbidität und Mortalität bei Schwangeren erhöht.
Während der Coronavirus-Pandemie mussten diese Patientinnen drei Mal häufiger auf der Intensivstation behandelt und beatmet werden, teilten die US-Centers for Disease Control and Prevention (CDC) im vergangenen Jahr mit.
Nun legen Forscher der Universität Oxford Ergebnisse vor, die im Rahmen der INTERCOVID-Studie mit 43 teilnehmenden Gesundheitszentren aus 18 Ländern erlangt wurden. Die Studie untersucht die Entwicklung von Kindern während der Schwangerschaft und den ersten zwei Lebensjahren. Dabei wurden rund 700 an COVID-19 erkrankte schwangere Frauen zwei möglichst vergleichbaren Schwangeren gegenübergestellt, die nicht infiziert waren.
Dabei stellte sich heraus, dass 40 Prozent der erkrankten Schwangeren ohne Symptome dennoch eine erhöhte Morbidität und Mortalität aufwiesen. Sie erkrankten zu 76 Prozent häufiger an einer Präeklampsie oder Eklampsie – dem sogenannten Schwangerschaftskrampf (relatives Risiko hier: RR 1,76; 95-Konfidenzintervall 1,27 bis 2,43). Insgesamt kam es 3-mal häufiger zu einer schweren Infektion (RR hier: 3,38; 1,63 bis 7,01). Zudem mussten die Patientinnen 5-mal häufiger auf Intensivstation versorgt (RR hier: 5,04; 3,13 bis 8,10).
Elf Schwangere aus der Untersuchungsgruppe der Infizierten starben. Die relative Müttersterblichkeit von 1,6 war somit deutlich höher, trat jedoch zum Großteil in ärmeren Ländern auf, wo die Möglichkeiten einer intensivmedizinischen Behandlung schlechter waren.
Weiter zeigte die internationale Vergleichsstudie, dass die Infektion der Schwangeren auch Auswirkungen auf die Gesundheit des ungeborenen Kindes hatte. Die Quote der Frühgeburten (RR hier 1,59; 1,30 bis 1,94) und der künstlich eingeleiteten Frühgeburten (RR hier 1,97; 1,56 bis 2,51) war höher als bei den gesunden Müttern. Und auch der „severe neonatal morbidity index“ (SNMI), der die häufigsten neonatalen Komplikationen umfasst, war erhöht (RR hier 2,66; 1,69-4,18). Das gilt auch für den Morbiditäts- und Mortalitätsindex (RR hier 2,14; 1,66 bis 2,75).
Hatten die Mütter Symptome wie Fieber und Atemnot, begünstigten diese ihr Komplikationsrisiko und auch das der Kinder. Mit 13 Prozent steckten sich 54 Neugeborene perinatal mit dem Virus an. Beim Stillen wurden hingegen keine Übertragungen festgestellt.
Warum die Morbidität und Mortalität während der Schwangerschaft erhöht ist, ist bislang nicht geklärt. Die Forscher vermuten, dass diese Risiken mit der physiologischen Veränderung des Körpers wie der gestiegenen Herzfrequenz und dem höheren Sauerstoffgebrauch sowie der verminderten Lungenkapazität und dem höheren Thromboserisiko einhergehen könnten. Zum anderen könnte die natürliche Immunsuppression, die das Ungeborene eigentlich schützen soll, eine Infektion begünstigen.
Deutschland war nicht an der Studie beteiligt.Villar J. et al. „Maternal and Neonatal Morbidity and Mortality Among Pregnant Women With and Without COVID-19 Infection: The INTERCOVID Multinational Cohort Study.“ JAMA Pediatr. Published online April 22, 2021. doi:10.1001/jamapediatrics.2021.1050
23. April 2021
------------------------------------------
Nachdem frühe Studien Korrelationen zwischen schweren COVID-Verläufen und Asthma beobachteten, gibt eine chinesische Meta-Studie mehr als ein Jahr nach Pandemiebeginn jetzt Entwarnung.
Für die Meta-Studie werteten die Forschenden die Rohdaten aus insgesamt 18 Arbeiten aus. Diese berichteten über die epidemiologischen und klinischen Merkmale von COVID-19 und seine Prävalenz bei Asthmapatienten berichteten, wurden eingeschlossen. Im Ergebnis zeigten die ausgewerteten Daten, dass Asthma das Risiko eines schweren COVID-Verlaufs nicht statistisch signifikant erhöht (Odds Ratio [OR] 1,04 (Konfidenzintervall 95 Prozent, Schwankungsbreite 0,75 bis 1,46)).
Die Erkrankung sei also doch kein eindeutiger Risikofaktor für die Entwicklung von schwerem COVID-19, schlussfolgern die Autoren. In der Studie wurden PubMed-, Embase- und Web of Science-Datenbanken systematisch nach Studien durchsucht, die zwischen dem 1. Januar und dem 28. August 2020 veröffentlicht wurden.
Eine dänische Studie hingegen untersuchte den Effekt von anderen chronisch entzündlichen Erkrankungen, wie entzündliche Darmerkrankungen, Psoriasis-Arthritis, rheumatoide Arthritis und Spondylarthropathie.
Mithilfe der Daten von Patientenfällen aus dem Zeitraum des 1. März 2020 bis 31. Oktober 2020 wurden eine Kohorte von stationären Patienten mit COVID-19 und entzündlichen Darmerkrankungen (IBD), rheumatoider Arthritis (RA), Spondyloarthropathie (SpA) oder Psoriasis-Arthritis (PsA) (n= 132) sowie eine Kontrollkohorte ohne diese Krankheiten (n=2.811) gebildet. Die Forschenden verglichen anschließend die mediane Dauer des Krankenhausaufenthalts, die Beatmungsnotwendigkeit sowie die 14-Tage- und 30 Tage-Sterblichkeit.
Das Ergebnis hier: Es gab keine statistisch signifikanten Unterschiede zwischen den exponierten Patienten und der Kontrollgruppe – sowohl in Bezug auf die Dauer des Krankenhausaufenthalts (6,8 Tage vs. 5,5 Tage), dem Bedarf an mechanischer Beatmung (7,6 Prozent vs. 9,4 Prozent), als auch der Sterblichkeit. Diese lag in beiden Gruppen ähnlich hoch (Odds Ratio [OR] 0,71; Konfidenzintervall 95 Prozent, Schwankungsbreite 0,42-1,22).
Ting Wu et al., „Asthma does not influence the severity of COVID-19: a Meta-analysis“, Journal of Asthma, Published online: 16. April 2021, DOI: 10.1080/02770903.2021.1917603
Jens Kjeldsen et al., „Outcome of COVID-19 in hospitalized patients with chronic inflammatory diseases. A population based national register study in Denmark.“ J Autoimmun. 2021 Mar 26;120:102632. DOI: 10.1016/j.jaut.2021.102632.
21. April 2021
------------------------------------------
Junge Menschen sind anfällig für asymptomatische Reinfektionen
Eine frühere COVID-19-Infektion schützt jungen Menschen nicht vollständig vor einer Reinfektion. Dies ergab eine Beobachtungsstudie mit mehr als 3.000 gesunden US-amerikanischen Rekruten.
Reinfektionen sind trotz überstandener Erstinfektion möglich. Das zeigt eine Studie an US-amerikanischen Rekruten, die während ihrer Grundausbildung in einem zentralen Lager engen Kontakt hatten. Obwohl strenge Test- und Quarantänemaßnahmen durchgeführt wurden, kam es zu einem Ausbruchsgeschehen vor Ort. Dabei wurde jeder zweite Rekrut bei der regelmäßigen PCR-Kontrolle positiv auf SARS-CoV-2 getestet. Einige davon waren bereits zu einem früheren Zeitpunkt infiziert.
In Lancet Respiratory Medicine wurden nun die Ergebnisse dieser Kohorten-Studie veröffentlicht. Vor Beginn der Ausbildung vor Ort wurden alle Teilnehmer auf Antikörper getestet. Nur 1.079 der 2.247 Rekruten hatten zu diesem Zeitpunkt keine Antikörper im Blut. Die meisten vorherigen Infektionen mussten asymptomatisch verlaufen sein, vermuten die Studienleiter.
In der Studie wurden zwischen Mai und November 2020 etwa 10 Prozent (19 von 189) der Teilnehmer, die zuvor mit SARS-CoV-2 infiziert waren (seropositiv), erneut infiziert, verglichen mit Neuinfektionen bei 50 Prozent (1.079 von 2.247) der Teilnehmer, die zuvor nicht infiziert waren (seronegativ).
Die relative Inzidenzrate (IRR) betrug 0,18 Prozent, abgeleitet aus dem 95-prozentigen Konfidenzintervall von 0,11 bis 20,8. Somit hinterlässt eine frühere SARS-CoV-2-Infektion einen 82-prozentigen Schutz vor einer erneuten Ansteckung. Die Ergebnisse decken sich mit anderen Studien. Sie sind ein Beleg dafür, dass auch junge Personen keine sichere Immunität ausbilden. Zu einer erneuten Infektion kann es aufgrund einer nur schwach ausgebildeten Immunantwort beim ersten Viruskontakt gekommen sein.
Allerdings vielen die Reinfektionen kürzer aus und gingen mit weniger schweren Symptomen einher. Auch deswegen werden Reinfektionen bei jüngeren Menschen oftmals übersehen, schreiben die Autoren. Die festgestellte Viruslast war bei der Zweitinfektion 10-mal geringer als bei den Erstinfektionen.
Obwohl die Studie an jungen, fitten, meist männlichen Marinerekruten durchgeführt wurde, gehen die Autoren davon aus, dass das in ihrer Studie gefundene Risiko einer Reinfektion auf viele junge Menschen zutrifft.
Hansen, C. H. et al.: „Assessment of protection against reinfection with SARS-CoV-2 among 4 million PCR-tested individuals in Denmark in 2020: a population-level observational study“ published on March, 17, 2021 in Lancet Respiratory Medicine https://doi.org/10.1016/S0140-6736(21)00575-4
19. April 2021
------------------------------------------
SARS-CoV-2 befällt orale Zellen
SARS-CoV-2 infiziert auch die Zellen im Mundraum. Hier könnte es sich sogar replizieren und damit einen unterschätzten Ansteckungsort darstellen. Die Erkenntnisse unterstützen außerdem die alternative Testmethode mittels Speichel.
SARS-CoV-2 ist bereits im Speichel von infizierten Personen nachgewiesen worden - auch in hoher Konzentration. Unklar war bislang, woher die Viren stammen. Bislang wird angenommen, dass sie gegebenenfalls aus dem Nasensekret oder dem Sputum aus dem Rachen der Erkrankten in den Mundraum gelangen. Aber woher kommen die Viren im Speichel von Infizierten ohne Atemwegsbeschwerden?
Dass das Virus neben dem Rachenraum und der Nase auch die Zellen der Mundhöhle befällt und sich hier replizieren kann, fanden Forschende der US-amerikanischen Gesundheitsbehörde National Institutes of Health (NIH) und der University of North Carolina heraus. Sie vermuten, dass die Übertragung über den Mund möglich sein könnte.
ACE 2-Rezeptor für den Zelleintritt in Mundraum gesichert
In ihrer Studie verglichen sie das Gewebe im Mund von gesunden Personen mit dem von infizierten. Dabei entdeckten sie die beiden Proteine, die das Virus zum Eintritt in die Zellen benötigt. Sowohl der ACE2-Rezeptor als auch das TMPRSS2-Enzym wurden in der Mundschleimhaut, dem Zahnfleisch und der Speicheldrüse identifiziert. Dabei waren Zellen zum Teil mit beiden Proteinen ausgestattet, was auf eine erhöhte Anfälligkeit dieser Bereiche hinweist.
In der Hälfte der Gewebeproben aus der Speicheldrüse von verstorbenen COVID-Patienten stellten die Forschenden mittels orthogonale RNA- und Protein-Expressionsuntersuchungen die RNA des Erregers tatsächlich fest. Bei akut infizierten Personen gelang die Entdeckung von spezifische Sequenzen viraler RNA, die darauf hinweisen, dass in den Zellen neue Virenkopien produziert werden. Die Forschenden halten die Replikation von SARS-CoV-2 in den Zellen der Mundhöhle daher für möglich.
Bei einem weiteren Test infizierte der Speichel von asymptomatischen Patienten gesunde Zellen in einer Versuchsschale im Labor. Somit wäre eine Übertragung durch den Speichel auch bei asymptomatischen Infektionen möglich. Die Ergebnisse könnten den alternativen Speicheltest auf SARS-CoV-2 unterstützen.
Das Virus befällt zahlreiche Bereiche im Organismus, wie das Gewebe der Lunge, der Nieren, des Verdauungstrakts sowie die Gewebewand der Blutgefäße. Die verschiedenen Infektionsorte können auch eine Erklärung für die unterschiedlichen Manifestationen der zahlreichen Symptome sein. Zu den oralen Symptomen zählen neben dem Verlust des Geschmacksinns auch eine Mundtrockenheit und Schleimhautläsionen, wie die Bildung von Bläschen.
Die Autoren erheben keinen Anspruch auf Vollständigkeit im Ergebnis, geben aber zu bedenken, dass das Übertragungsrisiko der Mundhöhle bislang unterschätzt wird. Weitere Untersuchungen sollen die Erkenntnisse verifizieren.
Huang, N. et al. "SARS-CoV-2 infection of the oral cavity and saliva". Published on March 26, 2021 in Nature Medicine. https://doi.org/10.1038/s41591-021-01296-8
16. April 2021
------------------------------------------
Eine Studie aus Oxford hat untersucht, wie hoch das Risiko einer Sinusvenenthrombose nach einer COVID-Erkrankung, nach einer Impfung mit den Vakzinen von BioNTech oder Moderna oder nach einer Grippeinfektion ist im Vergleich zur Fallhäufigkeit in der Allgemeinbevölkerung.
Das Team aus Wissenschaftlern des Department of Psychiatry der Universität Oxford und der Oxford Health NHS Foundation untersuchte die Häufigkeit auftretender Sinusvenenthrombosen (CVT) zwei Wochen nach einer festgestellten COVID-19-Erkrankung oder einer Influenza beziehungsweise der ersten Impfung. Als Vergleichswert zogen sie den CVT-Wert der Allgemeinbevölkerung heran. Daraus wurde im Anschluss die CVT-Inzidenz abgeleitet.
Im Ergebnis lag die CVT-Inzidenz nach einer COVID-Diagnose bei 39 pro eine Million und war somit deutlich höher als nach einer Grippeerkrankung mit 0 pro eine Million oder nach der Impfung mit einem mRNA-Impfstoff mit 4,1 pro einer Million. Und auch im Vergleich zur sogenannten Hintergrundrate der Allgemeinbevölkerung, die während des zwei wöchigen Testzeitraums bei 0,41 lag, war die Inzidenz der Sinusvenenthrombose nach einer COVID-Erkrankung höher.
Risiko nach COVID-Infektion 100-mal höher
Im Vergleich mit den derzeit zugelassenen Impfstoffen wardas Sinusvenenthrombose-Risiko nach einer COVID-Infektion um das Acht- bis Zehnfache erhöht, bilanzieren die Forschenden. In Relation zur Hintergrundinzidenz in der Allgemeinbevölkerung sei das CVT-Risiko nach einer COVID-Erkrankung rund 100-mal höher und berge das höchste Risiko. Die Studie belege damit auch, dass die Sinusvenenthrombose in Zusammenhang mit COVID-19 steht.
Die Studienautoren verweisen auf die unterschiedlichen Datenquellen für die Analyse und darauf, dass die Datenströme noch nicht als vollständig erachtet werden könnten. Daher liefere die Arbeit erste Anhaltspunkte für eine weitere Diskussion um den Einsatz des Impfstoffs von AstraZeneca.
Taquet, M. et al: "6-month neurological and psychiatric outcomes in 236 379 survivors of COVID-19: a retrospective cohort study using electronic health records" published in The Lancet Psychiatry on April 6, 2021. DOI:https://doi.org/10.1016/S2215-0366(21)00084-5
15. April 2021
------------------------------------------
Rheinland-Studie: Antikörperschutz lässt schnell nach
Zwischen April und Juni 2020 wurden im Rahmen der Studie rund 5.300 erwachsene Bonner auf Antikörper gegen SARS-CoV-2 untersucht. Dafür wurden Blutproben entnommen und analysiert. Bei positivem Erstbefund in einem Immunoassay durchliefen diese Proben zusätzlich einen "Plaque-Reduktions-Neutralisationstest", um sicherzustellen, dass sich die nachgewiesenen Antikörper spezifisch gegen SARS-CoV-2 richteten - und nicht gegen andere Coronaviren, die beispielsweise normale Erkältungen auslösen können. Das Team der Rheinland Studie kooperierte für diese Analysen mit dem Institut für Virologie an der Charité - Universitätsmedizin Berlin.
Jeder Fünfte hat heute keine Antikörper mehr
Bei 22 Probanden konnten "neutralisierende" und somit besonders wirksame Antikörper, die das Eindringen von SARS-CoV-2 in Zellen unmittelbar verhindern, nachgewiesen werden - was auf einen früheren Kontakt mit dem Virus hindeutete. Die Mehrheit berichtete nur von einem milden oder gar asymptomatischen Krankheitsverlauf. Sie wurden im September 2020 - also ungefähr vier bis fünf Monate nach der ersten Blutprobe - erneut getestet. Fazit: Bei den meisten war der Antikörper-Spiegel gesunken; bei vier Personen konnten sogar keine Antikörper mehr nachgewiesen werden.
Schlussendlich hat jeder fünfte Teilnehmer, bei dem im Frühjahr letzten Jahres neutralisierende Antikörper gegen SARS-CoV-2 im Blut gefunden worden waren, mittlerweile den Schutz vor einer erneuten Infektion wieder verloren.
Die zelluläre Immunantwort kann weiterhin Bestand haben
Aus diesen Daten lässt sich allerdings nicht direkt ableiten, inwieweit die Abnahme der Antikörper die Immunantwort beeinflusst, betont Dr. Ahmad Aziz, DZNE-Wissenschaftler und Erstautor der aktuellen Veröffentlichung.
"Der Rückgang an Antikörpern scheint relativ schnell zu gehen. Das Immunsystem hat allerdings weitere Instrumente, um Krankheitserreger abzuwehren. Antikörper sind zweifelslos bedeutsam, aber nur Teil eines größeren Arsenals. Andere Studien deuten darauf hin, dass eine andere Komponente, die wir die zelluläre Immunantwort nennen, trotz fallender Antikörper-Spiegel weiterhin Bestand haben kann."
Tatsächlich weiß man noch wenig über die Dauer der Immunität gegenüber SARS-CoV-2 nach einer Infektion. Das könnte auch von der jeweiligen Virusvariante abhängen. Die Autoren der Rheinland-Studie wollen daher die Auswirkungen der Pandemie auf die geistige und körperliche Gesundheit der Bevölkerung erfassen, um die Folgen zu verstehen und Risikofaktoren zu identifizieren.
Die Rheinland-Studie
In der Studie untersucht das DZNE, wie sich die Gesundheit von Erwachsenen bis ins hohe Alter entwickelt. An der 2016 gestarteten Untersuchung beteiligen sich aktuell rund 6.000 Bonner; langfristig soll ihre Anzahl auf bis zu 20.000 anwachsen. Die Mitwirkenden werden alle drei bis vier Jahre zu einer umfassenden Bestandsaufnahme ihrer körperlichen und geistigen Fitness eingeladen.
Aziz, N. A. et al. "Seroprevalence and correlates of SARS-CoV-2 neutralizing antibodies from a population-based study in Bonn, Germany." published on April 9, 2021 in Nat Commun 12 https://doi.org/10.1038/s41467-021-22351-5
13. April 2021
------------------------------------------
Monoklonale Antikörper-Kombination schützt vor COVID-Infektion
In einer kürzlich durchgeführten Phase-III-Studie konnte eine Antikörperkombination effektiv vor einer Ansteckung in COVID-19-positiven Haushaltskontakten schützen. Außerdem wurde bei nachweislich positiven asymptomatischen Patienten das Fortschreiten zu symptomatischem COVID-19 signifikant reduziert.
Monoklonale Antikörper sind aus der Therapie verschiedener Krebs- und Autoimmunerkrankungen bekannt, werden aktuell aber auch für den Einsatz gegen COVID-19 erprobt.
In einer doppelblinden, placebokontrollierten Phase-III-Studie wurde die präventive Wirkung der monoklonalen Antikörperkombination REGEN-COV (Casirivimab und Imdevimab) bei nicht infizierten Personen ohne Anti-SARS-CoV-2-Antikörper untersucht. Die Probanden lebten dabei im selben Haushalt mit einer Person, die innerhalb der letzten vier Tage positiv auf SARS-CoV-2 getestet worden war.
An der Phase-III-Studie, die das Pharmaunternehmen Regeneron Pharmaceuticals gemeinsam mit dem National Institute of Allergy and Infectious Diseases (NIAID) durchführte, nahmen insgesamt 1.505 Probanden teil. Alle wurden zu Beginn mit einem RT-PCR-Test aus Nasopharyngealabstrichen auf SARS-CoV-2 getestet. Anschließend wurde ihnen randomisiert (1:1) entweder eine Dosis REGEN-COV (1.200 mg) oder ein Placebo als subkutane Injektion verabreicht.
Ansteckungen konnten um 81 Prozent reduziert werden
Die Ergebnisse zeigen, dass durch die Antikörperinjektion das Risiko einer Infektion um durchschnittlich 81 Prozent (p<0,0001) reduziert werden konnte. In der ersten Woche nach Injektion besteht ein 72-prozentiger Schutz, der sich ab der zweiten Woche sogar auf sogar 93 Prozent erhöht.
Die Ergebnisse sind hoch-signifikant. Von 753 Probanden, die REGEN-COV erhielten, infizierten sich insgesamt nur 11 Probanden. Dies entspricht lediglich 1,5 Prozent. In der Placebo-Gruppe infizierten sich von den insgesamt 752 Teilnehmern 59 (7,8 Prozent).
Mildere und kürzere Krankheitsverläufe
Bei den elf mit REGEN-COV behandelten Personen, die eine symptomatische Infektion erlitten, verschwanden die Symptome im Durchschnitt innerhalb von einer Woche, verglichen mit drei Wochen unter Placebo. Die Verläufe unter REGEN-COV waren zudem wesentlich milder als in der Placebo-Gruppe.
Insgesamt hatten 31 Prozent der Teilnehmer mindestens einen bekannten Faktor, der sie einem erhöhten Risiko aussetzte, einen schwereren Verlauf von COVID-19 zu erleiden - zum Beispiel Diabetes mellitus oder eine immunsuppressive Erkrankung. Das Medianalter der lag bei 44 Jahren, der jüngste Proband war 12 Jahre, der älteste 92 Jahre alt.
Therapeutische Wirkung der monoklonalen Antikörperkombination
In einer weiteren Studie wurde die therapeutische Wirkung der Antikörperkombination beleuchtet. An der Studie nahmen 204 Personen teil, die positiv auf SARS-CoV-2 getestet wurden, aber zu Studienbeginn symptomfrei waren und noch keine Antikörper aufwiesen. Sie wurden randomisiert und erhielten entweder eine subkutane Injektion mit REGEN-COV (1.200 mg) oder ein Placebo.
REGEN-COV verringerte das Gesamtrisiko einer Progression zu symptomatischem COVID-19 um 31 Prozent (primärer Endpunkt nach 29 Tagen) und um 76 Prozent nach dem dritten Tag.
Zusätzlich zur Verringerung des Risikos symptomatischer Infektionen wurde die Gesamtzahl der Wochen, in denen die Patienten Symptome hatten, in der REGEN-COV-Gruppe im Vergleich zur Placebo-Gruppe fast halbiert (45 Prozent), und die Viruslast wurde um mehr als 90 Prozent reduziert.
Obwohl nicht im ursprünglichen Analyseplan enthalten, fanden die Forscher auch heraus, dass sechs der Placebo-Patienten während der 29-tägigen Wirksamkeitsbeurteilung aufgrund von COVID-19 entweder ins Krankenhaus eingeliefert wurden oder die Notaufnahme aufsuchten. Aus der REGEN-COV Gruppe wurde kein Patient im Krankenhaus vorstellig.
COVID-19 Study Assessing the Efficacy and Safety of Anti-Spike SARS CoV-2 Monoclonal Antibodies for Prevention of SARS CoV-2 Infection Asymptomatic in Healthy Adults and Adolescents Who Are Household Contacts to an Individual With a Positive SARS-CoV-2 RT-PCR Assay
9. April 2021
------------------------------------------
Mehr als ein Drittel der an COVID-19 erkrankten US-Amerikaner leiden während des ersten halben Jahres nach der Infektion unter neurologischen oder psychiatrischen Erkrankungen und müssen behandelt werden.
Ein Team der Oxford Universität hat in The Lancet Psychiatry die Ergebnisse einer umfangreichen Datenauswertung vorgestellt. Aus elektronischen Krankenakten von 81 Millionen US-amerikanischen Patienten werteten sie 236.379 Fälle von erwachsenen COVID-Erkrankten aus, die die Infektion überlebt hatten. Dabei interessierte die Experten, wie oft die Genesenen in den ersten sechs Monaten nach der Erkrankung wegen neurologischer oder psychiatrischer Erkrankungen behandelt wurden. Das war bei 33,6 Prozent der Patienten der Fall.
Darunter trat mit 17,4 Prozent am häufigsten Angststörungen auf, gefolgt von Depressionen mit 13,7 Prozent. Wegen Substanzmissbrauch mussten 7,1 Prozent und aufgrund von Schlafstörungen 5,4 Prozent behandelt werden. Neurologisch tragen 2,1 Prozent aufgrund eines Schlaganfalls, 0,7 Prozent wegen Demenz und 0,6 Prozent wegen Hirnblutungen symptomatisch in Erscheinung.
Die Auswertung trennte die hospitalisierten Patienten von denen mit leichten und mittelschweren Verläufen. Insgesamt 38,7 Prozent der stationär betreuten Patienten litten unter Langzeitfolgen. Bei Patienten auf der Intensivstation waren es 46,4 Prozent. Und bei Patienten mit Enzephalopathie bei 62,3 Prozent.
Da diese Symptome auch ohne COVID-19 auftreten können, setzten die Wissenschaftler die Zahlen in Bezug zu Influenza. Hier zeigte sich, dass das Risiko für neurologische oder psychiatrische Erkrankungen um 44 Prozent höher liegt. Abschließend reichen die Erkenntnisse aber nicht aus, um die gesamten Auswirkungen in ihrer Breite zu erfassen.
Taquet, M. et al: "6-month neurological and psychiatric outcomes in 236 379 survivors of COVID-19: a retrospective cohort study using electronic health records" published online first in The Lancet Psychiatry on April 06, 2021 DOI: https://doi.org/10.1016/S2215-0366(21)00084-5
7. April 2021
------------------------------------------
Wenn bei einer Corona-Infektion fünf spezifische Symptomen in den ersten sieben Tagen der Infektion auftreten, erhöht sich das Risiko für Long-COVID. Das zeigt eine Analyse internationaler Krankendaten.
Insgesamt wurden in der prospektiven, beobachtenden Kohortenstudie 4.182 Patientendaten und Symptomberichte analysiert. Von den untersuchten Patienten berichteten gut 13 Prozent von zurückbleibenden Beschwerden und Krankheitssymptomen, 4,5 Prozent hatten die Symptome länger als 8 Wochen und 2,3 Prozent länger als 12 Wochen.
Die 4.182 Probanden hatten sich bei der Anmeldung in einer Corona-App körperlich normal gefühlt, was eine genaue Bestimmung des Symptombeginns ermöglichte. Sie hatten dann angegeben, positiv auf SARS-CoV-2 getestet worden zu sein.
Risiko steigt mit Symptomen, Alter und Gewicht
Die Forschenden stellten bei der Auswertung fest, dass mit zunehmendem Alter und Gewicht das Risiko hier grundsätzlich steigt. Auch waren in der Patientengruppe häufiger Frauen als Männer betroffen. Zu den prädikativen Symptomen gehören Heiserkeit, Müdigkeit, Kopf- sowie Muskelschmerzen und Atemlosigkeit in der ersten Woche der Erkrankung. Traten diese auf, war die Assoziation mit Long-COVID häufiger.
Anhand der Erkenntnisse entwickelten die Forschenden ein Modell zur Unterscheidung von kurzen COVID-Erkrankungen und Long-COVID. Es könnte in vereinfachter Form in Kliniken angewendet werden. Das Modell wurde auf Datenbasis von 2.149 Patienten erstellt und mit einer unabhängigen Gruppe von 2.472 positiv getesteten Patienten überprüft.
Erkrankte, die Symptome über 28 Tage nach einer Infektion mit SARS-CoV-2 hinaus zeigen, erhalten Long-COVID als Diagnose. Zu den Beschwerden gehören vor allem Fatigue, Kopfschmerz, Atemlosigkeit und Störungen des Geruchssinns. Nach heutigem Wissensstand raten Ärzte bei Symptomen, die über zwölf Wochen hinaus anhalten, weitere Untersuchungen anzustellen und die Beschwerden abzuklären.
Sudre, C. H. et al: "Attributes and predictors of long COVID" published in Nature Med. on March 10, 2021. DOI: 10.1038/s41591-021-01292-y
30. März 2021
------------------------------------------
Wer eine Infektion mit dem neuartigen Coronavirus durchgemacht hat, besitzt den aktuellen Erkenntnissen nach einen 80-prozentigen Schutz vor einer erneuten Erkrankung - zumindest temporär. Wie sinnvoll ist also die Impfung von Infizierten?
Wissenschaftler an der Universität in Sheffield werteten die Daten von Mitarbeitern im Gesundheitswesen aus, die bereits infiziert waren und verglichen sie mit denen von nicht-infizierten Personen, die bereits zwei Mal geimpft wurden. Im Rahmen der SIREN-Studie (SARS-CoV-2 Immunity and Reinfection Evaluation) wurde in der Teilstudie PITCH (Protective Immunity from T-cells in Healthcare Workers) analysiert, inwieweit sich der Immunschutz bei Personen, die bereits eine Infektion überstanden haben, durch die einmalige Impfung mit dem BioNTech/Pfizer-Vakzin BNT162b2 verstärkt.
Impfung "boostet" auch Immunantwort von Infizierten
Für die vergleichende Untersuchung wurden zwei Tests in den beiden Gruppen durchgeführt. Zum einen wurde der Schutz durch Antikörper mittels der B-Zellen-Antwort gemessen, bei der die Viren außerhalb der menschlichen Zellen abgefangen und unschädlich gemacht werden. Zum anderen analysierten die Forscher auch die aufwendiger zu testende T-Zellen-Antwort. Die T-Zellen zerstören das in die Zellen bereits eingedrungene Virus. Diese zelluläre Immunantwort spielt eine wichtige Rolle bei der Abwehr der Coronaviren.Im Ergebnis erhöhte sich der Schutz noch einmal deutlich. Er war nach der einmaligen Impfdosis und der bereits gebildeten körpereigenen Immunantwort sogar höher als der Immunschutz von Personen, die noch nicht infiziert, aber zweifach geimpft waren. Die Impfung kann also die Schutzwirkung durch eine frühere Infektion messbar verstärken und wird daher von den Forschern empfohlen. Sie unterstützt eine breite Immunantwort, da T-Zellen und Antikörper mehr Stellen des Spike-Proteins erkennen als nach nur einer Impfung oder einer Infektion. Bei den Untersuchungen wurden auch Antikörper gegen die Varianten B.1.1.7 aus Großbritannien, B.1.135 aus Südafrika und P.1 aus Brasilien gefunden. Daher sollte den Forschern zufolge nicht auf eine Nachimpfung verzichtet werden.
Konkret waren die Antikörper-Titer 6,8-fach höher als bei Personen ohne Infektion nach der ersten Impfung und rund drei Mal höher als nach der zweiten Dosis.
Angyal, A. et al: "T-Cell and Antibody Responses to First BNT162b2 Vaccine Dose in Previously SARS-CoV-2-Infected and Infection-Naive UK Healthcare Workers: A Multicentre, Prospective, Observational Cohort Study" published on March, 25, 2021 in The Lancet. DOI: http://dx.doi.org/10.2139/ssrn.3812375
18. März 2021
------------------------------------------
Eine große Studie aus Dänemark zeigt, dass es selten zu einer Reinfektion mit SARS-CoV-2 kommt. Der durchschnittliche Schutz nach einer Infektion liegt bei 80 Prozent. Das Risiko haben eher Ältere.
Dänische Forscher haben umfangreich mikrobiologische Daten der kostenlosen Massentests analysiert, die 2020 allen Dänen angeboten wurden. Im vergangenen Jahr ließen sich rund 4 Millionen Dänen testen, das sind 69 Prozent der Gesamtbevölkerung. Insgesamt wurden im Rahmen des Testprojekts 10,6 Millionen PCR-Test durchgeführt. Darunter war also auch eine große Zahl von Mehrfachtestungen.
Die Wissenschaftler analysierten die Daten von reinfizierten Patienten, die sowohl während der ersten Welle von März bis Juni 2020 als auch während der zweiten Welle der Pandemie von September bis Dezember 2020 positiv getestet wurden, und werteten sie dann hinsichtlich Alter und Geschlecht aus. Dabei konnten sie feststellen, dass eher ältere Personen über 65 Jahren ein größeres Risiko für eine zweite Infektion haben.
Weiter gab es aber keine Anhaltspunkte dafür, dass die Wiederansteckungen bei einem Geschlecht häufiger auftreten als beim anderen. Auch fanden die Wissenschaftler keine Hinweise darauf, ob der Schutz in den ersten drei bis sechs Monaten einer Infektion höher war als nach sieben Monaten. Der Schutz nach einer überstandenen Infektion betrug im Durchschnitt 80 Prozent. Reinfektionen waren eher selten.
Die Studienerkenntnisse seien für die Weiterentwicklung der Impfstrategie wichtig, da die Immunabwehr bei älteren Personen eher eine Reinfektion zulässt, so das Fazit.
Hansen, C. H. et al: "Assessment of protection against reinfection with SARS-CoV-2 among 4 million PCR-tested individuals in Denmark in 2020: a population-level observational study" published on March 17, 2021. In The Lancet. doi.org/10.1016/S0140-6736(21)00575-4
16. März 2021
------------------------------------------
Eine Studie aus Schottland erhärtet die Vermutung, dass SARS-CoV-2-Geimpfte weniger infektiös sind: Nachdem Mitarbeiter im Gesundheitswesen mit AstraZeneca und BionTech geimpft wurden, gingen auch die Ansteckungen in ihren Familien deutlich zurück.
Seit dem 8. Dezember 2020 wird in Schottland gegen SARS-CoV-2 geimpft. Den Auftakt macht dabei auch das Personal im Gesundheitswesen. Für eine Studie untersuchte ein Projekt unter der Leitung von David McAllister der Universität Glasgow, inwieweit deren Impfung sich auf die Infektionshäufigkeit von Familien- beziehungsweise Haushaltsmitgliedern auswirkt. Im Ergebnis kam es bereits nach der ersten Impfung der Mitarbeiter aus Gesundheitsberufen zu deutlich weniger Ansteckungen in deren Familien. Das unterstreicht die Hoffnung auf die sogenannte sterile Immunität, also dass geimpfte Personen das Virus nicht übertragen.
Bereits Anfang März 2021 waren 78,3 Prozent der Mitarbeiter im Gesundheitswesen mindestens ein Mal geimpft. Dafür wurden die Vakzine von AstraZeneca und BioNTech verwendet. Schon nach der ersten Impfung gingen die Erkrankungen unter den Geimpften um 55 Prozent zurück. Zudem sanken die schweren Krankheitsfälle mit einer Einlieferung ins Krankenhaus um 84 Prozent. Bei den Angehörigen ging die Zahl der Infektionen um 30 Prozent zurück.
Nach der zweiten Impfung zeigte sich die Wirkung besonders deutlich: Die Infektionen nahmen um 92 Prozent ab und es waren keine Hospitalisierungen mehr notwendig. Infektionen bei Haushaltsmitgliedern gingen um 54 Prozent zurück. Da diese Personen selbst auch Kontakt zu anderen Personen außerhalb des Haushalts hatten, sind Infektionen hier nicht vollkommen ausgeschlossen. Die Wissenschaftler gehen daher von einem Schutzeffekt über den eigenen Infektionsschutz hinaus aus.
McAllister, D. et al: "Effect of vaccination on transmission of COVID-19: an observational study in healthcare workers and their households" published as pre print on March 12, 2021.
11. März 2021
------------------------------------------
Eine Studie auf Südkorea legt nahe, dass die Immunität bei Älteren, schwer Erkrankten und vor allem bei Patienten mit einer manifestierten Lungenentzündung länger anhält.
Eine Kohorten-Studie aus Südkorea die Antikörper von asymptomatischen Infizierten als auch von unterschiedlich schwer Erkrankten mit und ohne Lungenentzündung bestimmt. Ziel war, die Dauer der SARS-CoV-2-spezifischen humoralen und zellulären Immunität in Abhängigkeit vom klinischen Schweregrad der Erkrankung zu bewerten.
Über 85 Prozent haben Antikörper länger als sechs Monate
Bis zu sechs Monate nach der Diagnose konnten Virus-Antikörper nachgewiesen werden. So waren spezifische Immunglobulin-G-Werte (IgG) bei 66,7 Prozent der Patienten nachweisbar und bei 86,9 Prozent neutralisierende Antikörper.
Auffällig war, dass ältere Erkrankte, Patienten mit schweren Verläufen und hierbei vor allem solche mit einer manifestierten Lungenentzündung eine längere Immunität aufwiesen. Die SARS-CoV-2-spezifische T-Zellantworten zeigten sich bei pneumonischen Patienten stark ausgeprägt.
Zusammenfassend lässt sich den Autoren zufolge sagen, dass mehr als 85 Prozent der Patienten bis sechs Monate nach der Diagnose einer SARS-CoV-2-Infektion NAb in sich tragen, was Erkenntnisse für die Etablierung von Impfstrategien gegen COVID-19 liefert.
Noh, J. et al. "Longitudinal Assessment of Anti-SARS-CoV-2 Immune Responses for Six Months Based on the Clinical Severity of COVID-19." Published in The Journal of Infectious Diseases, March 4, 2021. https://doi.org/10.1093/infdis/jiab124
10. März 2021
------------------------------------------
Eine Impfung gegen SARS-CoV-2 kann eine symptomatische COVID-Erkrankung verhindern. Nun zeigen drei Studien erstmals, dass die Schutzwirkung der Impfungen auch asymptomatische Infektionen umfasst.
Die Erkenntnisse deuten darauf hin, dass es nicht nur Schutz vor Erkrankung, sondern auch Schutz vor einer Infektion durch eine Impfung entstehen kann. Diese Schutzwirkung würde großen Einfluss auf das Infektionsgeschehen haben und den Verlauf der Pandemie empfindlich reduzieren, so die Kommentare zu den Ergebnissen.
Publikationen der Cambridge University, des Public Health England Colindale aus England und eine Daten-reiche Studie aus Israel untersuchten die Schutzwirkung der Impfstoffe von BioNTech (BNT162b2) und AstraZeneca (AZD1222). Neue Daten des Addenbrooke's Hospital in Cambridge deuten demnach darauf hin, dass eine einzige Dosis des Impfstoffs von Pfizer BioNTech die Zahl der asymptomatischen SARS-CoV-2-Infektionen um 75 Prozent reduzieren kann. Dies impliziert, dass der Impfstoff das Risiko einer Übertragung des Virus von Menschen, die asymptomatisch sind, signifikant reduzieren könnte und auch andere vor einer Erkrankung schützt. Auch die Untersuchung von Krankenhauspersonal durch das Public Health England Colindale ergab, dass der BNT162b2-Impfstoff sowohl symptomatische als auch asymptomatische Infektionen bei Erwachsenen "im arbeitsfähigen Alter" wirksam verhindert. Die Kohorte wurde geimpft, als die dominante Variante im Umlauf B1.1.7 war, und belegt demnach die Wirksamkeit gegen diese Variante.
In Tel Aviv zeigen die landesweiten Daten zur Impfung, dass geimpfte Personen eine geringere Virusmenge in sich tragen. Das belegen die PCR-Testungen anhand der für die Viruslast-Bestimmung benötigten Zyklen. Noch wissen die Forschenden hier nicht, wie lange der Schutz auch gegen die asymptomtischen Infektionen bestehen bleibt.
Die Ergebnisse der Pre-Print-Studien müssen nun weiter bewertet und verifiziert werden.
Jones, N. K. et al: "Single-dose BNT162b2 vaccine protects against asymptomatic SARS-CoV-2 infection" in Authorea. Feb, 24, 2021. DOI: 10.22541/au.161420511.12987747/v1
Hall, V. J. et al: "Effectiveness of BNT162b2 mRNA Vaccine Against Infection and COVID-19 Vaccine Coverage in Healthcare Workers in England, Multicentre Prospective Cohort Study" in The Lancet on Feb, 22, 2021. DOI: http://dx.doi.org/10.2139/ssrn.3790399
Dagon, N. et al: "BNT162b2 mRNA Covid-19 Vaccine in a Nationwide Mass Vaccination Setting" in NEJM on Feb, 24, 2021. DOI: 10.1056/NEJMoa2101765
3. März 2021
------------------------------------------
Das Hospitalisierung-Risiko von COVID-Patienten steigt mit kardiometabolischen Erkrankungen
Forschende der Friedman School of Nutrition Science and Policy, Boston (USA), werteten für ihre Studie repräsentative Daten zur Verbreitung von kardiometabolischen Erkrankungen in den USA zwischen 2015 und 2018 sowie US-Register zur Hospitalisierung von COVID-Patienten aus.
Ergebnis: Bis zum 18. November 2020 wurden in den USA mehr als 906.000 Erwachsene aufgrund einer COVID-19-Erkrankung hospitalisiert. Davon entfielen einer Studie zufolge schätzungsweise
20,5 Prozent (Unsicherheitsintervall 95 Prozent, Schwankungsbreite 18,9 bis 22,1 Prozent) auf Diabetes mellitus,
30,2 Prozent (Unsicherheitsintervall 95 Prozent, Schwankungsbreite 28,2 bis 32,3 Prozent) auf Adipositas,
26,2 Prozent (Unsicherheitsintervall 95 Prozent, Schwankungsbreite 24,3 bis 28,3 Prozent) auf Bluthochdruck und
11,7 Prozent (Unsicherheitsintervall 95 Prozent, Schwankungsbreite 9,5-14,1 Prozent) auf Herzinsuffizienz.
Gemeinsam betrachtet (häufig waren Komorbiditäten vorhanden) waren 63,5 Prozent (Unsicherheitsintervall 95 Prozent, Schwankungsbreite 61,6 bis 65,4 Prozent) oder 575.419 (Unsicherheitsintervall 95 Prozent, Schwankungsbreite 559 072 bis 593 412) der COVID-19-Krankenhausaufenthalte auf diese vier Zustände zurückzuführen, folgern die Autoren weiter. Es wurden große Unterschiede in den Anteilen der kardiometabolischen risikobehafteten COVID-19-Krankenhausaufenthalte nach Alter und Rasse / ethnischer Zugehörigkeit festgestellt, wobei kleinere Unterschiede nach Geschlecht auftraten.
Fazit: Ein erheblicher Teil der COVID-19-Krankenhausaufenthalte in den USA scheint auf schwerwiegende kardiometabolische Erkrankungen zurückzuführen zu sein, schreiben die Forschenden. Ihre Hoffnung ist, dass die Ergebnisse dazu beitragen, Präventionsstrategien zu entwickeln, um die Belastung des Gesundheitswesens zu verringern.
Meghan O'Hearn et al. "Coronavirus Disease 2019 Hospitalizations Attributable to Cardiometabolic Conditions in the United States: A Comparative Risk Assessment Analysis", Journal of the American Heart Association, Published 25 Feb. 2021, https://doi.org/10.1161/JAHA.120.019259
1. März 2021
------------------------------------------
B.1.1.7 führt zu längerer Infektionsdauer
Vorläufige Studienergebnisse deuten darauf hin, dass die SARS-CoV-2-Variante B.1.1.7 deshalb übertragbarer ist, weil sie mehr Zeit in ihrem Wirt verbringt als der Wildtyp.
Forschende der Harvard T. H. Chan School of Public Health in Boston (USA) untersuchten in einer bisher als Preprint erschienenen Studie die täglichen SARS-CoV-2-Tests von 65 Infizierten, darunter sieben mit B.1.1.7. Sie beobachteten, wie lange die Infektion anhielt und wie viel Virus zu jedem Zeitpunkt vorhanden war.
Ergebnis: Bei Menschen, die mit B.1.1.7 infiziert waren, dauerten die Infektionen durchschnittlich 13,3 Tage, verglichen mit 8,2 Tagen bei anderen Varianten. Ansonsten gab es kaum Unterschiede in den Spitzenkonzentrationen des Virus zwischen den beiden Gruppen.
Diese Ergebnisse deuten darauf hin, dass B.1.1.7 deshalb leichter übertragen werden kann als andere Varianten, weil Betroffene einfach längere Zeit infiziert sind und daher eine größere Anzahl von Kontakten infizieren können. Möglicherweise rechtfertigen die Erkenntnisse längere Quarantänezeiten für Personen, die mit dieser Variante infiziert sind, schlussfolgern die Wissenschaftlerinnen und Wissenschaftler aus Boston.
Kissler, Stephen et al. "Densely sampled viral trajectories suggest longer duration of acute infection with B.1.1.7 variant relative to non-B.1.1.7 SARS-CoV-2." Preprint, 2021, https://dash.harvard.edu/handle/1/37366884
25. Februar 2021
------------------------------------------
Schottland: Impfung reduziert schwere COVID-Verläufe um bis zu 94 Prozent
Mit den Vakzinen von BioNTech/Pfizer und AstraZeneca Geimpfte haben ein um bis zu 94 Prozent reduziertes Risiko für einen schweren COVID-Verlauf. Das zeigt eine schottische Kohortenstudie.
Die Studie umfasst die gesamte schottische Bevölkerung (n=5,4 Millionen). Die Daten wurden zwischen dem 8. Dezember und dem 15. Februar 2020 erhoben. In diesem Zeitraum wurden in Schottland 1,14 Millionen Menschen gegen Corona geimpft. 650.000 Menschen erhielten dabei den Impfstoff von BioNTech/Pfizer, 490.000 das Vakzin von AstraZeneca.
Die Forscher analysierten die Daten jede Woche, bezogen Aufzeichnungen von Hausärzten über Impfungen, Krankenhauseinweisungen, Sterberegistrierungen und Labortestergebnisse ein und verglichen die Ergebnisse mit den Daten von Ungeimpften.
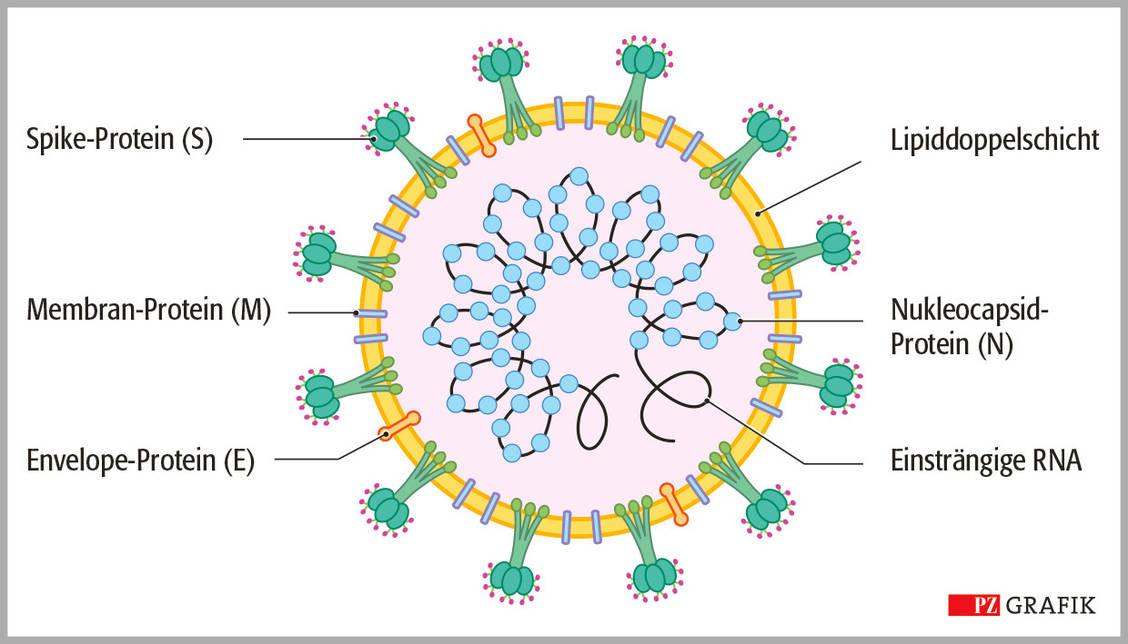
Das Ergebnis: Allein die erste Dosis des BioNTech/Pfizer-Impfstoffs reduzierte in 28 bis 34 Tagen nach der Impfung die Zahl der Hospitalisierungen wegen COVID-19 um 85 Prozent. Im selben Zeitraum betrug der Impfeffekt für das AstraZeneca-Vakzin 94 Prozent.
Bei Personen im Alter von 80 Jahren und älter war die Impfung mit einer 81-prozentigen Verringerung des Krankenhausaufenthaltsrisikos in der vierten Woche verbunden, wenn beide Impfstoffe kombiniert wurden.
Das Studienteam geht davon aus, dass die Ergebnisse auf andere Länder übertragbar sind. Sie weisen darauf hin, dass die Daten keine Vergleiche zwischen den beiden Impfstoffen zulassen.
Eleftheria Vasileiou et al.: "Effectiveness of First Dose of COVID-19 Vaccines Against Hospital Admissions in Scotland: National Prospective Cohort Study of 5.4 Million People." publishes online in The Lancet on February 19, 2021. Doi: https://papers.ssrn.com/sol3/papers.cfm?abstract_id=3789264
24. Februar 2021
------------------------------------------
London: Herzschäden bei der Hälfte der schwer COVID-Erkrankten
Bei schweren COVID-Erkrankungen manifestieren sich bei rund der Hälfte der hospitalisierten Patienten Herzschäden - vor allem des Herzmuskels.
Ein Indikator dafür ist der erhöhte Troponin-Wert, da Troponin Teil der Herzmuskelzellen ist. Sein Anstieg hängt zum Beispiel auch mit dem Abfall der Kardiomyozyten zusammen, was auf eine Infektion der Herzmuskelzellen oder eine Herzmuskelentzündung hinweist. Auch ein thrombotischer Verschluss einer Koronararterie, der zum Herzinfarkt führen kann, kann den Wert steigen lassen und eine Spätfolge der COVID-Infektion sein.
Ein Team aus Kardiologen des University College London hat für eine Studie 148 Patienten aus verschiedenen Kliniken mittels kardiovaskulärer Magnetresonanztomografie untersucht. Ein Drittel der Patienten wurde auf den Intensivstationen behandelt. Dabei wurde jedoch keine Verminderung der Pumpleistung am Herzen der ehemals schwer Erkrankten festgestellt. Lediglich bei 17 Patienten zeigte sich eine leicht abgeschwächte Leistung, die aber wohl auf vorliegende Vorerkrankungen zurückzuführen ist.
Daher gehen die Spezialisten davon aus, dass es bei einem schweren Verlauf durch den Troponin-Anstieg kurzfristig zu einer Herzinsuffizienz kommt. Ob die Schäden am Herzen dauerhaft sein können, ist noch nicht vollständig geklärt. Allerdings dokumentierte das Team bei der Hälfte der Patienten Herzmuskelschäden, wie Narbenbildung an dem Muskel, oder Schädigungen, die auf einen Infarkt hindeuten beziehungsweise auf ein ischämisches Verletzungsmuster (Blutleere).
Kotecha, T. et al: "Patterns of myocardial injury in recovered troponin-positive COVID-19 patients assessed by cardiovascular magnetic resonance" published in European Heart Journal on 18 Feb. 2021 https://doi.org/10.1093/eurheartj/ehab075
22. Februar 2021
------------------------------------------
Adipositas erhöht Sterberisiko von COVID-Patienten um 42 Prozent
Fettleibigkeit wird bereits seit Beginn der Corona-Pandemie mit einer erhöhten Sterblichkeit in Verbindung gebracht. Wissenschaftler aus Taiwan führten jetzt einen systematischen Review mit Meta-Analyse durch und untersuchten dazu 17 zwischen Januar und August 2020 erschienene Publikationen, die insgesamt mehr als 540.000 Patientenfälle umfassten.
Das Ergebnis: 16 dieser Studien berichten über ein signifikant erhöhtes Sterblichkeitsrisiko bei Patienten mit COVID-19, eine Studie von einem verringerten Sterblichkeitsrisiko. In der Gesamtauswertung ergab die Meta-Analyse ein signifikant erhöhtes Sterblichkeitsrisiko (+42 Prozent, Konfidenzintervall 95 Prozent, Schwankungsbreite 1,24 bis 1,63, p < 0,001) bei Adipositas. Dabei wiesen die ausgewerteten Studien laut den Autoren nur eine moderate Heterogenität auf.
Die Forschenden unterschieden in ihrer Betrachtung zudem die verschiedenen Klassen von Adipositas: die Klasse III war stark mit einem erhöhten Sterblichkeitsrisiko verbunden (+92 Prozent, Konfidenzintervall 95 Prozent, Schwankungsbreite 1,50 bis 2,47, p < 0,001). Adipositas der Klassen I und II zeigte auch einen starken Zusammenhang mit einem erhöhten Sterblichkeitsrisiko, das Risiko stieg um 27 Prozent (Konfidenzintervall 95 Prozent, Schwankungsbreite 1,05 bis 1,54, p = 0,01) sowie um 56 Prozent (Konfidenzintervall 95 Prozent, Schwankungsbreite 1,11 bis 2,19, p < 0,01).
Die Forschenden betonen, dass nur von Experten begutachtete Artikel für die Berechnung der Risikogröße einbezogen wurden. Die Gesamtqualität der Evidenz der Metaanalyse sei Prüfungen mit dem QUIPS-("Quality In Prognosis Studies")-Tool zufolge stark. In der Metaanalyse wurde auch untersucht, wie verschiedene Komorbiditäten von Adipositas-Patienten mit COVID das Sterberisiko beeinflussen. Ausgewiesen wurden:
Schlaganfall +80 Prozent (Konfidenzintervall 95 Prozent, Schwankungsbreite 0,89-3,64, p = 0,10)
Chronische Nierenerkrankung CKD +57 Prozent, Konfidenzintervall 95 Prozent, Schwankungsbreite 1,57 bis 1,91, p < 0,001)
Chronisch obstruktive Lungenerkrankung COPD +34 Prozent (Konfidenzintervall 95 Prozent, Schwankungsbreite 1,18 bis 1,52, p < 0,001)
Diabetes +19 Prozent (Konfidenzintervall 95 Prozent, Schwankungsbreite 1,07 bis 1,32, p = 0,001) und
Bluthochdruck +7 Prozent, Konfidenzintervall 95 Prozent, Schwankungsbreite 0,92 bis 1,25, p = 0,35)
Ärzte sollten sich dieser Risikofaktoren bewusst sein und eine schnelle Entscheidung für eine Intervention treffen, schlussfolgern die Autoren. Zudem seien weitere Studien dringend erforderlich, um den pathophysiologischen Zusammenhang zwischen Adipositas und dem Sterblichkeitsrisiko bei COVID-19-Patienten zu klären.
Tahmina Nasrin Poly et al. "Obesity and Mortality Among Patients Diagnosed With COVID-19: A Systematic Review and Meta-Analysis", Front. Med., 05 February 2021 | doi.org/10.3389/fmed.2021.620044
18. Februar 2021
------------------------------------------
Erst COVID, dann Diabetes?
SARS-CoV-2 infiziert bei gravierenden Krankheitsverläufen die Bauchspeicheldrüse. Dies erklärt möglicherweise das Auftreten von Diabetes-ähnlichen Symptomen von COVID-19-Patienten sowie die Verschlechterung des Zuckerstoffwechsels bei coronakranken Diabetikern.
In einer Studie konnten Ulmer Forscher nun nachweisen, dass SARS-CoV-2 bei gravierenden Krankheitsverläufen die insulinproduzierenden Beta-Zellen der Bauchspeicheldrüse infiziert.
Infizierte Beta-Zellen zeigen Veränderungen in Form und Funktion
Für die Untersuchung haben die Forscher Gewebe aus der Bauchspeicheldrüse mit SARS-CoV-2 in Kontakt gebracht und so herausgefunden, dass sich die sogenannten Langerhans'schen Inseln mit dem Virus infizieren lassen.
"Die Beta-Zellen exprimieren bestimmte Eiweißmoleküle, ohne die SARS-CoV-2 die Zellen nicht infizieren kann. Die körpereigenen Proteine TMPRSS2 und ACE2 sind sozusagen das Schloss, über das die Coronaviren mit ihrem Schlüsselprotein (Spike-Protein) in die Zellen eindringen. Daraufhin vervielfältigen sich die Virus-Bausteine, und viele neue infektiöse Viruspartikel werden freigesetzt", erklärt Prof. Jan Münch, Studienleiter vom Institut für Molekulare Virologie.
Zudem ergab die Untersuchung von verstorbenen Patienten, dass das Virus eine Infektion des Pankreas auslöste. Erstaunlicherweise war im Lungengewebe das Virus zum Teil nicht mehr nachzuweisen, in der Bauchspeicheldrüse dagegen schon. Dies deutet möglicherweise darauf hin, dass das neuartige Coronavirus nicht nur außerhalb der Lunge aktiv ist und andere Organe infiziert, sondern dass diese Infektionen häufiger und andauernder sind als bisher angenommen.
Weiter konnte in der Studie festgestellt werden, dass in diesen Fällen die Ausschüttung von Insulin gestört war.
Müller, J. A. et al. "SARS-CoV-2 infects and replicates in cells of the human endocrine and exocrine pancreas" published on 3 Feb 2021 in Nature Metabolism DOI: 10.1038/s42255-021-00347-1
15. Februar 2021
------------------------------------------
Autoantikörper könnten schwere COVID-Verläufe auslösen
Schon länger deuten Studien darauf hin, dass Auto-Antikörper verantwortlich für schwere COVID-Verläufe sein könnten. Jetzt wurde ein Mechanismus beschrieben, der die wichtigsten klinischen Befunde erklären kann.
Im Januar 2021 analysierten Forscher der New York University (NYU) Serumsproben von 86 Personen, die mit COVID-19 ins Krankenhaus eingeliefert worden waren auf Auto-Antikörper gegen Proteine wie Annexin A2. Es ist für die Zellmembranstabilierung und -reparatur nötig und gewährleistet die Integrität der kleinen Blutgefäße in der Lunge.
Die Forscher fanden einen signifikant höheren durchschnittlichen Spiegel von Anti-Annexin-A2-Antikörpern bei Patienten mit kritischem Verlauf als bei solchen mit einem weniger schweren Verlauf. Bei den Auto-Antikörpern gegen Annexin A5 wurden hingegen keine signifikanten Unterschiede bei den Antikörpern festgestellt. Anders als bei dem Anti-Annexin-A5-Antikörperspiegel korrelierte der A2-Antikörperspiegel stark mit der Sterblichkeit der Patienten.
Da bekannt sei, dass die Hemmung von Annexin A2 systemische Thrombose, Zelltod und nicht-kardiogenes Lungenödem induziert, schlussfolgern die Autoren, dass die Autoimmunität gegenüber Annexin A2 ein potenzieller Mechanismus ist, der die wichtigsten klinischen Befunde von schwerem COVID-19 erklären kann.
Marisol Zuniga et al."Autoimmunity to the Lung Protective Phospholipid-Binding Protein Annexin A2 Predicts Mortality Among Hospitalized COVID-19 Patients", medRxiv 2020.12.28.20248807; doi: https://doi.org/10.1101/2020.12.28.20248807
Coronaviren in Fledermäusen können direkt Menschen infizieren
Forscher der University of North Carolina implantierten Mäusen menschliches Lungengewebe und infizierten das Gewebe mit verschiedenen Coronaviren, darunter SARS-CoV, MERS-CoV und SARS-CoV-2 sowie zwei eng verwandte Coronaviren, die von Fledermäusen isoliert wurden.
Ergebnis: Die Infektion und Virusreplikation erforderte in diesem Modell keine Anpassung des Virus. Die akute SARS-CoV-2-Infektion war hochzytopathisch und induzierte eine robuste und anhaltende Typ-I-Interferon und entzündliche Zytokin/Chemokin-Reaktion. Die Ergebnisse deuten darauf hin, dass Fledermäuse endogene Coronaviren beherbergen, die in der Lage sind, ohne Zwischenwirt direkt Menschen zu infizieren.
Die Forscher nutzten das Tiermodell auch, um zu zeigen, dass die therapeutische und prophylaktische Verabreichung von EIDD-2801, einem oralen Breitspektrum-Virostatikum, das sich derzeit in klinischen Phase-II-III-Studien befindet, die SARS-CoV-2-Replikation in vivo stark hemmte. Das Präparat könnte, so die Einschätzung der Autoren, ein erhebliches Potenzial für die Prävention und Behandlung von COVID-19 haben.
Wahl, Angela et al. "SARS-CoV-2 infection is effectively treated and prevented by EIDD-2801". Nature (2021). https://doi.org/10.1038/s41586-021-03312-w
12. Februar 2021
------------------------------------------
Stereoid-haltige Asthmasprays unterbinden die Replikation von SARS-CoV-2 und können so schwere Verläufe verhindern.
Medizinern aus China war bereits früh aufgefallen, dass Asthma-Patienten seltener schwer an COVID-19 erkranken, obwohl bei ihnen eine chronische Atemwegsentzündung vorliegt. Lag das eventuell daran, dass die meisten Asthmatiker heute via Sprays Steroide inhalieren?
In Laborstudien kam heraus, dass die in handelsüblichen Asthma-Sprays enthaltenen Steroide, wie Glukokortikoide, die Vermehrung von SARS-CoV-2 im Atemwegsepithelien hemmen können. Nach einer weiteren Recover-Studie zeigte sich, dass der Verlauf der Infektion signifikant leichter ausfiel. Personen, die eine niedrige Dosis von Dexamethason, dem künstlichem Glukokortikoid, erhielten seltener verstarben. Seitdem werden Steroiden bei schweren Verläufen schon standardmäßig eingesetzt.
Eine Studie aus Oxford bestätigt nun, dass die Anwendung von Steroid-haltigen Asthmasprays schwere COVID-19-Krankheitsverläufe verhindern und milde Verläufe verkürzen kann. Die neue Studie ergab, dass inhalatives Budesonid, das Patienten mit COVID-19 innerhalb von sieben Tagen nach Auftreten der Symptome verabreicht wird, auch die Genesungszeit verkürzt. Budesonid ist ein Kortikosteroid, das bei der Langzeitbehandlung von Asthma und chronisch obstruktiver Lungenerkrankung (COPD) eingesetzt wird.
Bei einer zweimaligen Anwendung am Tag mit etwa 800 μg des Wirkstoffs über 28 Tage wurde das Risiko eines schweren Krankheitsverlaufs um 90 Prozent gesenkt. Darüber hinaus stellte die randomisierte Zwei-Phasen-Studie fest, dass auch milde Infektionsverläufe um durchschnittlich einen Tag verkürzt wurden bei der Anwendung von Asthma-Spray.
Die Teilnehmer, die den Budesonid-Inhalator erhielten, hatten auch ein schnelleres Abklingen von Fieber und Symptomen sowie weniger anhaltende Symptome nach 28 Tagen. Die Studie zeigte auch, dass es bei denjenigen, die Budesonid erhielten, zu einer Verringerung der anhaltenden Symptome kam.
Da die Studie jedoch nur 146 Patienten umfasste, sollte für eine gesicherte Evidenz eine größere randomisierten Doppelblindstudie folgen.
Ramakrishnan, S. et al. "Inhaled budesonide in the treatment of early COVID-19 illness: a randomised controlled trial" Preprint published on MedRxiv on 8 Feb 2021 DOI: https://www.medrxiv.org/content/10.1101/2021.02.04.21251134v1
10. Februar 2021
------------------------------------------
Impfstoff CoronaVac verhindert zu 100 Prozent schwere COVID-Verläufe
Der chinesische Impfstoffhersteller Sinovac hat Ergebnisse seiner Phase III-Studien bekanntgegeben. Das Vakzin soll hoch exponiertes Gesundheitspersonal absolut sicher schützen. Aber es bleiben offene Fragen.
Der chinesische Impfstoffhersteller Sinovac Biotech hat in einer Pressemitteilung die Ergebnisse der Phase III-Studien zu seinem Vakzin bekanntgegeben. Eine Publikation der Studienergebnisse steht jedoch noch aus. Die Versuche mit dem COVID-19-Impfstoff CoronaVac waren in Brasilien, der Türkei, Indonesien und Chile mit insgesamt 25.000 Probanden durchgeführt worden.
Die Phase-III-Studien in Brasilien und der Türkei bewerteten die Wirksamkeit des Impfstoffs bei Gesundheitspersonal, das COVID-19-Patienten behandelt. Beide Studien wurden randomisiert, doppelblind und Placebo-kontrolliert durchgeführt.
Ergebnis: 14 Tagen nach der Impfung mit zwei Dosen verhinderte der Impfstoff eine symptomatische SARS-CoV-2-Infektion in 50,65 Prozent der Fälle. Schwere Krankheitsverläufe mit einer Hospitalisierung verhinderte der Impfstoff zu 100 Prozent.
Zuvor hatte es widersprüchliche Medienmeldungen zur Wirksamkeit des Impfstoffs gegeben: Aus einer kleineren, brasilianischen Teilstudie mit knapp 1.400 Teilnehmenden war eine Wirksamkeit von knapp 70 Prozent, aus der indonesischen Teilstudie 63,5 Prozent und aus der türkischen Teilstudie 91,25 Prozent Wirksamkeit gemeldet worden.
In einer Stellungnahme erklärte Sinovac, die Teiluntersuchung in Brasilien habe ergeben, dass die Wirksamkeit um 20 Prozent steigt, wenn die zweite Impfdosis statt nach zwei erst nach drei Wochen verabreicht würde. Zudem habe es sich bei den Testpersonen in Brasilien um medizinisches Personal gehandelt, das sich um COVID-Patienten gekümmert habe. Diese seien dem hochinfektiösen Erreger stärker ausgesetzt gewesen als Personen in anderen Phase-III-Studien.
Brasilien und die Türkei haben das Vakzin von Sinovac bereits zugelassen. Das Unternehmen hat zudem mit mindestens acht Ländern Lieferverträge geschlossen, das sind Hongkong, Malaysia, Singapur, Indonesien, die Philippinen, Thailand sowie Chile und die Ukraine.
1. Februar 2021
------------------------------------------
Eine französische Studie hat die Charakteristika der beiden Krankheiten verglichen, von der Morbidität bis zur Mortalität, und dafür die Daten der French National Administrative Database von knapp 90.000 COVID-Patienten ausgewertet, die während der ersten Welle im Krankenhaus aufgenommen wurden. Dem gegenüber steht die Vergleichsgruppe von knapp 46.000 Influenza-Patienten aus der letzten Winter-Saison. Im Durchschnitt waren die Patienten zwischen 68 und 71 Jahre alt.
An COVID-19 erkrankten viel mehr übergewichtige Personen - auch sehr junge Patienten zwischen 11 und 17 Jahren - sowie Diabetiker oder Hochdruck-Patienten. Sie hatten häufiger Atemnot, Lungenembolien und Schlaganfälle während der Infektion. Die Grippe-Patienten litten hingegen vermehrt an Herzinsuffizienz, chronischen Atemwegserkrankungen, Zirrhosen und Blutarmut. Herzinfarkte und Vorhofflimmern traten bei ihnen auch öfter auf.
Es sterben mehr Patienten an COVID-19
Laut der Datenanalyse wiesen COVID-Patienten mit 16,9 Prozent zu 5,8 Prozent eine höhere Mortalität auf. Auffällig war weiter, dass sehr viel weniger Kinder mit COVID-19 ins Krankenhaus kamen als mit Influenza: 1,4 zu 19,5 Prozent. Das stützt die bisherigen Studienerkenntnisse, dass Kinder selten schwer an COVID-19 erkranken. Kamen Kinder unter fünf Jahren mit dem Coronavirus in die Klinik, mussten sie jedoch häufiger intensivmedizinisch behandelt werden als bei der Grippe: 2,3 zu 0,9 Prozent. Da Kinder in der Studie unterrepräsentiert waren, müssen die Ergebnisee den Autoren zufolge in weiteren Studien validiert werden.
Diese Ergebnisse unterstreichen demnach die Bedeutung geeigneter Präventivmaßnahmen bei COVID-19 sowie die Notwendigkeit eines Impfstoffs.
Die Ergebnisse im Überblick:
Patienten, die mit COVID-19 ins Krankenhaus kamen, waren häufiger übergewichtig als Patienten mit Influenza und wiesen andere Vorerkrankungen auf.
Das Sterberisiko war bei COVID-19 deutlich höher.
Es kamen weniger Kinder mit COVID-19 ins Krankenhaus als mit Influenza.
Piroth, L. et al. "Comparison of the characteristics, morbidity, and mortality of COVID-19 and seasonal influenza: a nationwide, population-based retrospective cohort study" published on 27 Dec in The Lancet DOI: https://doi.org/10.1016/S2213-2600(20)30527-0
28. Januar 2021
------------------------------------------
Neuer Impfstoff erzielt bis zu 100 Prozent Wirksamkeit - Produktion gestartet
Erste Aussagen zur Wirkung sind gut - auch bei Menschen über 65, die Nebenwirkungen gering. Bald sollen zum Impfstoffkandidaten Ad26.COV2.S Ergebnisse der Phase III vorliegen. Die Produktion läuft bereits.
Eine multizentrische, placebokontrollierte Phase-1-2a-Studie untersuchte sowohl für gesunde Erwachsene im Alter von 18 bis 55 Jahren (Kohorte 1) als auch Personen ab 65 Jahren (Kohorte 3) für den Impfstoffkandidaten Ad26.COV2.S Wirkung und Nebenwirkungen.
Ergebnis: Bereits nach der ersten Dosis kam es bei mehr als 90 Prozent der 805 Studienteilnehmer zur Bildung von neutralisierenden Antikörpern gegen SARS-CoV-2 . Nach 57 Tagen hatten sogar 100 Prozent Antikörper gebildet. Auch bei Älteren schlug der Impfstoff sehr gut an. Die Antikörper-Titer blieben bis mindestens Tag 71 stabil, schreiben die Autoren. Eine zweite Impfdosis sorgte für eine Erhöhung des Titers um den Faktor 2,6 bis 2,9. Spike-bindende Antikörperreaktionen ähnelten neutralisierenden Antikörperreaktionen.
Zulassungsantrag könnte im Februar erfolgen
Der US-Konzern Johnson & Johnson (J&J) arbeitet Medienberichten zufolge mit Hochdruck am geplanten Marktstart seines Corona-Impfstoffs Ad26.COV2.S in Europa. Die Produktion ist im Werk im niederländischen Leiden laut einer Unternehmenssprecherin "bereits angelaufen". Noch im Januar werde mit den Ergebnissen der Phase III Studie gerechnet, hieß es außerdem. Je nach Ergebnislage will das Unternehmen dann "zeitnah den Zulassungsantrag bei der europäischen Arznei-Mittel-Agentur (EMA) stellen."
Nach der Verabreichung der ersten Impfstoffdosis kam es in den Kohorten 1 und 3 und nach der zweiten Dosis in Kohorte 1 lediglich zu Müdigkeit, Kopfschmerzen, Muskelschmerzen und Schmerzen an der Injektionsstelle. Das häufigste systemische unerwünschte Ereignis war Fieber. Systemische Nebenwirkungen traten in Kohorte 3 weniger häufig auf als in Kohorte 1.
In Kohorte 2 werden längerfristige Daten gesammelt, die eine Einzeldosis-Gabe mit einer Gabe von zwei Dosen vergleichen. Die Ergebnisse dieser Kohorte sind nicht Gegenstand der Veröffentlichung.
Jerald Sadoff et al, "Interim Results of a Phase 1-2a Trial of Ad26.COV2.S Covid-19 Vaccine", Interim Results of a Phase 1-2a Trial of Ad26.COV2.S Covid-19 Vaccine. N Engl J Med. 2021 Jan 13. doi: 10.1056/NEJMoa2034201.
26. Januar 2021
------------------------------------------
SARS-CoV-2 greift das Herz an
Infektionen mit SARS-CoV-2 bedeuten nicht nur eine Belastung für die Lunge. Das Virus befällt auch massiv das Herz-Kreislauf-System.
Das Forschungsteam des Instituts für Molekulare und Translationale Therapiestrategien der Medizinischen Hochschule Hannover (MHH) hat in Zusammenarbeit mit den MHH-Kliniken für Kardiologie und Angiologie sowie für Pneumologie Blutproben von 38 COVID-19-Patienten untersucht, die intensivmedizinisch behandelt und beatmet wurden.
Die These: Sogenannte nicht kodierende mikroRNAs, die keine Baupläne für genetische Information tragen, spielen eine wesentliche regulatorische Rolle bei der überschießenden Immunreaktion und den anschließenden Umbauarbeiten im Bindegewebe der Lunge und des Herzens.
Dazu wurde das Blut von Grippe-Patienten mit akutem Atemnotsyndrom (Acute Respiratory Distress Syndrome ARDS) untersucht, die ebenfalls intensivmedizinisch behandelt und beatmet werden mussten, und mit dem einer gesunden Kontrollgruppe verglichen. Ergebnis: Im Vergleich zu den Gesunden war die Konzentration der mikroRNA-Marker im Blutserum der schwerkranken COVID-19-Patienten deutlich erhöht. Sie unterschied sich aber auch signifikant von den Werten der schwerkranken, ebenfalls mechanisch beatmeten Grippe-Patienten.
Der Nachweis, dass auch das Herz direkt von SARS-CoV-2-Infektionen betroffen ist, hat möglicherweise Folgen für die Behandlung Erkrankter, schreiben die Autoren. "Nach unserer Einschätzung müsste die Herzfunktion von COVID-19-Patienten im Langzeitverlauf beobachtet werden", sagt Studienleiter Prof. Dr. Dr. Thomas Thum.
Nun will das Forschungsteam untersuchen, ob mithilfe der Biomarker auch eine Prognoseabschätzung für den Krankheitsverlauf und für die Genesung möglich ist. Eine weitere Hoffnung ist, dass die mikroRNAs Ansätze für neue Therapien ermöglichen könnten.
Ankita Garg et al, "Circulating cardiovascular microRNAs in critically ill COVID‐19 patients Short title: microRNA signatures in COVID‐19", European Journal of Heart Failure, First published: 09 January 2021 https://doi.org/10.1002/ejhf.2096
25. Januar 2021
------------------------------------------
Wuhan: Sechs Monate nach der Behandlung in einer Klinik untersuchten Ärzte im Zuge einer Long-COVID-Studie die ehemaligen Patienten. Ergebnis: Insgesamt 76 Prozent klagten über anhaltende Symptome.
In der Jin Yin-tan Klinik in Wuhan wurden im Frühjahr 2020 rund 2.500 Patienten mit COVID behandelt. Sechs Monate später befragten Mediziner gut 1.700 von ihnen zu ihrem aktuellen gesundheitlichen Befinden. 390 Personen wurden für die Studie umfangreich nachuntersucht. Insgesamt gaben 76 Prozent der befragten ehemaligen Patienten an, auch nach einem halb Jahr Spätfolgen zu spüren: Bei 63 Prozent treten Müdigkeit und Muskelschwäche auf. Weiter gaben 26 Prozent Schlafstörungen und 23 Prozent sogar Depressionen an.
Bei Lungenfunktionstests wurde bei vielen Patienten eine verringerte Diffusionskapazität gemessen. Auch bestehende Milchglas-Trübungen auf den Kontrollbildern der CT geben Hinweis darauf, dass eine diagnostizierte Lungenentzündung noch nicht vollständig ausgeheilt war.
Bei 94 Prozent der Teilnehmer wurden spezifische Antikörper-Untersuchungen gemacht. Hier sankt die Seropositivität von 96 auf 58 Prozent und der durchschnittliche Titer neutralisierender Antikörper von 19 auf 10. Durch den sinkenden Immunschutz schließen die Forscher die Möglichkeit einer erneuten Ansteckung mit SARS-CoV-2 nicht aus.
Zwar langen keine Angaben zum Gesundheitszustand beziehungsweise Beschwerden und Erkrankungen vor der COVID-Infektion in dieser Studie vor, dennoch sind die möglichen Langzeitfolgen von COVID nicht von der Hand zu weisen.
Huang, C. et al. "6-month consequences of COVID-19 in patients discharged from hospital: a cohort study" published in The Lancet on 6 Jan 2021 DOI: https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(20)32656-8/fulltext
22. Januar 2021
------------------------------------------
Report aus den USA: Nur 21 Anaphylaxis-Fälle bei 1,9 Millionen Corona-Impfungen
Anaphylaxie ist eine schwere, lebensbedrohliche allergische Reaktion, die in seltenen Fällen nach der Impfung auftritt. Im Zeitraum vom 14. bis 23. Dezember 2020 wurden in den USA 21 Fälle von Anaphylaxie nach Verabreichung einer ersten Impfdosis gemeldet. Insgesamt wurden in dem Zeitraum 1.893.360 Dosen des Impfstoffs von Pfizer-BioNTech verabreicht. Das ergibt 11,1 Fälle pro einer Million Dosen, fasst die US-amerikanischen Behörde CDC (Center for Disease Control and Prevention) in einem ersten Bericht zum Thema zusammen. 71 Prozent dieser Reaktionen davon traten innerhalb von 15 Minuten nach der Impfung auf.
Insgesamt wurden 175 Fallberichte zur weiteren Überprüfung als mögliche Fälle schwerer allergischer Reaktionen, einschließlich Anaphylaxie, identifiziert. In den letztlich als Anaphylaxie definierten 21 Fällen handelte es sich bei 17 Personen um solche mit einer dokumentierten Vorgeschichte von Allergien oder allergischen Reaktionen, von denen sieben bereits eine Anaphylaxiegeschichte hatten.
Daten zum Moderna-Impfstoff sind im Bericht noch nicht enthalten
Die CDC erklärt allerdings, dass die Ergebnisse ihres Reports diversen Einschränkungen unterliegen. Zunächst wurden die Berichte über allergische Reaktionen durch passive Überwachung auf der Grundlage spontaner Berichte gesammelt. Spontane Berichterstattung unterliegt jedoch Meldevorurteilen, argumentiert die Behörde. Eine zweite potenzielle Quelle von Verzerrungen ergebe sich aus der stimulierten Berichterstattung im Zusammenhang mit einem verstärkten Bewusstsein für ein potenzielles Sicherheitsproblem.
So sei es möglich, dass die intensive mediale Aufmerksamkeit rund um das nationale COVID-19-Impfprogramm und ein erhöhtes Bewusstsein für Berichte über Anaphylaxie zu einer größeren Zahl von Verdachtsfällen führt und einen niedrigeren Schwellenwert für die frühzeitige Behandlung von Verdachtsfällen, was zu einer Zunahme der Diagnose von Verdacht auf Anaphylaxie führt. Außerdem sei es möglich, dass Datenverzögerungen und unvollständige Berichte über verabreichte Impfstoffdosen zu temporär verzerrten Werten führen.
Aktuell liegt der Fokus des Berichts auf dem COVID-19-Impfstoff von Pfizer-BioNTech. Der Grund: Daten über den Moderna-Impfstoff, der in den USA eine Woche später verfügbar wurde, waren zunächst begrenzt. Die Impfung mit dem Impfstoff Moderna COVID-19 begann am 21. Dezember 2020, und bis zum 23. Dezember 2020 wurden schätzungsweise 224.322 erste Dosen des Impfstoffs verabreicht.
Tom Shimabukoru, "Allergic Reactions Including Anaphylaxis After Receipt of the First Dose of Pfizer-BioNTech COVID-19 Vaccine - United States, December 14-23, 2020", Weekly / January 15, 2021 / 70(2);46-51, https://www.cdc.gov/mmwr/volumes/70/wr/mm7002e1.htm
19. Januar 2021
------------------------------------------
Genesene Krankenhaus-Mitarbeiter sind gut gegen Reinfektionen geschützt
Die britische SIREN-Studie (Sarscov2 Immunity & REinfection EvaluatioN) untersucht anhand einer multizentrischen prospektiven Kohorte die Auswirkungen von nachweisbaren SARS-CoV-2-Antikörpern auf die Inzidenz von COVID-19 bei Beschäftigten im Gesundheitswesen. Die mehr als 20.000 Teilnehmer sind alle in öffentlich finanzierten Krankenhäusern des Vereinigten Königreichs beschäftigt und unterziehen sich alle zwei bis vier Wochen PCR- und Antikörpertests und füllen vierzehntägig Fragebögen zu Symptomen und Expositionen aus.
Bei der Einschreibung wurden die Teilnehmer entweder der positiven Kohorte (Antikörper positiv oder vorheriger PCR-/Antikörpertest positiv) oder der negativen Kohorte (Antikörper negativ, bisher nicht bekannt als PCR/Antikörper positiv) zugeordnet. Anschließend wurden die Reinfektionsraten in der positiven Kohorte mit neuen PCR-Positiven in der negativen Kohorte verglichen.
Ergebnis: Zwischen dem 18. Juni und dem 9. November 2020 wurden 44 mögliche Reinfektionen in der positiven Kohorte (6.614 Teilnehmer) festgestellt. Nachdem geprüft wurde, ob die Tests nicht vielleicht nur verbliebene Viren der ersten Infektion erneut nachgewiesen hatten, stuften die Wissenschaftler nur zwei der 44 Fälle als "wahrscheinliche" Reinfektionen ein. Dem stehen 318 neue PCR-positive Infektionen und 94 Serokoversionen - also das erstmalige Auftreten von Antikörpern im Blutserum - in der negativen Kohorte (14.173 Teilnehmer) gegenüber.
Die bislang noch nicht begutachteten Zwischenergebnisse zeigen nach Einschätzung der Autoren, dass eine überstandene SARS-CoV-2-Infektion für mindestens fünf Monate (das entspricht der bisher ausgewerteten Laufzeit der Studie) zu einem um 83 Prozent reduzierten Infektionsrisiko führt. Möglicherweise sei der Wert sogar noch höher, weil die beobachteten Serokonversionen in dieser Kalkulation nicht berücksichtigt wurden.
Das Team fand allerdings auch heraus, dass die Reinfizierten hohe Mengen des Virus in Nase und Rachen tragen können ohne Symptome zu zeigen. Derartige Viruslasten könnten das Risiko erhöhen, das Virus zu übertragen.
Die Studie läuft nun weiter, um Aussagen zu einem über fünf Monate hinausreichenden Schutz treffen zu können. Außerdem geht es darum, die Auswirkungen der in Großbritannien zuerst sequenzierten SARS-CoV-2-Variante B.1.1.7 zu untersuchen. Denn offen ist, ob die Immunantwort gegen unterschiedliche Varianten des Virus unterschiedlich stark wirksam sind.
Hall, V. et al., "Do antibody positive healthcare workers have lower SARS-CoV-2 infection rates than antibody negative healthcare workers? Large multi-centre prospective cohort study (the SIREN study), England: June to November 2020", Preprint at medRxiv, https://doi.org/10.1101/2021.01.13.21249642.
18. Januar 2021
------------------------------------------
Männer haben um 18 Prozent höheres Risiko für schweren COVID-Verlauf
Eine Metaanalyse von 59 Studien mit 36.470 Patienten zeigt, dass Männer ein höheres Risiko für einen schweren COVID-Verlauf, einen höheren Bedarf an Intensivpflege und ein höheres Sterberisiko haben. Das relative Risiko (RR) für einen schweren Verlauf wuchs demnach im Mittel um 18 Prozent (die Schwankungsbreite lag bei einem Konfidenzintervall von 95 Prozent bei einem relativen Risiko von +10 bis +27 Prozent), für einen höheren Bedarf an Intensivpflege um 38 Prozent (Schwankungsbreite von +9 bis +74 Prozent) und ein um 50 Prozent höheres Sterberisiko (Schwankungsbreite +18 bis +91 Prozent)
Das gilt den Analysen zufolge auch für Patienten ab 70 Jahren. Sie haben ein deutlich höheres Infektionsrisiko (RR +65 Prozent, Schwankungsbreite von +50 bis +81 Prozent), ein höheres Risiko für eine schwere COVID-19-Krankheit (+105 Prozent, Schwankungsbreite von +27 bis +232 Prozent), einen höheren Bedarf an Intensivmedizin (RR +170 Prozent, Schwankungsbreite von +59 bis +360 Prozent) sowie ein höheres Sterberisiko nach der Infektion (RR +261 Prozent, Schwankungsbreite +170 bis +384 Prozent) im Vergleich zu Patienten unter 70 Jahren.
Bart G. Pijls et al. "Demographic risk factors for COVID-19 infection, severity, ICU admission and death: a meta-analysis of 59 studies." BMJ Open. 2021 Jan 11;11(1):e044640. doi: 10.1136/bmjopen-2020-044640.
14. Januar 2021
------------------------------------------
Das Coronavirus greift auch die Zellen der Darmschleimhaut an: Stuhlproben legen ein deutlich verändertes Vorkommen bestimmter Darmbakterien bei schweren Verläufen offen, wie eine kleine Studie aus Hongkong zeigt.
COVID-19 greift verschiedene Organe beziehungsweise deren Zellen im Körper an, so auch die Zellen der Darmschleimhaut. Da im Darm ein wesentlicher Teil des Immunsystems angesiedelt ist und hier das Bakterienvorkommen im Darm kontrolliert wird, liegt die Annahme nahe, dass es bei einer COVID-Erkrankung zu einer Veränderung der Darmflora kommen kann. Da das Immunsystem häufig mit einer Überreaktion auf das Virus reagiert, könnte das Einfluss auf die Zusammensetzung der Darmflora haben, vrmuten die Forscher.
An der Chinesischen Universität in Hongkong haben Forscher Stuhlproben von Erkrankten, die im Frühjahr in der Uniklinik behandelt wurden, ausgewertet. In den Proben wurden tatsächlich einige Bakterien, wie zum Beispiel Ruminococcus gnavus, Ruminococcus torques und Bacteroides dorei, vermehrt festgestellt. Andere kamen hingegen seltener vor als bei Personen ohne Infektion, darunter Bifidobacterium adolescentis und Eubacterium rectale.
Dieses geringere Vorkommen wurde nach Berücksichtigung des Alters und der Einnahme von Antibiotika mit schweren Verläufen assoziiert. Insgesamt korrelierte die auf diese Zusammensetzung veränderte Flora mit den Entzündungswerten der Patienten.
Die Studie liefert jedoch bislang nur erste Anhaltpunkte und eignet sich noch nicht für eine pauschale Schlussfolgerung. Nicht ausgeschlossen werden kann, dass die Veränderungen auch mit vorliegenden Vorerkrankungen wie Diabetes und Übergewicht sowie mit früherer Einnahme von Antibiotika zusammenhängen können.
Yun Kit Yeoh et al. "Gut microbiota composition reflects disease severity and dysfunctional immune responses in patients with COVID-19" DOI: https://gut.bmj.com/content/early/2021/01/04/gutjnl-2020-323020 published 11 Jan 2021 in Gut microbiota
+++
Studie erklärt Limitierungen von Remdesivir
Forscher des Max-Planck-Instituts (MPI) für biophysikalische Chemie in Göttingen und der Universität Würzburg haben nun aufgeklärt, wie Remdesivir die virale Polymerase beim Kopieren stört und warum es sie nicht vollständig hemmt. Ihre Ergebnisse erklären, warum das Medikament eine eher schwache Wirkung hat. Zu Beginn der Pandemie hatte das Team aufgeklärt, wie das Coronavirus sein RNA-Genom dupliziert. Für den Erreger ist dies eine kolossale Aufgabe, da sein Genom rund 30.000 RNA-Bausteine umfasst, was es besonders lang macht.
Remdesivirs Struktur ähnelt der von RNA-Bausteinen, weshalb die Polymerase irregeführt wird und die Substanz in die wachsende RNA-Kette integriert. Die Forschenden untersuchten darum die Polymerase-RNA-Komplexe mit biochemischen Methoden und Kryo-Elektronenmikroskopie. Sie entdeckten, dass der Kopiervorgang genau dann unterbrochen wird, wenn drei weitere Bausteine hinzugefügt wurden, nachdem Remdesivir in die RNA-Kette eingebaut wurde. Die Polymerase erlaubt anschließend nicht die Installation einer vierten. Diese Pause wird durch nur zwei Atome in der Struktur von Remdesivir verursacht.
Das Problem: Remdesivir blockiert die RNA-Produktion nicht vollständig. Oft setzt die Polymerase ihre Arbeit fort, nachdem der Fehler behoben wurde, erklären die Autoren. Das Verständnis der Wirkungsweise von Remdesivir eröffne jedoch neue Möglichkeiten bei der Entwicklung neuer Therapeutika gegen COVID-19.
Goran Kokic et al. "Mechanism of SARS-CoV-2 polymerase inhibition by remdesivir". Nature Communications 12, 279 (2021), doi: 10.1038/s41467-020-20542-0
13. Januar 2021
------------------------------------------
Eine Studie in Brasilien untersuchte die Reinfektion zwei Mitarbeiterinnen aus dem Gesundheitswesen im Norden des Landes, die sich binnen weniger Monate erneut mit einer Mutante von SARS-CoV-2 ansteckten.
Bislang versetzten die Meldungen von Mehrfach-Infektionen die Wissenschaft nicht in Sorge. Im Fall der beiden Frauen aus Brasilien ist indes bemerkenswert, dass die neuen Infektionen durch eine andere Virusvariante verursacht wurden. Die festgestellte Genveränderung trägt die Bezeichnung E484K und wird auch in der deutlich ansteckenderen Virusmutation aus Südafrika vermutet.
Erste Laboruntersuchungen dazu zeigen, dass gebildete Antikörper gegen die Mutation schwächer wirken, da sie sich schwächer an das Virus binden. So kann auch eine Reinfektion einfacher erfolgen und auch die Frage nach der Wirksamkeit der Impfstoffe gegen die neuen Virusmutationen gibt Anlass zur weiteren Prüfung.
Die Fälle: Im Abstand von vier Monaten wurde eine der beiden Frauen zwei Mal positiv auf das Virus getestet. "Die Sequenzierung des gesamten Genoms ergab, dass die beiden Infektionen durch die brasilianischen Sars-CoV-2-Linien B.1.1.33 und B.1.1.28 verursacht wurden", heißt es in der bislang von ungeprüften Studie aus dem Labor für Atemwegsviren und Masern in Rio de Janeiro. Die zweite Frau infizierte sich innerhalb von fünf Monaten zwei Mal - zunächst mit derselben Viruslinie, dann mit der Variante B.1.1.248, die nah mit der Variante B.1.1.28-Linie verwandt ist.
Diese Fälle der Reinfektion durch Virusmutationen von SARS-CoV-2 sind den Forschern zufolge zu einen entmutigend, zum anderen aber als Einzelfälle noch nicht für endgültige Schlussfolgerungen geeignet. Dennoch bleibe die Frage, wie lange die schützende Immunantwort nach einer überstandenen Infektion oder der Impfung Bestand hat.
Resende, P. C. et al. "Spike E484K mutation in the first SARS-CoV-2 reinfection case confirmed in Brazil, 2020" published on 11 Jan 2021 as Pre Print on virological.org
8. Januar 2021
------------------------------------------
Wichtige Erkenntnisse zum Immungedächtnis für SARS-CoV-2: Bis zu acht Monate stabil
Das Verständnis des Immungedächtnisses gegen SARS-CoV-2 ist entscheidend für die Verbesserung von Diagnostika und Impfstoffen sowie für die Prognose des Pandemieverlaufs. Eine US-Studie zum Thema macht Mut.
Die Forschenden analysierten mehrere Kompartimente des zirkulierenden Immungedächtnisses zu SARS-CoV-2 in 254 Proben aus 188 COVID-19-Fällen, einschließlich 43 Proben ≥ 6 Monate nach der Infektion. Ergebnis: Antikörper zum Spike-Protein waren über mehr als sechs Monate relativ stabil. Spike-spezifische Gedächtnis-B-Zellen waren ein halbes Jahr nach dem Auftreten der ersten Symptome sogar häufiger als fünf Monate zuvor. Die SARS-CoV-2-spezifischen CD4 + T-Zellen und CD8 + T-Zellen nahmen hingegen etwa mit einer Halbwertszeit von drei bis fünf Monaten ab.
Einschränkend sei laut der Studienautoren festzuhalten, dass jede Komponente des Immungedächtnisses eine unterschiedliche Kinetik aufweist und in der vorliegenden Studie nur das zirkulierende Immungedächtnis bewertet wurde. Die Bedeutung des lokalen Immungedächtnisses nach einer Primärinfektion mit SARS-CoV-2 sei noch offen. Außerdem sei die Heterogenität der Immunantworten auf SARS-CoV-2 zwischen Individuen ein zentrales Merkmal aller bisherigen Untersuchungen zum Thema. Aus dieser Heterogenität leitet sich nach Ansicht der Autorinnen und Autoren ab, dass weitere Langzeitlängsstudien mit engmaschigen Probenentnahmen erforderlich sind, um die Antikörperkinetik gegen SARS-CoV-2 genauer zu definieren.
Die bisher vorliegenden Daten legten jedoch nahe, dass das T-Zell-Gedächtnis über die ersten acht Monate nach einer SARS-CoV-2-Infektion hinaus ein stabileres Plateau oder eine langsamere Zerfallsphase erreichen könnte. Ein Befund, der allerdings keine direkten Schlussfolgerungen über eine schützende Immunität erlaube.
Jennifer M. Dan et al. "Immunological memory to SARS-CoV-2 assessed for up to 8 months after infection", published in Science 6 Jan 2021, DOI: 10.1126/science.abf4063
Olfaktorischen Dysfunktion tritt vor allem bei leichten COVID-Verläufen auf
Eine neue Studie aus Belgien, Frankreich und Spanien widmet sich der Prävalenz und Rekonvaleszenz von Olfaktorischer Dysfunktion (OD) bei COVID-Patienten. Dazu wurde ein zwischen dem 22. März und 3. Juni 2020 erhobener Datensatz von 2.581 Patienten aus 18 europäischen Krankenhäusern ausgewertet und diese befragt. Von den 1.916 Patienten mit OD nahmen 1.363 bis zum Ende an der Erhebung teil (71,1 Prozent).
Ergebnis: Die Prävalenz von OD war bei milden Verläufen von COVID-19 (85,9 Prozent) signifikant höher als bei moderaten bis kritischen Verläufen (4,5-6,9 Prozent; P = 0,001). Insgesamt 328 Patienten (24,1 Prozent) erholten sich - ihrer subjektiven Bewertung nach - auch bis 60 Tage nach Beginn der Dysfunktion nicht. Die mittlere Dauer der selbst berichteten OD betrug 21,6 ± 17,9 Tage.
Objektive olfaktorische Bewertungen ergaben Hyposmie / Anosmie in 54,7 Prozent bzw. 36,6 Prozent von leichter bis kritischer Form (P = 0,001). Innerhalb von 60 Tagen erholten sich 84,7 Prozent der objektiv anosmischen / hyposmischen Patienten vollständig. Nach sechs Monaten lag dieser Wert bei 95,3 Prozent.
J. R. Lechien et al. "Prevalence and 6‐month recovery of olfactory dysfunction: a multicentre study of 1363 COVID‐19 patients", Published in Journal of Internal Medicine, 05 January 2021, https://doi.org/10.1111/joim.13209
6. Januar 2021
------------------------------------------
Während die Schließung von Lehrstätten wie Schulen und Universitäten die Ansteckung um bis zu 40 Prozent reduzieren konnte, sind Ausgangsperren offenbar wenig effektiv.
Angesichts der aufgeheizten Diskussion um die Verlängerung und Verschärfungen der Pandemie-Maßnahmen, bringen wissenschaftliche Daten vielleicht Klarheit: An der britischen Oxford-Universität haben Forscher per Datenanalyse zum Infektionsgeschehen in 41 vorrangig europäischen Ländern errechnet, welche Maßnahmen wie wirkungsvoll sind.
Dafür verglichen sie Daten vom 20. Januar bis zum 30. Mai 2020 zu registrierten Infektionen und Sterbefällen und stellten diese in Zusammenhang mit den in dem Zeitraum geltenden Regelungen.
Ergebnisse: Die Schließungen von Schulen und Universitäten sowie die Kontaktbeschränkungen im privaten Bereich zeigten den Errechnungen nach die deutlichste Wirkung auf die Virusausbreitung.
Dagegen hatte die Schließung von Gastronomie und Geschäften nur einen mittelstarken Einfluss. Ausgangsperren waren sogar nur in einem so geringen Umfang effektiv, so dass diese Restriktion nicht zwangsläufig nötig gewesen wäre, schreiben die Studienautoren.
Als ersten Schritte wurde anhand der Meldezahlen der Infektionen und Todesfälle der tatsächliche Pandemieverlauf in dem Zeitraum der ersten Welle errechnet. Die sich daraus ergebene reale Reproduktionszahl wurde im Anschluss zur Errechnung der realen Effektivität der Maßnahmen verwendet. Da diese in den Ländern unterschiedlich ausfielen, konnten die Forschern die Wirksamkeit vergleichen und Rückschlüsse anstellen.
Schulschließungen haben demnach die Reproduktionszahl um bis zu 40 Prozent reduziert. Die Ausgangssperren hingegen zeigten nur einen 10-prozentigen Minderungseffekt. Auch wenn die Aussagen der Studie eher allgemein ausfallen, sei doch ein klarer Trend zu erkennen, resümieren die Autoren.
Brauner, J. M. et al. "Inferring the effectiveness of government interventions against COVID-19" published in Science 15 Dec 2020 DOI: 10.1126/science.abd9338
5. Januar 2021
------------------------------------------
Eine experimentelle Studie belegt, dass hohe Blutdruckwerte durch SARS-CoV-2 verursachte Entzündungen begünstigen. Allerdings kann diese Gefahr mit ACE-Hemmern signifikant gesenkt werden.
Hypertonie gehört zu den häufigsten Risikofaktoren für einen ernsten Krankheitsverlauf bei COVID-19. Bleibt er unentdeckt oder unbehandelt, steigt die Gefahr, nach der Virusinfektion schwer zu erkranken.
Wissenschaftler um die Berliner Professorin Irina Lehmann von der Berliner Charité haben im Rahmen einer kleinen Studie dazu weitere Daten ermittelt und heben darin auch auf den Einsatznutzen von ACE-Hemmern ab: Eine medikamentöse Bluthochdrucktherapie kann das Risiko von schwer entzündlichen Verläufen demnach senken. Das gilt jedoch nicht für Sartane als Therapeutika. In Deutschland hat ein Drittel der Erwachsenen erhöhte Blutdruckwerte. Ab einem Lebensalter von 60 Jahren weist sogar jeder zweite Bluthochdruck auf - dieser ergibt zusammen mit steigendem Alter einen prägnanten Risikofaktor für COVID-19. Aber wie die Studie belegt, stellt sich Bluthochdruck unbehandelt auch als alleiniger Risikofaktor dar.
Für die Studie wurden Daten von Patienten und ihren Nasopharyngeal-Abstrichen ausgewertet. Bei Erkrankten mit einer arteriellen Hypertonie wiesen die Immunzellen eine stärkere Entzündungsreaktion auf als bei Patienten ohne erhöhte Blutdruckwerte. Die Infektionen dauerten im Durchschnitt länger bis sie ausgeheilt waren und zeigten häufiger eine Anfälligkeit für schwere Atemwegsinfektionen. Weiter zeigt die Studie, dass verabreichte ACE-Hemmer das Risiko des schweren Verlaufs nahezu auf das Niveau eines Patienten mit normalen Bluthochdruckwerten senken. Diese Erkenntnis verdeutlicht laut der Autoren, wie wichtig es ist, eine Hypertonie in der Pandemie zu erkennen und zu behandeln.
Die Ergebnisse werden derzeit in Fachkreisen diskutiert. Die Studie ist von der Teilnehmerzahl nicht umfangreich genug, um verschiedene Blutdrucksenker miteinander zu vergleichen. Bis dahin gelten weiterhin die Empfehlungen der Deutschen Hochdruckliga, eine bestehende Medikamentation während der COVID-Erkrankung nicht zu verändern.Lukassen, S. et al. "Hypertension delays viral clearance and exacerbates airway hyperinflammation in patients with COVID-19." published in Nature Biotechnology on 24 Dec 2020. DOI: https://doi.org/10.1038/s41587-020-00796-1
4. Januar 2021
------------------------------------------
Sehr viel ansteckender, aber nicht tödlicher - eine Studie hat anhand von Patientendaten die Virusmutation B.1.1.7 mit alten Varianten verglichen und bestätigt damit wissenschaftliche Annahmen.
Nach den aktuellen Untersuchungen der britischen Gesundheitsbehörde Public Health England verursacht die neue Virusmutation keinen schwereren Verlauf, wie zunächst von verschiedenen Gesundheitsexperten befürchtet. Dafür zeigt sich die Befallsrate, die sogenannte Secondary Attack Rate, höher als bei bekannten Varianten. Kontaktpersonen können durch die neue Mutation einfacher angesteckt werden.
Für die Erkenntnisse werteten die Forscher Daten von 1.769 Infizierten mit der Mutation und die von 1.769 Infizierten mit den bekannten SARS-CoV-2-Erregern aus. Berücksichtigt wurden beim Vergleich Angaben zum Alter, Geschlecht, dem Wohnort der Infizierten und der Testzeitpunkt. Von den insgesamt 3.538 infizierten Personen wurden 42 im Krankenhaus behandelt, davon waren 16 an der neuen Mutation erkrankt. Zwölf Personen verstarben an dieser neuen Variante. In der Kontrollgruppe hingegen zehn.
Die Studie ist noch nicht abgeschlossen, ihre Erkenntnisse werden derzeit diskutiert. Sie bestätigen bereits gewonnene Zwischenerkenntnisse einer Untersuchung aus Birmingham, die feststellte, dass symptomatische Infizierte mit der B.1.1.7-Variante bis zu 35 Prozent mehr Viruslast in ihren Proben aufweisen als asymptomatische. Bei den herkömmlichen Varianten waren es hingegen nur zehn Prozent. Vorläufig halten die Autoren fest, dass die Studie keinen statistisch signifikanten Unterschied in der Hospitalisierung und der 28-Tage-Todesrate in Zusammenhang mit der Mutation zeigt.
Die neue Mutation wurde in Deutschland bereits im November festgestellt. Zuvor hatte man sie auch in Chilie und dem US-Bundesstaat Colorado nachgewiesen.
Chand, M. et al in "Investigation of novel SARS-CoV-2 variantVariant of Concern 202012/01" Public Health England on Dec 28, 2020
18. Dezember 2020
------------------------------------------
Am 9. März 2020 entwickelten die 60-jährigen männliche Zwillinge Symptome, die mit Fieber und Nasenverstopfung begannen, sich mit Müdigkeit, Dyspnoe und trockenem Husten fortsetzten und nach 10 Tagen zu einer Hospitalisierung führten.
Nasopharyngeale Abstriche mit einem Reverse-Transkriptase-Polymerase-Kettenreaktionstest in Echtzeit waren positiv. Keiner der Zwillinge hatte eine Vorgeschichte mit chronischen Krankheiten, kardiovaskulären Risikofaktoren oder Langzeittherapie. Sie lebten im selben Haus und arbeiteten am selben Ort in einer Karosseriewerkstatt, wo sie Autos reparierten. Die Kontaktverfolgung identifizierte einen ihrer Kunden, der ohne Schutzmaßnahmen eng mit ihnen interagierte, als wahrscheinliche Quelle ihrer Infektionen.
Die Zwillinge hatten beide eine leichte interstitielle Pneumonie. Dasselbe medizinische Team versorgte beide Zwillinge während der ersten zwei Wochen ihres Krankenhausaufenthalts, wo sie mit zusätzlichem Sauerstoff, Paracetamol, Hydroxychloroquin, Darunavir/Cobicistat und Enoxaparin in prophylaktischer Dosierung behandelt wurden.
Dennoch hatten die Zwillinge unterschiedliche klinische Verläufe. Zwilling 1 wurde ohne Komplikationen entlassen und erholte sich ohne Probleme. Im Unterschied dazu hatte Zwilling 2 einen progressiven Anstieg der Leukozytenzahl und des C-reaktiven Proteinspiegels, der mit einem variablen Anstieg der Körpertemperatur einherging. Außerdem war eine nicht-invasive Beatmung aufgrund einer Abnahme des Pao2/FIo2-Verhältnisses erforderlich.
Nach 3 Tagen ineffektiver Beatmung wurde er auf die Intensivstation verlegt, wo er intubiert und mechanisch beatmet wurde. Er entwickelte einen septischen Schock aufgrund einer anaeroben bakteriellen Infektion, die Vasopressoren, Antibiotika, Steroide und eine 4-tägige invasive Beatmung erforderte. Auf den Aufenthalt auf der Intensivstation folgten 17 Tage unkomplizierter Krankenhausaufenthalt und eine langsame Erholung, die jedoch mit einer vollständigen Wiederherstellung des Gasaustauschs ohne langfristige Folgen endete.
Einen Grund für den unterschiedlichen Verlauf konnten die Forscher nicht ermitteln. Außer dass der schwer erkrankte Zwilling nicht verheiratet war, waren die Patienteneigenschaften identisch. Die Autoren vermuten, dass die Unterschiede im Virus (Unterschiede in der Infektionsdosis oder Viren mit unterschiedlichen Mutationen) die Unterschiede in der Krankheitsschwere erklären.
Davide Lazzeroni, Simultaneous COVID-19 in Homozygous Twins, published at Annals.org on 8 December 2020, https://doi.org/10.7326/L20-1207
14. Dezember 2020
------------------------------------------
Masken in der Öffentlichkeit reduzieren Virusausbreitung um 50 Prozent
Jena war während der ersten Pandemie-Welle die erste Stadt in Deutschland, die eine Maskenpflicht für den öffentlichen Raum anordnete. Mit Erfolg: Nachdem am 6. April auf öffentlichen Plätzen, in Geschäften und im Nahverkehr ein Mund-Nasen-Schutz getragen werden musste, verringerte sich das Infektionsgeschehen in den folgenden 20 Tage um 75 Prozent. Bei der Altersgruppe 60 Plus betrug der Rückgang sogar 90 Prozent.
Das Beispiel von Jena diente den Wissenschaftlern der Universität Mainz als Ausgangspunkt für einen bundesweiten Vergleich, um den allgemeinen Effekt einer Maskenpflicht zu untersuchen. Für die Studie verglichen sie die Ansteckungszahlen in den Städten Cloppenburg, Trier, Darmstadt und Rostock vor und drei Wochen nach Einführung der Schutzmaßnahme. Diese Städte sind in ihrer Bevölkerungszahl und -dichte, dem durchschnittlichen Alter der Einwohner, dem Seniorenanteil, dem Infektionsgeschehen sowie dem Angebot von Ärzten und Apotheken mit Jena vergleichbar.
Im Ergebnis war der Eindämmungseffekt nicht so signifikant ausgeprägt wie in Jena, aber eindeutig: Die Ausbreitung des Virus konnte um knapp 50 Prozent reduziert werden, nachdem die Menschen zum Tragen einer Maske im öffentlichen Raum angehalten wurden. Die Neuinfektionen sanken den Studienautoren zufolge von 100 auf 55. Umgekehrt heißt das: Ohne Masken gäbe es 38.000 anstatt 20.000 Neuinfektionen pro Tag in Deutschland.
Dieses Ergebnis stehe mit der Einschätzung von Epidemiologen und Virologen in Einklang, dass ein Mund-Nasen-Schutz den Luftstrom beim Sprechen hemmt und dadurch die Übertragung infektiöser Partikel eingedämmt wird. Die Masken könnten auch eine Art Signalfunktion für die Bevölkerung haben, sich an die Kontaktbeschränkungen zu halten. "Unsere Ergebnisse legen nahe, dass eine Maskenpflicht ein Baustein auch für die weitere Eindämmung von Covid-19 ist", sagt Prof. Dr. Klaus Wälde, Volkswirt an der Johannes Gutenberg-Universität Mainz.
Mitze, T. et al: "Face masks considerably reduce COVID-19 cases in Germany" published 3 Dec, 2020 in PNAS https://doi.org/10.1073/pnas.2015954117
9. Dezember 2020
------------------------------------------
So hoch ist das Komplikationsrisiko bei COVID-19
Wissenschaftler aus Buffalo im US-Bundesstaat New York haben auf der Basis von 70.288 COVID-19-Patientendaten das Risiko für die häufigsten Komplikationen errechnet. Demnach entwickelt 28 Patienten eine virale Lungenentzündung, 23 leiden an akutem Lungen- und zwölf an akutem Nierenversagen und zehn an einer Sepsis.
Diese Krankheitserscheinungen haben eine starke Assoziation mit COVID-19 und weisen ein hohes absolutes Risiko auf. Weniger risikoreich und dennoch assoziiert sind Begleiterscheinungen wie Luftansammlungen im Brustkorb (Pneumothorax) mit einem absoluten Risiko von 0,4 Prozent, eine Herzmuskelentzündung (0,1 Prozent) und Gefäßgerinnungen (disseminierte intravasale Koagulopathie) mit 0,1 Prozent von 100 COVID-19-Patienten. Etwa fünf Prozent der Patienten wurde auf der Intensivstation behandelt, gut die Hälfte stationär. Die Patienten waren im Mittel 65 Jahre alt. Die Daten wurden im Zeitraum zwischen dem 1. März und dem 30. April 2020 erhoben.
Murk, W. et al. "Diagnosis-wide analysis of COVID-19 complications: an exposure-crossover study" Dec. 07 2020 in CMAJ DOI: https://www.cmaj.ca/content/early/2020/12/07/cmaj.201686
7. Dezember 2020
------------------------------------------
Eine Studie hat herausgefunden, dass gut zehn Prozent der 987 untersuchten COVID-Patienten mit einer lebensbedrohlichen Pneumonie Antikörper gegen die zentralen Proteine des eigenen Immunsystems entwickelten - Interferone. Diese Proteine weisen eine immunstimulierende, antivirale Wirkung auf.
Die Wissenschaftler halten einen angeborenen B-Zell-Immundefekt, der bei einer Zytokin-Immunität existiert, für eine Ursache von schweren Verläufen. Hier werden neutralisierende Autoantikörper aktiv. Bei den Patienten beeinträchtigt die adaptive Autoimmunität die angeborene, intrinsische antivirale Immunität. Wie die Studie zeigt, waren unter den untersuchten Patienten 94 Prozent männlich. Das könnte eine Erklärung sein, warum mehr männliche Patienten schwer erkranken.
In einer zweiten Studie konnten die Forscher feststellen, dass weitere 3,5 Prozent der kritisch Erkranken Mutationen an ihren Genen aufweisen, die die Interferone an der Virenbekämpfung hindern. Es wird angenommen, dass die Autoantikörper bereits vor der Pandemie gebildet worden waren, bis dahin aber nicht getriggert wurden. Warum das den jetzt Betroffenen keine Probleme verursachte, ist noch nicht geklärt. Die Forscher vermuten, dass das Coronavirus selbst die Interferone unterdrückt.
Bastard, p. et al: "Autoantibodies against type I IFNs in patients with life-threatening COVID-19" published on 23 Oct. 2020 in Science DOI: 10.1126/science.abd4585
4. Dezember 2020
------------------------------------------
COVID-19 verursacht auch im Darm Entzündungen und verändert dadurch die Bakterienwelt
Eine Infektion mit SARS-CoV-2 kann eine Vielzahl von Organen befallen, so auch den Verdauungstrakt. Erbrechen, Übelkeit und vor allem Durchfall sind inzwischen festgestellte Symptome. Sie treten vorrangig in der frühen Phase der Infektion auf. Patienten reagieren hier mit Entzündungen, die das Virus auslöst. Durch den Befall wird auch das Mikrobiom stark verändert, berichtet Herbert Tilg, Direktor der Universitätsklink für Innere Medizin Innsbruck. Untersuchungen haben hier gezeigt, dass bei rund 50 Prozent der Betroffenen die Leberwerte krankhaft erhöht sind. Auch hier kommt es zu entzündlichen Prozessen.
COVID-19 verursacht demnach nicht nur eine Entzündung in der Lunge, sondern wahrscheinlich auch im Dünn- und Dickdarm.
"Wir haben gelernt, dass diese Erkrankung ein sehr breites klinisches Bild zeigt", erklärt Tilg. "Das heißt, es können verschiedene Organe beteiligt sein. Es gibt keine andere Virusinfektion, die in einem so großem Ausmaß Entzündungen im Körper verursacht. COVID-19 ist also eine entzündliche Erkrankung, die den Organismus "überfährt".Im Stuhl der Patienten lässt sich das Entzündungseiweiß Calprotectin nachweisen, das auf eine Entzündung im Dick- und Dünndarm hinweist und die Mikrobiota, vermutlich abhängig vom Schweregrad der Erkrankung, stark beeinflusst. Das wiederum kann die weitere Ausbreitung im Organismus begünstigen und einen "nachhaltigen Effekt auf das Krankheitsbild haben", so Tilg. Seine Schlussfolgerung: Das Mikrobiom muss bei der Therapie mitberücksichtig werden.
2. Dezember 2020
------------------------------------------
COVID-19: Kontakt mit Erkältungsviren bietet offenbar keinen Schutz
Viele Menschen hatten bereits vor dem Auftreten des neuartigen Coronavirus Kontakt zu anderen Coronaviren, etwa als Auslöser von Erkältungskrankheiten. Eine Hypothese war daher, dass diese früheren Kontakte zu einem besseren Immunschutz auch vor einer SARS-CoV-2-Infektion beitragen könnten. Forscher vom Institut für Immunologie der Christian-Albrechts-Universität zu Kiel (CAU) und dem Universitätsklinikum Schleswig-Holstein (UKSH) gingen dieser Frage jetzt noch einmal nach.
Sie konnten zeigen, dass Menschen, die noch keine Infektion mit SARS-CoV-2 durchgemacht haben, tatsächlich bestimmte Immunzellen, sogenannte T-Gedächtniszellen aufweisen, die auch SARS-CoV-2 als Fremdkörper erkennen können. Allerdings sind diese "prä-existierenden" T-Gedächtniszellen offenbar nicht besonders gut in der Lage, eine SARS-CoV-2-Infektion zu erkennen und für deren Bekämpfung zu sorgen, da sie das Virus nur schwach binden. Stattdessen könnten diese Gedächtniszellen sogar eher zu einem schweren Krankheitsverlauf beitragen.
Trifft das Immunsystem auf einen bis dahin unbekannten Erreger, werden sogenannte naive T-Zellen aktiviert, die eine Immunreaktion bilden, die nach einer Lernphase die Immunreaktion gegen den neuen Erreger vorantreiben. Dieses "Wissen" über den konkreten Krankheitserreger wird nach der akuten Immunreaktion in Form von T-Gedächtniszellen im Körper gespeichert. Kommt das Immunsystem dann wieder mit dem gleichen Erreger in Kontakt, werden diese Gedächtniszellen aktiviert und können schneller und wirkungsvoller den Erreger bekämpfen als naive Zellen. Auch auf ähnliche Erreger, zum Beispiel verschiedene Stämme von Coronaviren, können diese Gedächtniszellen in einer Kreuzreaktion reagieren und auch diese schneller bekämpfen.
Für die Untersuchung wurde das Blut von Probanden, die bisher keinen Kontakt zu SARS-CoV-2 hatten, auf Immunzellen analysiert. Viele wiesen tatsächlich T-Gedächtniszellen auf, die das Virus erkennen können. "Allerdings haben jüngere Menschen, die häufiger an gewöhnlichen Erkältungen erkranken, entgegen der Erwartung keine größere Anzahl dieser Zellen. Außerdem reagiert nur ein kleiner Teil dieser Zellen auch mit den Corona-Erkältungsviren. Die Gedächtniszellen haben also offenbar wenig mit früheren Kontakten zu Corona-Erkältungsviren zu tun", erklärt Prof. Alexander Scheffold, Direktor des Instituts für Immunologie der CAU. Ihre Fähigkeit, das neue Coronavirus zu erkennen sei eher zufällig, da im Laufe des Lebens das Repertoire an Immunreaktionen mit T-Zellenbildung steigt. In der Wissenschaft nennt man das "immunologisches Alter", das mit dem biologischen Alter vergleichbar ist.
Doch obwohl diese Gedächtniszellen in jedem vorhanden sind, sind sie offensichtlich nicht an der Abwehr einer SARS-CoV-2-Infektion beteiligt. Das liegt vermutlich an ihrer Qualität: "Diese T-Gedächtniszellen erkennen zwar SARS-CoV-2-Viren, allerdings machen sie das nicht besonders gut. Dadurch sind sie wahrscheinlich nicht in der Lage, dafür zu sorgen, dass das Virus erfolgreich bekämpft wird", erläutert die Erstautorin Prof. Petra Bacher.Denn tatsächlich fand das Forschungsteam bei Patienten mit mildem Verlauf vor allem T-Zellen, die das Virus sehr gut erkennen. Bei schweren Verläufen zeigt sich das umgekehrt: Die T-Zellen erkannten das Virus schlecht, ebenso die T-Gedächtniszellen. "Das könnte darauf hindeuten, dass diese Immunzellen bei den schweren COVID-Fällen von den schlecht bindenden prä-existierenden T-Gedächtniszellen abstammen", führt Bacher aus.
Das könnte auch eine simple Erklärung dafür sein, warum ältere Menschen ein höheres Risiko für einen schweren Krankheitsverlauf haben. "Sie haben vielfach auch ein höheres immunologisches Alter und damit auch eine höhere Wahrscheinlichkeit, dass das Immunsystem auf diese "inkompetenten" prä-existierenden Gedächtniszellen zurückgreift", so Bacher.Bacher et al.: "Low avidity CD4+ T cell responses to SARS-CoV-2 in unexposed individuals and humans with severe COVID-19". Immunity (2020). DOI: 10.1016/j.immuni.2020.11.016
26. November 2020
------------------------------------------
Immungedächtnis könnte über Jahre vor schweren COVID-Verläufen schützen
Eine Studie hat das Immungedächtnis bis zu 240 Tage nach dem Auftreten der ersten COVID-Symptome untersucht. Erstaunlicherweise haben die Gedächtniszellen keine erkennbare Halbwertszeit.
Entscheidend Im Kampf gegen SARS-CoV-2 ist das Immungedächtnis zu verstehen. Eine US-Studie hat 185 Personen zwischen 19 und 81 Jahren mit COVID-19 rekrutiert. Die Probanden (43 Prozent Männer, 57 Prozent Frauen) repräsentierten eine Reihe von asymptomatischen, leichten, mittelschweren und schweren Verläufen. Die Mehrheit der hatte einen leichten Krankheitsverlauf, nur 8 Prozent mussten hospitalisiert werden.
Die meisten Probanden stellten 6 und 240 Tage nach Auftreten der Symptome eine Blutprobe zur Verfügung. 41 dieser Proben wurden mehr als sechs Monate nach dem Auftreten der Symptome entnommen. 38 Probanden stellten zu zwei bis vier Zeitpunkten über einen Zeitraum von mehreren Monaten Blutproben zur Verfügung.
Bei der Auswertung der Proben stellten die Forschenden fest, dass jede Komponente des SARS-CoV-2-Immungedächtnisses eine unterschiedliche Kinetik aufwies. Spike IgG war über mehr als sechs Monate relativ stabil, Spike-spezifische Gedächtnis-B-Zellen waren nach 6 Monaten sogar häufiger als nach einem Monat. SARS-CoV-2-spezifische CD4 + T-Zellen und CD8 + T-Zellen nahmen mit einer Halbwertszeit von 3-5 Monaten ab. Die Ergebnisse schwankten von Patient zu Patient jedoch sehr stark, im Einzelfach um das 200-Fache.
Bemerkenswert ist, so die Forschenden, dass in fast allen COVID-19-Fällen Gedächtnis-B-Zellen ohne erkennbare Halbwertszeit nachgewiesen wurden. Sie mutmaßen darum, dass das Immungedächtnis viele Patienten Jahre vor schweren COVID-Verläufen schützen könnten. Direkte Schlussfolgerungen über die schützende Immunität könnten hingegen nicht auf der Grundlage der Quantifizierung von zirkulierenden SARS-CoV-2-Antikörpern, Gedächtnis-B-Zellen, CD8 + T-Zellen und CD4 + T-Zellen gezogen werden.
Jennifer M. Dan et al., "Immunological memory to SARS-CoV-2 assessed for greater than six months after infection", bioRxiv 2020.11.15.383323; doi: https://doi.org/10.1101/2020.11.15.383323
25. November 2020
------------------------------------------
Hohe Blutzuckerwerte sind auch für Nicht-Diabetiker ein Risikofaktor
Hohe Blutzuckerwerte können auch unabhängig von einem vorliegenden Diabetes ein Risikofaktor für eine erhöhte Sterblichkeit bei COVID-19 sein. Das ergab die Auswertung von über 11.000 Patientendaten aus 109 spanischen Krankenhäusern, die den Blutzuckerwert ermittelt hatten.
Demnach starben 41 Prozent der eingelieferten Patienten mit einem Blutzuckerwert von über 180 mg/dl, obwohl hier kein langfristiger Diabetes bekannt war. Lag der Wert zwischen 140 und 180 mg/dl, betrug das Sterberisiko immer noch 33 Prozent. Zum Vergleich: Bei Patienten, deren Blutzuckerwert unter 140 Prozent lag, ergab sich nach der Datenauswertung ein 15,7 prozentiges Sterberisiko. Ebenso waren eine Einweisung auf die Intensivstation und eine künstliche Beatmung bei einer Hyperglykämie häufiger notwendig.
Diabetes gilt als einer der größten Risikofaktoren für eine schwere COVID-19-Erkrankung. Noch ist der Zusammenhang hier nicht vollständig geklärt. Es gibt Anhaltspunkte zu der Annahme, dass der Erreger das endokrine Pankreas infiziert und dort die Beta-Zellen schädigt, die ACE2-Rezeptoren enthalten, über die das Eindringen in die Zellen möglich wird. Bei Diabetikern ist eine Störung des Glukosestoffwechsels bereits vorhanden und die Bauchspeicheldrüse belastet. Auch können die heftigen Entzündungsreaktionen, die bei einer schweren COVID-Erkrankung entstehen, zu einer Insulinresistenz führen.
Carrasco-Sánchez, F. et al.: "Admission hyperglycaemia as a predictor of mortality in patients hospitalized with COVID-19 regardless of diabetes status: data from the Spanish SEMI-COVID-19 Registry" published 4 Nov. 2020 in Annals od Medicine DOI: https://doi.org/10.1080/07853890.2020.1836566
23. November 2020
------------------------------------------
Dänische Studie quantifiziert Schutzwirkung von OP-Masken
Der hauptsächliche Nutzen chirurgischer Masken in der Öffentlichkeit besteht im Schutz anderer. Diese Tatsache hebt eine Studie aus Dänemark hervor, deren Ergebnis bereits existierende Erkenntnisse bestätigt, dass das Tragen einer chirurgischen Maske dem Träger selbst keinen sicheren Schutz vor einer Infektion bietet.
Die Studie "Danmask-19" wurde von Mitte April bis Anfang Juni durchgeführt. Während dieser Zeit gab es Empfehlungen zur Handhygiene und dem Social Distancing. Der öffentliche Personennahverkehr und die Geschäfte blieben geöffnet, während Restaurants und Cafés bis Mitte Mai geschlossen waren. Besuche in Krankenhäusern und Pflegeheimen durften nur eingeschränkt stattfinden. Eine Maskenpflicht bestand jedoch noch nicht.
Insgesamt 6.024 Erwachsene wurden randomisiert in zwei Gruppen aufgeteilt, von der die eine Hälfte zum Tragen von chirurgischen Einweggesichtsmasken mit drei Schichten und einer Filtrationsrate von 98 Prozent gebeten wurde. Alle Teilnehmer hielten sich pro Untersuchungstag rund drei Stunden im Freien auf. Im Anschluss wurde per Rachenabstrich, Bluttest auf Antikörper oder klinischer Diagnose ermittelt, wie viele Teilnehmer sich infiziert hatten.
Die Rate lag dabei nicht weit auseinander: In der Gruppe der Maskenträger infizieren sich 42 Personen, während es in der Kontrollgruppe ohne Maskenschutz 53 Personen waren. Das ergab eine Infektionsrate von 1,8 Prozent zu 2,1 Prozent. Nach Auswertung weiterer Parameter ermittelten die Wissenschaftler ein um 18 Prozent geringeres Ansteckungsrisiko für die Maskenträger.
Die Untersuchung geht allerdings nicht auf das Ansteckungsrisiko für andere Personen ein und gibt keine klare Einschätzung für den Nutzen der Masken als Maßnahme zur Pandemie-Bekämpfung. Die verringerte Virusfreisetzung von infizierten Personen in die Umwelt könne der Mechanismus zur Abschwächung der Übertragung in Gemeinden sein, in denen die Verwendung von Masken häufig oder vorgeschrieben ist. Die Ergebnisse legten auch nahe, dass Personen andere COVID-19-Sicherheitsmaßnahmen unabhängig von der Verwendung von Masken nicht aufgeben sollten.
Henning Bundgaard et al, "Effectiveness of Adding a Mask Recommendation to Other Public Health Measures to Prevent SARS-CoV-2 Infection in Danish Mask Wearers", Annals of Iternal Medicine, 18 November 2020, https://doi.org/10.7326/M20-6817
Metastudie: Jeder dritte COVID-Intensivpatient stirbt
Eine systematische Analyse wertete 32 Studien zu den klinischen Verläufen von COVID-Intensivpatienten aus, die bis zum 15. August 2020 veröffentlicht waren. Preprints und Berichte wurden ebenfalls aufgenommen, wenn sie die Einschlusskriterien erfüllten. Die Kriterien waren prospektive, retrospektive oder registrierungsbasierte Volltextveröffentlichungen, in denen die Ergebnisse bei Patienten beschrieben wurden, die auf der Intensivstation für COVID-19 unter Verwendung eines validierten Tests aufgenommen wurden.
Die eingeschlossenen Artikel werteten insgesamt 69.093 Patientenfälle aus. Die meisten in die Studien einbezogenen Patienten waren männlich (59 Prozent), das mittlere Patientenalter betrug 56 Jahre (95% CI 48,5-59,8) Jahre, die mittlere Verweildauer auf der Intensivstation betrug 9,0 (95% CI 6,5-11,2) Tage. Mehr als die Hälfte der auf der Intensivstation aufgenommenen Patienten benötigte eine mechanische Beatmung (58 Prozent) für durchschnittlich 8,4 (95% CI 1,6-13,7) Tage. Unter ihnen war die Mortalität laut Metastudie sehr hoch (59 Prozent). Generell lag die Sterberate der COVID-19-Patienten auf der Intensivstation bei 32,3 Prozent. Die wichtigsten beschriebenen Interventionen waren die Verwendung von nicht-invasiver Beatmung, extrakorporaler Membranoxygenierung, Nierenersatztherapie und Vasopressoren.
Rodrigo B. Serafim et al., "Clinical course and outcomes of critically ill patients with COVID-19 infection: a systematic review", Clin Microbiol Infect. 2020 Oct 23, doi: 10.1016/j.cmi.2020.10.017
20. November 2020
------------------------------------------
Oxford-Coronavirus-Impfstoff erzeugt auch bei Älteren starke Immunantwort
Während der Phase-2-Studie wurde der Impfstoff an 560 gesunden Erwachsenen im Alter zwischen 18 und 55 Jahren, zwischen 56 und 69 Jahren und über 70 Jahren untersucht. Die Freiwilligen erhielten 2 Dosen des Impfstoffs ChAdOx1 nCoV-19 oder einen Placebo-MenACWY-Impfstoff. Dabei wurden keine schwerwiegenden Nebenwirkungen beobachtet. Diese Daten stimmen mit den Phase-I-Daten überein, die Anfang dieses Jahres für gesunde Erwachsene im Alter von 18 bis 55 Jahren gemeldet wurden.
"Ältere Erwachsene sind eine vorrangige Gruppe für die COVID-19-Impfung, da sie ein erhöhtes Risiko für schwere Krankheiten haben", erklärt Dr. Maheshi Ramasamy aus der Forschergruppe. "Wir wissen jedoch, dass sie tendenziell schlechtere Impfreaktionen haben."
Darum sei man erfreut zu sehen, dass der Impfstoff auch von älteren Erwachsenen gut vertragen wurde und ähnliche Immunantworten stimulierte wie bei jüngeren Freiwilligen. Der nächste Schritt ist nun die Untersuchung der Schutzwirkung. Die Phase-III-Studien mit dem Impfstoff ChAdOx1 nCov-2019 sind noch nicht abgeschlossen, so die Autoren. In den kommenden Wochen sollen jedoch frühzeitige Messungen der Wirksamkeit möglich sein.
Maheshi N. Ramasamy et al., "Safety and immunogenicity of ChAdOx1 nCoV-19 vaccine administered in a prime-boost regimen in young and old adults (COV002): a single-blind, randomised, controlled, phase 2/3 trial", The Lancet, November 18, 2020; DOI:https://doi.org/10.1016/S0140-6736(20)32466-1
19. November 2020
------------------------------------------
Schwangere mit COVID-19 haben erhöhtes Risiko für schwere Krankheitsverläufe
Die US-Zentren für Krankheitskontrolle und -prävention (CDC) haben ihre Risikoeinschätzung für schwangere Frauen angepasst: So wurden schwangere Frauen signifikant häufiger als nicht schwangere Frauen auf eine Intensivstation eingewiesen (1,05 Prozent gegenüber 0,39 Prozent). Auch die Zahl der invasiv Beatmeten unter den Schwangeren war deutlich höher als in der Vergleichsgruppe (0,29 gegenüber 0,11 Prozent). 34 Todesfälle (0,15 Prozent) wurden bei 23.434 symptomatischen schwangeren Frauen gemeldet gegenüber 447 (0,12 Prozent) bei 386.028 nicht schwangeren Frauen.
Um das Risiko für schwere Krankheiten und den Tod durch COVID-19 zu verringern, schlussfolgert die CDC, sollten Schwangere über die Wichtigkeit einer sofortigen medizinischen Versorgung nach Bekanntwerden der Infektion beraten werden. Schwangere und ihre Familien sollten außerdem bei allen Arztbesuchen gezielt über Maßnahmen zur Verhinderung einer SARS-CoV-2-Infektion informiert werden.
Laura D. Zambrano et al., "Update: Characteristics of Symptomatic Women of Reproductive Age with Laboratory-Confirmed SARS-CoV-2 Infection by Pregnancy Status - United States, January 22-October 3, 2020", https://www.cdc.gov/mmwr/volumes/69/wr/mm6944e3.htm?s_cid=mm6944e3_w
Remdesivir hilft im Laborexperiment bei Symptomen wie Übelkeit und Durchfall
Da bei etwa der Hälfte der COVID-19-Patienten die Symptome Übelkeit und Durchfall auftreten und diese auch mit schweren Krankheitsverläufen assoziiert werden (siehe Meldung vom 16. November 2020), versuchen Forscher zu verstehen, wie das neuartige Coronavirus den menschlichen Verdauungstrakt angreift. Ein Team an der Universität Ulm aus Gastroenterologen und Virologen hat dafür den molekularen Infektionsvorgang in einem Darm-Modell in eigens gezüchteten kleinen Dünndärmen aus embryonalen Stammzellen untersucht.
Professor Jan Münch vom Institut für Molekulare Virologie des Universitätsklinikums Ulm erklärt, wo das Virus im Darm andockt: "Eine Infektion mit SARS-CoV-2 ist nur möglich, wenn der Rezeptor ACE2, an den das Virus andocken kann, sowie die Protease TMPRSS2 im Gewebe vorhanden sind. In gesundem Darm haben wir diese Proteine durchgehend und besonders häufig im Zwölffingerdarm gefunden". Auch in den gezüchteten Därmen sind viele dieser Andockstellen verfügbar.
Eine Infektion führt zum Verlust spezialisierter Darmzellen, was letztlich zu Durchfall und Übelkeit führen kann. Die zentrale Frage der Forschungsarbeit ist daher, wie dieser Vorgang unterbunden werden kann. Tatsächlich zeigte Remdesivir eine gute Wirkung, denn es blockiert der Wirkstoff die RNA-Polymerase und somit die Vermehrung von SARS-CoV-2, berichten die Autoren.
Krüger, J. et al "Drug inhibition of SARSCoV-2 replication in human pluripotent stem cell-derived intestinal organoids, Cellular and Molecular Gastroenterology and Hepatology (2020), https://www.sciencedirect.com/science/article/pii/S2352345X2030182X3
16. November 2020
------------------------------------------
Einer von sechs Patienten hat ausschließlich Bauchbeschwerden
Forscher um Mitchell Wilson von der Universität Alberta, Kanada, haben 36 bestehende Studien analysiert, die sich mit den Symptomen von COVID-19-Patienten beschäftigt haben.
Hierbei wurden auch bildgebende Untersuchungen des Magen-Darm-Trakts der Betroffenen ausgewertet. Diese zeigten teilweise sichtbare Veränderungen der Organe in Form von Darmwandverdickungen, einen flüssigkeitsgefüllten Dickdarm, seltene Gasansammlungen in der Darmwand (Pneumatose) sowie eine Gasansammlung in der Bauchhöhle (Pneumoperitoneum), Darmeinstülpungen, Flüssigkeitsansammlungen in der Bauchhöhle (Aszites) und Entzündungen des Dick- und Dünndarms.
Insgesamt stellte sich heraus, dass die Magen-Darm-Symptome deutlich häufiger vorkommen als bislang angenommen. Demnach sollte bei Auftreten dieser Krankheitsanzeichen auch an eine mögliche Virusinfektion gedacht werden, raten die Forscher. Denn SARS-CoV-2 kann Zellen des Darms infizieren und somit sichtbare Veränderungen im Magen-Darm-Trakt hervorrufen.
Neben den Atemwegen - und in der Folge weit verbreiteten grippeähnlichen Symptomen der Viruserkrankung - können also auch weitere Organe befallen sein wie der Verdauungstrakt, der häufig betroffen ist. Zwar gab es bereits Meldungen über diese Komplikationen aus China zu Beginn der Pandemie, jedoch legt die Arbeit des Forscherteams nun erstmals offen, dass Bauchschmerzen, Übelkeit und Durchfall auch als alleinige Symptome der Erkrankung auftreten können. Rund 18 Prozent der Patienten litten an den Beschwerden, 16 Prozent gaben sogar an, ausschließlich die Symptome festzustellen.
Lui, K., Wilson, M.P. & Low, G. "Abdominal imaging findings in patients with SARS-CoV-2 infection: a scoping review." Abdom Radiol (2020). doi.org/10.1007/s00261-020-02739-5
5. November 2020
------------------------------------------
Auch bei älteren Menschen schränkt eine OP-Maske nicht den Sauerstoffgehalt ein
In Kanada haben Ärzte an der McMaster-Universität in Hamilton mit einer kleinen Studiengruppe von 25 Teilnehmern, die im Durchschnitt 76 Jahre alt waren und maximal eine chronische Erkrankung aufwiesen, untersucht, ob das Tragen einer OP-Maske ihre Versorgung mit ausreichend Sauerstoff einschränkt.
Entgegen der Argumentation von sogenannten Masken-Kritikern, die Mundschutze würden gerade älteren Menschen zu schaffen machen, konnten die Wissenschaftler belegen, dass dies nicht der Fall ist: In keiner Untersuchung der Senioren sank der Sauerstoffgehalt im Blut unter 92 Prozent. Das Masken-Tragen ist somit für den Alltag unbedenklich - unter Berücksichtigung (chronischer) Vorerkrankungen.
Für den Test erhielten die Bewohner eines Seniorenwohnheims den gleichen Masken-Typ und wurden mit einem Pulsoxymeter ausgestattet. Keiner von ihnen litt an einer Ruhedyspnoe, also einer Atemnot, die sich bereits in der Ruhephase manifestiert. Die Messungen wurden je eine Stunde vor, während und nach dem Tragen der Masken in Ruhe und bei alltagsüblichen Aktivitäten gemessen und dabei die periphere Sauerstoffsättigung (SpO2) ermittelt. Diese lag im Durchschnitt bei 96,1 Prozent vor dem Tragen der Maske, bei 96,5 Prozent während und bei 96,3 Prozent nach dem Tragen. Zu keiner Zeit sank der Wert unter 92 Prozent und damit in einen gesundheitsbedenklichen Bereich, der auf ein Sauerstoff-Defizit hindeutet.
Chan, N. C. et al.: "Peripheral Oxygen Saturation in Older Persons Wearing Nonmedical Face Masks in Community Settings" published in JAMA on Oct. 30, 2020 doi:10.1001/jama.2020.21905
++++++++++
Covid-19-Super-Spreading-Ereignisse spielen eine übergroße Rolle bei der Übertragung
Eine mathematische Analyse von Wissenschaftlern der Priceton University und des Massachusetts Institute of Technology legt nahe, dass die Vermeidung großer Ansammlungen die COVID19-Infektionsraten signifikant senken könnte. Die Untersuchung von etwa 60 Superspreading-Ereignissen zeigt, dass Ereignisse, bei denen eine Person mehr als sechs andere Personen infiziert, viel häufiger auftreten als erwartet. Basierend auf ihren Erkenntnissen entwickelten die Forscher auch ein mathematisches Modell der COVID-19-Übertragung, mit dem sie belegen, dass die Begrenzung von Versammlungen auf zehn oder weniger Personen die Anzahl der Super-Spreading-Ereignisse signifikant reduzieren und die Gesamtzahl der Infektionen senken kann.Die Forscher definierten Superspreader als Personen, die das Virus an mehr als sechs andere Personen weitergaben. Unter Verwendung dieser Definition identifizierten sie 45 Superspreading-Ereignisse aus der aktuellen SARS-CoV-2-Pandemie und 15 zusätzliche Ereignisse aus dem SARS-CoV-Ausbruch 2003, die alle in Artikeln in wissenschaftlichen Fachzeitschriften dokumentiert sind. Während der meisten dieser Ereignisse waren zwischen 10 und 55 Menschen infiziert, aber an zwei von ihnen, beide aus dem Ausbruch von 2003, waren mehr als 100 Menschen beteiligt.Die Ergebnisse legen nahe, dass das Verhindern von Superspreading-Ereignissen einen signifikanten Einfluss auf die Gesamtübertragung von Covid-19 haben könnte, sagen die Forscher. "Es gibt uns einen Überblick darüber, wie wir die anhaltende Pandemie kontrollieren können, indem wir Strategien identifizieren, die auf Superspreader abzielen", lautet ihr Fazit. Eine Möglichkeit, bestehe darin, zu verhindern, dass jemand auf einer großen Versammlung mit über zehn Personen interagiert.
Felix Wong, James J. Collins, "Evidence that coronavirus superspreading is fat-tailed", Proceedings of the National Academy of Sciences Nov 2020, 202018490; DOI: 10.1073/pnas.2018490117
4. November 2020
------------------------------------------
COVID-19 kann zum Umbau der Organstruktur in der Lunge führen
Zu den charakteristischen Merkmalen der gefundenen Lungenverletzungen gehören Thrombosen im Lungenmakro- und Mikrogefäßsystems, die Persistenz von virusinfizierten Zellen, Lungenpneumozyten und Endothelzellen. Die dysmorphen Zellen zeigten dabei sehr oft Merkmale eines Syncytiums - es waren also mehrere große Zellen entstanden, die sich jeweils durch mehrere Zellkerne mit reichlich Zytoplasma auszeichneten. Ein besonderer und unerwarteter Befund bei allen untersuchten Patienten war schließlich das Vorhandensein atypischer Merkmale von Bronchialchondrozyten, die oft sehr groß und dysmorph waren.
Auffällig war auch, dass in der Kohorte der untersuchten Patienten den anderen Organen offensichtliche Anzeichen einer direkten Virusinfektion fehlten - häufig trotz massiver Veränderungen in der Lunge.
Rossana Bussani et al., "Persistence of viral RNA, pneumocyte syncytia and thrombosis are hallmarks of advanced COVID-19 pathology", published in Ebiomedicine by The Lancet, Nov. 3, 2020 https://doi.org/10.1016/j.ebiom.2020.103104
++++++++++
Hohes Ansteckungsrisiko bei Personen im selben Haushalt
Dass sich Personen, die im gleichen Haushalt leben, leicht mit SARS-CoV-2 infizieren können, erscheint logisch. Beim Zusammenleben in den gleichen Räumlichkeiten ist das Risiko hier mit dem Virus in Berührung zu kommen so hoch, wie kaum woanders. Wie genau das geschieht und wieviel Zeit bis zur Ansteckung verstreicht, haben US-Forscher analysiert.
Danach breitet sich das Virus schneller und weiter in den US-Haushalten aus als bisher berichtet wurde. Dies geht aus neuen Voruntersuchungen einer multizentrischen Studie hervor, die von Forschern des Vanderbilt University Medical Center geleitet und in einem wöchentlichen Bericht der Centers for Disease Control and Prevention (CDC) veröffentlicht wurde.
Dafür wurden zwischen April und September in Nashville, Tennessee, und Marshfield, Wisconsin, auch bei den Angehörigen Abstriche genommen, die mit einem nachweislich Infizierten zusammenlebten. Ergänzend führten die Teilnehmer Tagebuch zu möglichen Symptomen. In sieben Tagen fiel der Test bei 102 von insgesamt 192 Personen in infizierten Haushalten positiv aus, was eine sekundäre Infektionsrate von 53 Prozent ausmacht. Davon hatten jedoch nur 41 Personen Symptome am ersten Tag mit positivem Testergebnis. Im weiteren Studienverlauf waren 68 Personen symptomatisch. Deren Symptome traten wenige Tage nach denen von den Index-Patienten auf.
Die Studie ergab, dass mindestens 75 Prozent der sekundären Infektionen innerhalb von fünf Tagen nach dem Auftreten der Symptome bei der ersten Person im Haushalt auftraten. Ähnliche Studien in den USA, Europa und Asien kamen dagegen zu dem Ergebnis, dass sich maximal 30 Prozent der Haushaltsmitglieder ebenfalls infiziert hatten.
Fast 70 Prozent der Index-Patienten waren am Tag vor dem Krankheitsausbruch über vier Stunden mit den Haushaltsmitgliedern zusammen im selben Raum. Nach dem Krankheitsbeginn waren es noch 40 Prozent.
Die Studie konnte jedoch nicht die unterschiedlichen Wohnraum-Situationen und das Risikobewusstsein der Studienteilnehmer berücksichtigen. In den US-Haushalten stand für jede Person in etwa ein Schlafzimmer zur Verfügung.
Grundsätzlich kann das Infektionsrisiko abgesenkt werden, wenn getrennte Schlafzimmer und Badezimmer vorhanden sind, schreiben die Wissenschaftler in ihrer Auswertung. Die Selbstquarantäne sei sofort einzuleiten noch bevor das Testergebnisse vorliegt. Immer da, wo der Mindestabstand nicht eingehalten werden kann, sollten alle Mitglieder des Haushalts Masken tragen und sich von möglichen Risikopatienten fernhalten.
Grijalva, C. G., et al: "Transmission of SARS-COV-2 Infections in Households - Tennessee and Wisconsin, April-September 2020" published in Morbidity and Mortality Weekly Report (MMWR), Oct. 30, 2020. https://www.cdc.gov/mmwr/volumes/69/wr/mm6944e1.htm
3. November 2020
------------------------------------------
In Russland zugelassenes Aprotinin-Aerosol könnte schweren COVID-Verlauf verhindern
Eine weitere Arbeit eines internationalen Forscherteams aus Frankfurt am Main, Hannover und Kent (Großbritannien) bestätigte vorherige Beobachtungen, die auf einen vielversprechenden Einsatz eines bereits zugelassenen Präparats hinweisen: Aprotinin, das früher zur Behandlung von Blutungen eingesetzt wurde, die auf einer Hyperfibrinolyse beruhen. Aprotinin ist in Russland als Aerosol zur Influenza-Behandlung zugelassen. Eine Analyse zeigte, dass die SARS-CoV-2-Replikation mit einer Herunterregulierung von Proteaseinhibitoren der Wirtszellen verbunden ist. Daher könnte Aprotinin herunterregulierte Proteasen der Wirtszellen während späterer Virusreplikationszyklen kompensieren.
Nach Einschätzung der Forschenden könnte die lokale Behandlung der Atemwege mit Aprotinin-Aerosol eine besonders vielversprechende Strategie sein, um die Virusreplikation und Lungenverletzung frühzeitig zu unterdrücken und das Fortschreiten von COVID-19 zu einem schweren Verlauf verhindern.
Bojkova, D. et al, "Aprotinin Inhibits SARS-CoV-2 Replication". Cells 2020, 9, 2377. https://doi.org/10.3390/cells9112377
++++++++++
Antidepressivum als mögliches Therapeutikum gegen COVID-19
Am Institut für Medizinische Biochemie, Zentrum für Molekularbiologie der Entzündung (ZMBE) der Westfälischen Wilhelms-Universität Münster (WWU) befassen sich Wissenschaftler unter der Leitung von Prof. Ursula Rescher mit dem therapeutischen Potenzial von bereits klinisch zugelassenen Medikamenten, die an der Schnittstelle von Wirt und Erreger wirken. Das Team fand bei In vitro-Untersuchungen heraus, dass das Antidepressivum Fluoxetin und auch das Antimykotikum Itraconazol als Kombinationsbehandlungen mit Remdesivir sowohl die Aufnahme von SARS-CoV-2-Viren in die Zellkultur als auch ihre Weiterverbreitung hemmt (Produktion infektiöser SARS-CoV-2-Partikel > 90%), ohne dabei Zellen oder Gewebe zu beschädigen.
Das Ergebnis macht Hoffnung, da die medikamentöse Behandlung sich als gut verträglich erweist und sich eine starke Beeinträchtigung der viralen Replikation beobachten lässt. Die Kombination der Wirkstoffe zeigen laut den Forschern stärkere antivirale Aktivitäten gegen SARS-CoV-2 als die Remedesivir-Monotherapie.
In der Veröffentlichung schreiben sie daher: "Sowohl die Itraconazol-Remdesivir- als auch die Fluoxetin-Remdesivir-Kombinationen sind vielversprechende therapeutische Optionen zur Kontrolle der SARS-CoV-2-Infektion und der schweren Progression von COVID-19." Ziel der Untersuchung war, ein möglichst schnell anwendbares und kostengünstiges Präparat zur Therapie schwerer und mittel schwerer Verläufe zu finden.
Rescher, U. et al: "Drug synergy of combinatory treatment with remdesivir and the repurposed drugs fluoxetine and itraconazole effectively impairs SARS-CoV-2 infection in vitro" published Oct. 16, 2020 in bioRxiv https://www.biorxiv.org/content/10.1101/2020.10.16.342410v1
29. Oktober 2020
------------------------------------------
Sterberate von COVID-Patienten sinkt in England nach erster Welle
Eine Analyse von der Exeter University aus England legt dar, dass die Sterberate von schwer an COVID-19 erkrankten Patienten während der zweiten Pandemie-Phase im Juni gesunken ist. Die Erkenntnisse seien nicht nur darauf zurückzuführen, dass weniger ältere und multimorbide Menschen stationär behandelt werden. Die Wissenschaftler gehen auch davon aus, dass sich die die zunehmend bessere Behandlung auswirkt.
Verglichen wurden die Daten aus dem zentralen Melderegisters "COVID-19 Hospitalisation in England Surveillance System" (CHESS) von März und Juni, die die Angaben von fast 15.400 Patienten aus 108 englischen Kliniken umfassen. Dabei sank die 30-Tages-Sterblichkeit auf den "Intermediate Care"-Stationen von 26 auf sieben Prozent, auf den Intensivstationen von 41 auf 21 Prozent. Weiteres Ergebnis: Die hospitalisierten Patienten waren im Frühsommer im Durchschnitt jünger und hatten weniger Begleiterkrankungen.
Doch auch nach Berücksichtigung dieser Faktoren reduzierte sich die Sterblichkeit im "Intermediate Care"-Bereich um 12,7 Prozent auf den Intensivstationen um 8,9 Prozent.
Dennis, J. et al. "Improving Survival of Critical Care Patients With Coronavirus Disease 2019 in England. A National Cohort Study, March to June 2020" pubished October 26, 2020 in Critical Care Medicine doi: 10.1097/CCM.0000000000004747
++++++++++
Neutralisierende Antikörper gegen SARS-CoV-2-Infektionen bleiben über Monate bestehen
Fragen zur Robustheit, Funktionalität und Langlebigkeit der Antikörperantwort auf das SARS-CoV-2-Virus sind bislang wenig erforscht. US-Wissenschaftler konnten jetzt zeigen, dass die überwiegende Mehrheit der infizierten Personen mit leichtem bis mittelschwerem COVID-19 robuste IgG-Antikörperantworten gegen das virale Spike-Protein aufweist.
Dazu wurde ein Datensatz von 30.082 positiv getesteten Personen ausgewertet, die am Mount Sinai Health System in New York City untersucht wurden. Diese Antikörperantwort ist laut Studie über einen Zeitraum von ungefähr fünf Monaten relativ stabil und der Anti-Spike-Bindungstiter korreliert signifikant mit der Neutralisation von authentischem SARS-CoV-2.
Ania Wajnberg et al.; "Robust neutralizing antibodies to SARS-CoV-2 infection persist for months", Published Online 28 Oct 2020, DOI: 10.1126/science.abd7728
28. Oktober 2020
------------------------------------------
Luftverschmutzung ist Ko-Faktor bei COVID-19-Sterbefällen
Eine im wissenschaftlichen Fachmagazin Cardiovascular Research veröffentlichte Studie schätzt, dass etwa 15 Prozent der weltweiten Todesfälle durch COVID-19 auf Luftverschmutzung zurückzuführen ist. Den Autoren des Max-Planck-Instituts für Chemie, der Harvard T.H. Chan School of Public Health, des London Centre for Climate Change and Planetary Health, der Berliner Charité und der Universitätsmedizin Mainz zufolge liegt der Anteil der luftverschmutzungsbedingten COVID-19 Todesfälle in Europa bei 19 Prozent, in Nordamerika bei 17 Prozent und in Ostasien bei 27 Prozent. Erstautor Dr. Andrea Pozzer vom Mainzer Max-Planck-Institut für Chemie betont, dass der zurechenbare Anteil keinen direkten Zusammenhang zwischen Luftverschmutzung und COVID-19-Mortalität beweist, sondern einen indirekten Effekt, weswegen er und seine Kollegen auch relative Zahlen angeben: "Unsere Schätzungen zeigen die Bedeutung der Luftverschmutzung auf Komorbiditäten, also Gesundheitsfaktoren, die sich gegenseitig verschlimmern und so tödliche gesundheitliche Folgen der Virusinfektion auslösen können."
Ko-Autor Prof. Thomas Münzel aus Mainz ergänzt: "Wenn Menschen verunreinigte Luft einatmen, wandern die sehr kleinen Schadstoffpartikel, die PM2,5, von der Lunge in das Blut und die Blutgefäße und verursachen Entzündungen und schweren oxidativen Stress. Dies ist ein Ungleichgewicht zwischen freien Radikalen und Oxidantien im Körper, die normalerweise Zellschäden reparieren. Dadurch wird die Innenauskleidung der Arterien, das Endothel, geschädigt, was zu einer Verengung und Versteifung der Arterien führt. Das COVID-19-Virus gelangt auch über die Lunge in den Körper und verursacht ähnliche Schäden an den Blutgefäßen, so dass es heute als Endothelerkrankung gilt.Wenn sowohl die langfristige Belastung durch Luftverschmutzung als auch die Infektion mit dem COVID-19-Virus zusammentreffen, dann haben wir eine additive negative Auswirkung auf die Gesundheit, insbesondere auf das Herz und die Blutgefäße, was zu einer größeren Anfälligkeit und geringeren Widerstandsfähigkeit gegenüber COVID-19 führt. Wenn Sie bereits an einer Herzerkrankung leiden, dann verursachen Luftverschmutzung und eine Infektion mit dem Coronavirus Probleme, die zu Herzinfarkt, Herzinsuffizienz und Schlaganfall führen können."
Für die einzelnen Länder ergeben die Schätzungen der mit Luftverschmutzung in Zusammenhang stehenden COVID-19-Todefälle ein sehr unterschiedliches Bild: Vergleichsweise hoch ist der Anteil in der Tschechischen Republik mit 29 Prozent, in China mit 27 Prozent und in Deutschland mit 26 Prozent - niedriger ist der Anteil beispielsweise in Italien (15 Prozent) oder Brasilien (12 Prozent). Einstellig sind die Werte für Israel (6 Prozent), Australien (3 Prozent) und Neuseeland (1 Prozent).
Für ihre Auswertung verwendeten die Forscher Auswertungen einer US-amerikanischen Studie, die den Zusammenhang zwischen der COVID-19-Mortalität und der Belastung mit Feinstaub abgeschätzt hat. Die Ergebnisse wurden mit chinesischen Studien verglichen, die die Folgen der Feinstaubbelastung auf die SARS-CoV-1-Epidemie 2003 analysiert hatten und bestätigten, dass in Gebieten mit Luftverschmutzung das Risiko, an der Krankheit zu sterben im Vergleich zu Gebieten mit relativ sauberer Luft um mehr als 80 Prozent höher war.
Die Wissenschaftler schlussfolgern daraus, dass ein Zusammenhang zwischen COVID-19-Todesfällen und der langfristigen Exposition gegenüber PM2.5 sehr wahrscheinlich ist. Den regionalen Anteil der COVID-19-Todesfälle ermittelten die Wissenschaftler mithilfe von Daten der globalen Feinstaubverteilung, die sie aus Satellitendaten, bodengestützten Luftverschmutzung-Netzwerken und numerischen Modellen gewannen. Da die Ergebnisse auf epidemiologischen Daten der dritten Juniwoche 2020 basieren, planen die Wissenschaftler eine abschließende Bewertung der gesamten Daten nach dem Abklingen der COVID-19 Pandemie.
Andrea Pozzer et al., "Regional and global contributions of air pollution to risk of death from COVID-19", Cardiovascular Research, cvaa288, https://doi.org/10.1093/cvr/cvaa288
+++++++++
Menschen mit Trisomie 21 haben 25 mal so hohes Sterberisiko bei COVID-Erkrankung
Für Menschen mit Trisomie 21 (Down-Syndrom) endet eine COVID-19-Erkrankung viel häufiger tödlich als bei Menschen ohne Trisomie 21. Das ist das das Ergebnis einer britischen Kohortenstudie, die Gesundheitsdaten von mehr als 8,2 Millionen Briten untersuchte. Von den Untersuchten hatten 4.053 ein Down-Syndrom.
Ergebnis: 68 Personen mit Down-Syndrom starben im Beobachtungszeitraum vom 24. Januar bis 30. Juni, 27 (39,7 Prozent) von ihnen an/mit COVID-19, 17 (25,0 Prozent) an Lungenentzündung oder Pneumonitis und 24 (35,3 Prozent) an anderen Ursachen. Von den Personen ohne Down-Syndrom starben 41.685, 8.457 (20,3 Prozent) an/mit COVID-19, 5.999 (14,4 Prozent) an Lungenentzündung oder Pneumonitis und 27.229 (65,3 Prozent) an anderen Ursachen.
Bereinigt um Alter und Geschlecht erhöte sich die Wahrscheinlichkeit für COVID-19-bedingte Todesfälle bei Erwachsenen mit versus ohne Down-Syndrom auf das 24,94-Fache (95% CI, 17,08 bis 36,44). Nach Anpassung an Alter, Geschlecht, ethnische Zugehörigkeit, BMI, Demenzdiagnose, Pflegeheimaufenthalt, angeborene Herzkrankheit und eine Reihe anderer komorbider Erkrankungen und Behandlungen betrug die Wahrscheinlichkeit für COVID-19-bedingte Todesfälle noch das 10,39-Fache (CI 7,08 bis 15,23); für den Krankenhausaufenthalt war die Wahrscheinlichkeit um das 4,94-Fache (CI 3,63 bis 6,73) erhöht.
Hintergrund der Studie: Im Vereinigten Königreich wurde eine strikte Selbstisolierung (Abschirmung) für diejenigen empfohlen, die aufgrund des ausgewählter Vorerkrankungen oder nach Ermessen ihrer Allgemeinmediziner als klinisch äußerst anfällig eingestuft werden. Das Down-Syndrom steht weder auf der britischen Abschirmungsliste noch auf der Liste der Gruppen mit "erhöhtem Risiko" der US-amerikanischen Behörde CDC.
Ashley Kieran Clift et al., "COVID-19 Mortality Risk in Down Syndrome: Results From a Cohort Study Of 8 Million Adults", Annals.org, 21. October 2020, https://doi.org/10.7326/M20-4986
27. Oktober 2020
------------------------------------------
Wie verändern sich die Bestandteile der Atemluft von SARS-CoV-2-Infizierten?
Bei einer SARS-CoV-2-Infektion bilden sich sogenannte flüchtige organische Verbindungen (VOC) in der Atemluft. Deren Analyse könnte zur Diagnostik der Viruserkrankung genutzt werden, schreiben Forscher von der Universität Edinburgh und des Klinikums Dortmund. Sie haben in ihrer Studie ein Analyseverfahren an COVID-19-Patienten getestet.
Ähnlich wie bei einer Diabeteserkrankung verändert sich die Atemluft bei einer Coronavirus-Infektion. Speziell trainierte Hundenasen können diese Veränderungen riechen und davor warnen. Allerdings ist das Training der Tiere langwierig und daher für den breiteren klinischen Einsatz wenig praktikabel. Darum suchen Wissenschaftler nach einer elektronischen Methode, die VOC nachzuweisen.
Dabei wird unter anderem ein Gas-Chromatograf verwendet, der mit einer Ionen-Mobilitäts-Spektrometrie (GC-IMS) verbunden ist. Die getesteten Patienten pusten für die Analyse in ein Einwegröhrchen aus Plastik, aus dem dann mittels einer einfach Spritze die Luft entnommen und in den Gaschromatograf eingespeist wird. Bereits nach kurzer Zeit und ohne Reagenzien liegen dann die Ergebnisse vor. Diese Diagnostik-Methode eignet sich nach Angaben der Autoren auch für Schnelltests vor Ort.
Übereinstimmung mit PCR-Tests beträgt 80 Prozent
Für die Studie wurden die Proben von COVID-19-Patienten mit denen von Patienten mit Atemwegerkrankungen wie etwa Asthma, COPD oder anderen viralen und bakteriellen Infektionen verglichen. Außerdem verglichen die Wissenschaftler die Testergebnisse von Abstrichen mit denen der Atemluft-Analyse. Hierbei zeigte sich eine Treffsicherheit von 80 Prozent (Sensitivität/Spezifität 82,4 %/75 %; AUC-Wert 0,87).
Woher die VOC bei SARS-CoV-2 kommen, zu denen in den Untersuchungen beispielsweise Ethanol, Methanol sowie Octanal, Aceton und auch Isopren, Propanol, Propanal und Heptanal zählten, können die Forscher derzeit nur vermuten. Wahrscheinlich entsteht das freigesetzte Aceton durch den Angriff der Viren auf die Beta-Zellen in der Bauchspeicheldrüse und das Methanol aufgrund einer veränderten Darmflora. Die entstandenen Aldehyde könnten mit weiteren Entzündungsprozessen zu tun haben.
Ruszkiewicza, D., M. et al. "Research PaperDiagnosis of COVID-19 by analysis of breath with gas chromatography-ion mobility spectrometry - a feasibility study" 9 Oct 2020 in The Lancet DOI: 10.1016/j.eclinm.2020.100609++++++++++
Pathomechanismus von schweren COVID-Verläufen ähnelt dem bei systemischem Lupus erythematodes
Eine in Nature Immunology publizierte Studie zeigt, dass es bei schweren COVID-19-Verläufen zur gleichen Aktivierung von B-Zellen und Autoantikörperbildung kommt wie bei Patienten mit akuten Schüben des systemischen Lupus erythematodes (SLE). Das wirft nach Einschätzung von Experten die Frage auf, ob der Einsatz von zielgerichteten immunmodulatorischen Therapien, die beim SLE eingesetzt werden, auch bei schweren COVID-19-Erkrankungen erfolgversprechend sein könnte.
Der systemischen Lupus erythematodes (SLE) ist eine chronisch-entzündliche, meistens schubförmig verlaufende Autoimmunerkrankung mit zum Teil lebensbedrohlichen Verläufen. Es kommt zu Manifestationen an verschiedenen Organen wie Haut, Lunge, Herz, zentralem Nervensystem, Muskeln, Gelenken - und den Nieren. Die Ursachen sind multifaktoriell, die Pathomechanismen komplex. Bekannt ist: Es kommt zu einer Aktivierung von Immunzellen sowie zur Bildung verschiedener Autoantikörper, die körpereigene, gesunde Zellen angreifen, mit der Folge von Immunkomplexablagerungen, die schwere Entzündungprozesse im Körper anstoßen.
Die US-amerikanische Arbeitsgruppe zeigte nun in ihrer Arbeit, dass bei schwerkranken COVID-19-Patienten der gleiche Pathomechnaismus zugrunde liegt. Es kommt bei diesen Patienten ebenfalls zu einem Anstieg von autoantikörperbildenen Zellen, den sogenannten extrafollikulären CD19+-B-Zellen, sowie zu deren Aktivierung zu Antikörper-sezernierenden Zellen wie bei SLE-Patienten.
Matthew C. Woodruff et al., "Extrafollicular B cell responses correlate with neutralizing antibodies and morbidity in COVID-19". Nature Immunology, 2020; DOI: 10.1038/s41590-020-00814-z. https://www.nature.com/articles/s41590-020-00814-z
20. Oktober 2020
------------------------------------------
Geruchstest zeigt Korrelation von Geruchsintensität und Infektionsprävalenz
Die Messungen der Geruchsintensität könnten der Infektionsprävalenz dienen und somit eine Corona-Screening-Methode werden. Forscher aus Schweden haben für das wissenschaftliche Projekt Smelltracker durch die Abfrage der Geruchsbewertung von mittelstarken Haushaltsgerüchen wie etwa Honig, Kaffee oder auch Zahnpasta eine Einschätzungsmöglichkeit zur Prävalenz aufgezeigt. Die Einbuße der Riechfähigkeit oder sogar der Verlust des Geruchssinns zählten zu den möglichen Symptomen einer COVID-Erkrankung.
In der Untersuchung wurden 2.440 erkrankte Erwachsenen um Angaben zur Geruchswahrnehmung im Haushalt gebeten und diese dann mit möglicherweise weiteren vorliegenden COVID-Symptomen abgeglichen. Im Anschluss wurde die durchschnittliche Geruchsintensitätseinschätzung mit der vorhergesagten COVID-19-Prävalenz in der schwedischen Bevölkerung verglichen. Über mehrere Tage füllten die Teilnehmer online einen Fragebogen zur Intensität und dem positiven oder negativen Empfinden der fünf häufig im Haushalt vorhandenen Geruchsquellen aus. Das Ergebnis: Die wahrgenommene mittlere Geruchsintensität und die Prävalenz der Infektionen korrelierten (r = -0,83). Zudem wurden Erkenntnisse zum Symptomverlauf gewonnen: Wenn Patienten zunächst keine Symptome entwickelten, so nahm die Geruchsleistung im Laufe der Zeit doch spürbar ab. Weiter zeigen die Daten, dass sich ein großer Unterschied in der geschätzten Intensität zwischen Personen mit und ohne COVID-19-Symptomen ergab.Die Methode soll weiter an einer breiten, repräsentativen Masse getestet werden und könnte vor allem in wirtschaftlich armen Ländern, in denen finanzielle Mittel für Labortests fehlen, als Indikator eingesetzt werden. Neben Hygienemaßnahmen und gesellschaftlichen Strategien gegen die Ausbreitung der Coronavirus-Infektionen kommt der Überwachung der Infektionsprävalenz eine bedeutende Rolle zuteil. Die Methode der Geruchsinnkontrolle ist einfach und für die breite Masse anzuwenden. Behzad, I. et al. "Relationship Between Odor Intensity Estimates and COVID-19 Prevalence Prediction in a Swedish Population." Published 7 July in Chemical Senses https://doi.org/10.1093/chemse/bjaa034
16. Oktober 2020
------------------------------------------
Infektionsrisiko von Neugeborenen SARS-CoV-2-positiver Mütter ist gering
Eine retrospektive Kohortenanalyse überprüfte die medizinischen Daten von 101 Neugeborenen und 100 Müttern, die vom 13. März bis 24. April 2020 positiv getestet wurden. 82 Neugeborene wohnten bei ihren Müttern, die Masken tragen mussten, 19 wurden geburtsbedingt intensivmedizinisch versorgt. Das direkte Stillen wurde mit angemessener Hygiene gefördert.
Zwei Babys hatten ein positives Testergebnis auf das Virus, zeigten jedoch keinerlei klinische Anzeichen von COVID-19. Ansonsten gab es keine Anzeichen einer Übertragung des Virus bei den untersuchten Kindern. 55 Säuglinge wurden in den ersten zwei Lebenswochen in einer neuen COVID-19-Neugeborenen-Nachsorgeklinik nachuntersucht, alle blieben gesund. Diese Ergebnisse legen nach Einschätzung der Autoren nahe, dass während der COVID-19-Pandemie eine Trennung von infizierten Müttern und deren Neugeborenen möglicherweise nicht gerechtfertigt ist und auch das direkte Stillen sicher zu sein scheint.
Dani Dumitriu et al., "Outcomes of Neonates Born to Mothers With Severe Acute Respiratory Syndrome Coronavirus 2 Infection at a Large Medical Center in New York City", JAMA Pediatr. Published online October 12, 2020. doi:10.1001/jamapediatrics.2020.4298
15. Oktober 2020
------------------------------------------
Fall in den USA: SARS-CoV-2-Reinfektion führt zu schwererem COVID-Verlauf
Eine in "The Lancet" erschienene Studie beschreibt den ersten bestätigten Fall einer SARS-CoV-2-Reinfektion in den USA. Nur 48 Tage nach dem ersten Test wurde der 25-jährige Patient erneut durch einen PCR-Test positiv getestet. Besorgniserregend ist laut Studienautoren, dass die SARS-CoV-2-Reinfektion zu einer schlimmeren Erkrankung führte als die erste Infektion. Der Patient musste hospitalisiert und mit Sauerstoff versorgt werden. Nach der Reinfektion hatte der Patient positive Antikörper. Ob er nach der ersten Infektion bereits Antikörper hatte, ist unbekannt.
Die Sequenzierung des viralen Genoms zeigte, dass beide Proben zu einer in Nordnevada vorherrschenden Mutationsgruppe gehörten, sie unterschieden sich jedoch signifikant, wodurch die Wahrscheinlichkeit, dass das Virus von derselben Infektion stammt, gering sei.
WHO beauftragt Nachforschungen
Ist eine Reinfektion bei COVID-19 möglich?
Können COVID-19-Patienten rückfällig werden? In Südkorea wird um die erneuten Positiv-Tests von bereits Genesenen gerätselt, die als immun galten. Was ist mit dem Reaktivierungspotenzial von SARS-CoV-2?
Der beschriebene Fall (männlich, 25 Jahre) ist die vierte dokumentierte Reinfektion mit SARS-CoV-2, nach Fällen in Hongkong (männlich, 33 Jahre), Belgien (weiblich, 51 Jahre) und Ecuador (männlich, 46 Jahre). Die Autoren betonen jedoch, dass Reinfektionen nur bei symptomatischen Verläufen mit anschließenden Tests erkannt werden können. Aufgrund des Mangels an umfassenden Tests und Überwachung sei offen, wie häufig eine erneute Infektion bei Personen auftritt, die sich von ihrer ersten Infektion erholt haben. Asymptomatische Reinfektionsfälle könnten nur durch routinemäßige oder situationsbedingten Tests, etwa an Flughäfen, auffallen.
Nach Ansicht der Autoren wird die Anzahl der asymptomatischen Reinfektionen wahrscheinlich stark unterschätzt. Weitere Untersuchungen seien darum notwendig.
Fest stehe nach Einschätzung eines Kommentars in "The Lancet" aufgrund der dokumentierten Reinfektionsfälle jedoch schon jetzt, dass sich die Gesellschaft nicht auf eine durch natürliche Infektionen erworbene Immunität verlassen kann. Die Strategie, auf diese Weise eine Herdenimmunität zu erreichen, "ist nicht nur für viele tödlich, sondern auch nicht effektiv", schreibt Akiko Iwasak. Stattdessen erfordere Herdenimmunität sichere und wirksame Impfstoffe und eine robuste Impfimplementierung.
Richard L. Tillett et al. "Genomic evidence for reinfection with SARS-CoV-2: a case study", Published:October 12, 2020, DOI:https://doi.org/10.1016/S1473-3099(20)30764-7
Akiko Iwasak, "What reinfections mean for COVID-19", Lancet infect Dis 2020, Published Online October 12, 2020, https://doi.org/10.1016/S1473-3099(20)30783-0
++++++++++
Studie berechnet Pandemie-bedingte Übersterblichkeit für 21 Länder
Eine internationale Studie hat für 19 Industrieländer in Mittel- und Westeuropa sowie Australien und Neuseeland den Gesamtmortalitätseffekt der Pandemie berechnet. Danach starben von Mitte Februar bis Mai 2020 in diesen Ländern 206.000 mehr Menschen als ohne die Pandemie. Die Zahl der Todesfälle, Todesfälle pro 100.000 Einwohner und die relative Zunahme der Todesfälle waren in den meisten Ländern bei Männern und Frauen ähnlich.
England, Wales und Spanien verzeichneten den größten Effekt: In England und Wales kam es zu einem relativen Anstieg von 37 (30-44) Prozent, in Spanien von 38 (31-45) Prozent. In Bulgarien, Neuseeland, Slowakei, Australien, Tschechien, Ungarn, Polen, Norwegen, Dänemark und Finnland kam es zu Veränderungen der Sterblichkeit, die von möglichen kleinen Rückgängen bis zu einem Anstieg von 5 Prozent oder weniger. Die heterogenen Mortalitätseffekte der COVID-19-Pandemie spiegeln laut den Autoren, wie gut die Länder mit der Pandemie umgegangen sind und wie belastbar die jeweiligen Gesundheitssysteme sind. Deutschland ist nicht unter den betrachteten Nationen.
Kontis, V., Bennett, J.E., Rashid, T. et al. Magnitude, demographics and dynamics of the effect of the first wave of the COVID-19 pandemic on all-cause mortality in 21 industrialized countries. Nat Med (2020). https://doi.org/10.1038/s41591-020-1112-0
13. Oktober 2020
------------------------------------------
Antikörperkonzentration nach COVID-19-Erkrankung länger feststellbar als bisher angenommen
Frühere Studien hatten zu belegen versucht, dass Patienten nach einer COVID-19-Erkrankung eine Immunität entwickeln, die nur von begrenzter Dauer ist. In den beiden neuen Studien wurden nun bedeutend höhere Fallzahlen untersucht - und die Wissenschaftler kommen zu anderen Ergebnissen als ihre Kollegen: Auch drei Monate nach der Erkrankung war die Antikörperkonzentration nicht wieder abgefallen, sowohl im Blut als auch im Speichel der Patienten waren protektive Antikörper feststellbar.
So untersuchten US-Forscher um Richelle Charles vom Massachusetts General Hospital in Boston mehrfach Blutproben von insgesamt 343 Patienten, die zuvor schwer an COVID-19 erkrankt waren. 93 Prozent davon waren im Krankenhaus gewesen. Die Letalitätsrate lag bei 13 Prozent. Für die Studie wurden Plasma- und/oder Serumantikörperreaktionen bis 122 Tage nach Symptombeginn gemessen und mit Reaktionen von 1.548 Personen verglichen, deren Blutproben vor der Pandemie entnommen worden waren.
Kanadische Forscher um Baweleta Isho analysierten die SARS-CoV-2-Antikörperreaktion über einen Zeitraum von 115 Tagen im Serum und Speichel von 567 Patienten und stellten ebenfalls Antikörperreaktionen über eine Dauer von über drei Monaten fest.
Anita S. Iyer et al., "Persistence and decay of human antibody responses to the receptor binding domain of SARS-CoV-2 spike protein in COVID-19 patients", published 8 Oct. 2020 in Science Immunology, doi: 10.1126/sciimmunol.abe0367
Baweleta Isho et al, "Persistence of serum and saliva antibody responses to SARS-CoV-2 spike antigens in COVID-19 patients", published 8 Oct. 2020 in Science Immunology, doi: 10.1126/sciimmunol.abe5511
++++++++++
Schwangere und Frauen, die frisch entbunden haben, haben verlängerten und unspezifischen COVID-Verlauf
Eine landesweite prospektive US-Kohortenstudie erfasst schwangere Frauen und Frauen bis zu sechs Wochen nach der Schwangerschaft, die an einer diagnostizierten oder vermuteten Infektion mit SARS-CoV-2 leiden. Analysiert werden dabei das klinische Erscheinungsbild und der Krankheitsverlauf.
Von 991 Teilnehmerinnen, die zwischen 22. März und 10. Juli 2020 erfasst wurden, hatten 736 zum Zeitpunkt des Tests Symptome von COVID-19, 594 davon wurden positiv auf SARS-CoV-2 getestet. Das Durchschnittsalter betrug 31,3 Jahre. 95 Prozent wurden ambulant versorgt.
Die häufigsten ersten Symptome in der Kohorte der Patienten, die positiv auf SARS-CoV-2-Infektion getestet wurden, waren Husten (20 Prozent), Halsschmerzen (16 Prozent), Körperschmerzen (12 Prozent), und Fieber (12 Prozent). Die mediane Zeit bis zur Symptomauflösung betrug 37 Tage (95 Prozent CI 35-39). Ein Viertel (25 Prozent) der Teilnehmer, die positiv auf SARS-CoV-2 getestet wurden, hatten acht oder mehr Wochen anhaltende Symptome.
Die Ergebnisse legen nahe, argumentieren die Autoren, dass schwangere Patientinnen ein anderes klinisches Erscheinungsbild und eine andere Morbidität aufweisen als die an COVID-19 erkrankte nicht schwangere Bevölkerung. So zeigen Schwangere eine geringere Prävalenz von Fieber und höhere Raten von Müdigkeit, Körperschmerzen und Kopfschmerzen. Zudem führt eine Schwangerschaft bei COVID-Patienten zu einem verlängerten Krankheitsverlauf.
Yalda Afshar et al., "Clinical Presentation of Coronavirus Disease 2019 (COVID-19) in Pregnant and Recently Pregnant People", Obstetrics & Gynecology: October 07, 2020 - Volume Latest Articles - Issue - 10.1097/AOG.0000000000004178 doi: 10.1097/AOG.0000000000004178
12. Oktober 2020
------------------------------------------
Geruchssinnverlust ist auch bei schwachen und mittelschweren COVID-Verläufen häufig
Der Verlust von Geruchs- und Geschmacksinn gehört zu protokollierten Symptomen der Infektion mit SARS-CoV-2. Vermutet wird ein neuronaler Zusammenhang der Viruserkrankung sowie die Betroffenheit des Bereichs des Riechkolbens, der für die Bildung des Geruchssinns vorgesehen ist - hier nistet sich das Enzym ein, welches den Viren beim Eintritt in den Körper hilft. Forscher der Johns Hopkins University School of Medicine aus Baltimore stellten in der Untersuchung von Gewebeproben aus der Nase bereits ein sehr hohes Vorkommen des Enzyms ACE-2 (Angiotensin Converting Enzyme II) fest.
US-Studie
Enzym verantwortlich für Geruchssinnverlust bei COVID-19
Ein Enzym lässt die Corona-Viren in die Zellen und ist somit verantwortlich für den Verlust des Geruchssinns vieler Patienten. Zu dem Schluss kommen US-Forscher - und machen einen Vorschlag für eine Therapie.
Jedoch gibt es bislang wenig qualitative Ergebnisse zu den olfaktorischen Störungen. Wie viele Patienten tatsächlich vorübergehenden Geruchs- und Geschmackstörungen aufweisen, ist daher nicht genau belegt. Eine kleine indische Studie brachte nun objektiv gemessene Daten dazu. Den objektiven Testungen nach sind mehr Patienten von dem beeinträchtigten Sinn getroffen, als selbst angaben.
Objektive Tests zeigen tatsächliche Betroffenheit
Die Patienten wiesen leichte bis mittelschwere COVID-Verläufe auf und waren nicht auf der Intensivstation. Nach den Symptomen gefragt, gaben knapp 27 Prozent an, eine Beeinträchtigung des Geruchssinns zu haben (n=62). Knapp elf Prozent hatte den Geschmackssinn verloren. Objektiv bewerten waren es aber deutlich mehr: So haben den Tests nach gut 41 Prozent der Studien-Teilnehmer (n=95) hier Beeinträchtigungen. Ein Drittel der Studienteilnehmer hatten den Geruchssinn vollständig verloren. Die Ergebnisse bestätigen erneut das Symptom bei einer SARS-CoV-2-Infektion, welches nach Husten, Fieber und Abgeschlagenheit zu den häufigsten Beschwerden zählt.
Rajkumar, I. et al. "Contemporary Analysis of Olfactory Dysfunction in Mild to Moderate Covid 19 Patients in A Tertiary Health Care Centre" published 30 Sept. 2020 in Indian J Otolaryngol Head Neck Surg, doi:10.1007/s12070-020-02175-3
++++++++++
Junge COVID-Patienten mit Komorbiditäten sind stark gefährdet
21 Prozent der hospitalisierten COVID-19-Patienten zwischen 18 und 34 Jahren benötigten Intensivpflege, 10 Prozent eine mechanische Beatmung und 2,7 Prozent starben. Das zeigt eine neue US-Studie, die die klinischen Profile und Verläufe von 3.222 jungen Erwachsenen untersuchte, die in den USA wegen COVID-19 ins Krankenhaus eingeliefert werden mussten.
Auffällig war laut der Studienautoren, dass die Sterblichkeitsrate der jungen Patienten im Krankenhaus zwar niedriger als bei älteren Erwachsenen mit COVID-19 war, aber ungefähr doppelt so hoch liegt wie bei jungen Erwachsenen mit akutem Myokardinfarkt. Junge Erwachsene mit mehr als einer Komorbidität (Adipositas, Hypertonie oder Diabetes) hatten ein ähnliches Risiko für einen schlechten Krankheitsverlauf Erwachsene mittleren Alters ohne Komorbidität.
Und: Mehr als die Hälfte der Patienten, die ins Krankenhaus eingeliefert werden mussten, waren Schwarze oder Hispanoamerikaner, was mit früheren Befunden über einen unverhältnismäßigen Schweregrad der Erkrankung in diesen Bevölkerungsgruppen übereinstimmt. Angesichts der stark steigenden COVID-19-Infektionsraten bei jungen Erwachsenen unterstreichen diese Ergebnisse die Bedeutung von Maßnahmen zur Infektionsprävention in dieser Altersgruppe.
Cunningham, J., Vaduganathan, M., Claggett, B., et al. "Clinical Outcomes in Young US Adults Hospitalized With COVID-19". JAMA Intern Med. Published online September 09, 2020. doi:10.1001/jamainternmed.2020.5313
9. Oktober 2020
------------------------------------------
Kinder mit COVID-19 leiden unter Vitamin D-Mangel
Anfang September kam eine retrospektive Kohortenstudie zu dem Ergebnis, dass Vitamin-D-Mangel das relative Risiko, positiv auf SARS-CoV-2 getestet zu werden, erhöht (siehe Kasten). Jetzt untersuchte eine türkische Studie, ob dies auch für Kinder gilt. Diese Untersuchung umfasste 85 Kinder im Alter zwischen einem Monat und 18 Jahren, darunter 40 Patienten, bei denen COVID-19 diagnostiziert wurden sowie 45 gesunde Kontrollpersonen mit normalen Vitamin-D-Spiegeln.
Kohortenstudie
Vitamin-D-Status könnte Einfluss auf Infektionsrisiko haben
Das relative Risiko, positiv auf SARS-CoV-2 getestet zu werden, ist einer Studie zufolge bei Patienten mit mangelhaftem Vitamin-D-Status 1,77-mal höher als bei Patienten mit unauffälligen Werten.
Ergebnis: Kindern mit COVID-19 zeigten signifikant häufiger einen niedrigen Vitamin D-Spiegel (n: 29, 72,5 Prozent) als jene aus der Kontrollgruppe (n: 11, 27,5 Prozent). Gleichzeitig war das Symptom Fieber in Gruppe 1 deutlich häufiger (34,5 Prozent) als in Gruppe 2 (0 Prozent). Es wurden jedoch keine signifikanten Korrelationen zwischen anderen klinischen Parametern und dem Vitamin D-Spiegel gefunden. Die Autoren gehen darum nicht davon aus, dass Vitamin D eine Rolle in der Physiopathologie von jungen COVID-19-Patienten spielt.
K. Yilmaz K, V. Şen, "Is Vitamin D Deficiency a Risk Factor for Covid 19 in Children?", Pediatr Pulmonol. 2020 Oct 5. doi: 10.1002/ppul.25106. Epub ahead of print. PMID: 33017102.
8. Oktober 2020
------------------------------------------
Bereits überstandene Infektionen mit anderen Coronaviren können Verlauf abschwächen
Forscher der Boston University School of Medicine haben in Kooperation mit dem Boston Medical Center in einer Studie untersucht, inwieweit bereits überstandene Infektionen in Zusammenhang mit den vier geläufigen endemischen Coronaviren den Verlauf einer COVID-19-Erkrankung beeinflussen können. Diese Viren (OC43, HKU1, NL63 und 229E) treten fast überall auf der Welt auf und verursachen vornehmlich respiratorische Infektionen.
Dafür nutzten die Wissenschaftler die Daten von knapp 16.000 Patienten, die in den vergangenen fünf Jahren auf eines der humanpathogenen Coronaviren getestet wurden. Hier ergaben 875 Fälle ein positives Testergebnis. Verglichen mit der Gruppe der Negativ-Tests fielen keine gravierenden Anhaltspunkte zu Komorbiditäten auf. Anders hingegen sind die Erkenntnisse aus den Vergleichen von COVID-19-Patienten mit früheren Positiv-Tests, deren Anzahl sich in der Datenbank auf 1.812 belief: Die Gruppe derer, die mit nachgewiesener, bereits überstandener Infektion mit einem der vier anderen Coronaviren hospitalisiert werden mussten und verstarben, lag mit 4,8 Prozent deutlich unter der Sterblichkeitsrate derer, die ohne Immunreaktionen auf die anderen Coronaviren verstarben (17,7 Prozent).
Die Schlussfolgerung der Untersuchung lautet daher, dass frühere Infektionen mit Coronaviren einen COVID-19-Verlauf abschwächen können. Die Daten zeigen eine geringere Sterberate für diesen Patientenkreis. Verhindert werden kann eine Infektion mit dem neuen Virus bisherigen Erkenntnissen nach jedoch nicht.
Sagar, M. et al. "Recent endemic coronavirus infection is associated with less severe COVID-19" published online 30 Sept 2020 in JCI: https://doi.org/10.1172/JCI143380
++++++++++
Schlaganfall kann das Erstsymptom bei jüngeren COVID-19-Patienten sein
Für ihre Metaanalyse untersuchte ein internationales Wissenschaftlerteam zehn Studien, in denen die Schlaganfallhäufigkeit bei COVID-19-Patienten angegeben wurde und kombinierten diese mit einer bisher unveröffentlichten Arbeit aus Kanada. Außerdem führten sie eine zusätzliche systematische Suche nach Schlaganfallserien bei COVID-19-Patienten durch (n = 125) und betrachteten diese zusammen mit bisher unveröffentlichten Fällen aus Kanada, den USA und dem Iran (n=35).
Die Analyse der klinischen Merkmale und Mortalität erfolgte nach Altersgruppen (<50, 50-70,> 70 Jahre) getrennt. Ergebnis: Der Anteil der COVID-19-Patienten mit Schlaganfall (1,8%, 95% CI 0,9-3,7%) und Mortalität 34,4%, 95% CI 27,2-42,4%) war "außerordentlich hoch", schreiben die Wissenschaftler. Der Verschluss großer Gefäße war in allen Altersgruppen hoch, selbst wenn keine Risikofaktoren oder Komorbiditäten vorlagen. Die Schlussfolgerung: Schlaganfall ist bei COVID-19-Patienten relativ häufig und hat verheerende Folgen für alle Altersgruppen.
Weitere Ergebnisse: 42,9 Prozent der Schlaganfall-Patienten unter 50 Jahren wiesen keine vorherigen Risikofaktoren oder Komorbiditäten auf - und 48,3 Prozent der Schlaganfälle ereigneten sich vor dem Auftreten der ersten COVID-19-Symptome.
Sebastian Fridman et al., "Stroke Risk, phenotypes, and death in COVID-19: Systematic review and newly reported cases", Neurology, Published Ahead of Print on Sept. 15, 2020 DOI:10.1212/WNL.000000000001085
5. Oktober 2020
------------------------------------------
Fehler in der Immunabwehr spielen große Rolle bei schweren Verläufen
In einer In-vitro-Studie untersuchte ein internationales Forschungsteam von der New Yorker Rockefeller University Blutproben von 987 Menschen mit einer lebensgefährlichen Covid-19-Infektion. Bei 101 Patienten fanden sie Antikörper, die sich gegen das körpereigene Interferon richteten und dessen Fähigkeit neutralisierten, SARS-CoV-2 zu blockieren. Diese Antikörper wurden bei 663 Personen mit asymptomatischer oder milder Infektion nicht gefunden und waren nur bei 4 von 1.227 gesunden Personen vorhanden. Auffällig zudem: die von dieser Immunschwäche betroffenen Patienten sind zu 95 Prozent Männer. Die gefundene Immunschwäche ist nach Einschätzung der Wissenschaftler bei mindestens 2,6 Prozent der Frauen und 12,5 Prozent der Männer verantwortlich für die Ausbildung einer lebensbedrohlichen COVID-19-Pneumonie.
Paul Bastard et al, "Auto-antibodies against type I IFNs in patients with life-threatening COVID-19", Published Online
24 Sep 2020,
DOI: 10.1126/science.abd4585
++++++++++
Genetisch bedingter Mangel an Interferon kann den Krankheitsverlauf beeinflussen
Eine zweite Studie beschäftigt sich mit dem Zusammenhang zwischen genetischen Veränderungen und schweren Verläufen von COVID-19. Die Autoren untersuchten bei 659 Patienten jene 13 Genabschnitte, die früheren Studien zufolge mit einem Defekt im Interferon-Mechanismus in Verbindung gebracht worden waren. Im Erbgut von 23 der untersuchten Patienten identifizierten sie in acht dieser Genabschnitte seltene Mutationen. Die Interferon-Spiegel im Blut dieser Patienten waren zudem extrem niedrig.
Nach Einschätzung der Autoren kann davon ausgegangen werden, dass bei diesen 3,5 Prozent der schwer Erkrankten ein genetisch bedingter Mangel an Interferon die Infektion erschwert hat. Dies lege auch nahe, heißt es weiter, dass die Verabreichung von Interferon bei ausgewählten Patienten zumindest früh im Verlauf einer SARS-CoV-2-Infektion von therapeutischem Nutzen sein kann.
Qian Zhang et al., "Inborn errors of type I IFN immunity in patients with life-threatening COVID-19", Published Online 24. Sep 2020, DOI: 10.1126/science.abd4570
30. September 2020
------------------------------------------
COVID-19 auch für Erwachsene mittleren Alters deutlich gefährlicher als Grippe
Eine neue Meta-Regressionsanalyse zeigt, dass eine exponentielle Beziehung zwischen Alter und dem Infizierten-Verstorbenen-Anteil (englisch infection fatality rate, kurz: IFR) für COVID-19 besteht. Sind die geschätzten altersspezifischen IFRs für Kinder und jüngere Erwachsene sehr niedrig, steigen sie jedoch progressiv auf 0,4 Prozent im Alter von 55 Jahren, 1,3 Prozent im Alter von 65 Jahren, 4,2 Prozent im Alter von 75 Jahren und 14 Prozent im Alter von 85 Jahren an.
Zum Vergleich: Die Influenza hat über einen mehrjährigen Zeitraum etwa in den USA eine IFR von 0,05 Prozent. Weitere Erkenntnis: Die international zu beobachtende geografische Variation der IFR erklären sich zu 90 Prozent aus der der Altersstruktur der jeweiligen Bevölkerung.
Die IFR für COVID-19 sollte nach Ansicht der Autoren darum nicht als fester Parameter angesehen werden, sondern als eng mit dem altersspezifischen Infektionsmuster verbunden. Folglich könnten Maßnahmen im Bereich der öffentlichen Gesundheit zur Minderung von Infektionen bei älteren Erwachsenen die Gesamtzahl der Todesfälle erheblich senken.
Nach einem ersten Screening von 1.145 Studien überprüften die Autoren den Volltext von 111 Studien, wovon 50 Studien aufgrund fehlender altersspezifischer Daten zur COVID-19-Prävalenz oder zu Todesfällen ausgeschlossen wurden.
Andrew T. Levin et al., "Assessing the Age Specificity of Infection Fatality Rates for COVID-19: Systematic Review, Meta-Analysis, and Public Policy Implications", medrxiv.org, 24. September 2020, https://www.medrxiv.org/content/10.1101/2020.07.23.20160895v5.full.pdf
++++++++++
Bluthochdruck erhöht das Risiko für schwere COVID-19-Verläufe
Eine Kohortenstudie aus China und Großbritannien wertete den Verlauf von 472 Patienten aus, die zwischen dem 16. Januar und dem 10. März an COVID-19 erkrankten. Dabei wurde untersucht, welchen Einfluss Bluthochdruck auf die Wahrscheinlichkeit einer Einweisung auf die Intensivstation, einer mechanische Beatmung oder einen lethalen Ausgang der Erkrankung hatte.
Ergebnis: Der zusammengesetzte Endpunkt - also eines der drei Ereignisse - trat bei 65 (13,8 Prozent) aller untersuchten Patienten auf. Eine multivariate schrittweise logistische Regressionsanalyse zeigte, dass älteres Alter (Odds Ratio [OR] 1,39, 95% -Konfidenzintervall (CI) 1,05-1,85 pro 10-Jahres-Inkrement), vorausgegangene Hypertonie (OR 2,82, 95% CI 1,09-7,29), die Neutrophilenzahl (OR 1,33) und das Lactat-Dehydrogenase-Level (OR 1,01) unabhängig mit dem Endpunkt assoziiert waren. Hypertensive Patienten hatten im Vergleich ein größeres Risiko für die Aufnahme auf der Intensivstation, die Notwendigkeit einer mechanischen Beatmung und Tod. Blutdrucksenkende Medikamente hatten keinen Einfluss auf die Ergebnisse.
Xiong Tian-Yuan et al., "Hypertension is a risk factor for adverse outcomes in patients with coronavirus disease 2019: a cohort study." Ann Med. 2020 Nov;52(7):361-366. doi: 10.1080/07853890.2020.1802059. Epub 2020 Jul 31. PMID: 32716217.
22. September 2020
------------------------------------------
BCG-Impfung schützt ältere Menschen vor Atemwegsinfektionen
In einer in Cell veröffentlichten, randomisierten Studie hat eine Impfung mit dem Tuberkuloseimpfstoff BCG bei Probanden über 65 Jahre die Zahl der Atemwegsinfektionen deutlich gesenkt. Ob ein ähnliches Vorgehen auch vor COVID-19 schützen könnte, ist unklar - wird jedoch aktuell von mehreren internationalen Studien untersucht. Mediziner des Athener Universitätskrankenhaus Attikon hatten für die Studie im September 2017 begonnen, Patienten im Alter von mehr als 65 Jahren bei der Entlassung mit BCG oder einem Placebo zu impfen.
Die Studie sollte noch einige Zeit fortgesetzt werden, die Wissenschaftler hatten sich angesichts der Pandemie dann aber zu einer Zwischenanalyse entschieden. Diese inkludierte 150 Probanden, erklären die Wissenschaftler, wobei zu diesem Zeitpunkt insgesamt 198 Probanden an der Studie teilgenommen hatten. Mit großem Effekt: in den ersten 12 Monaten nach der Krankenhausentlassung erkrankten nur 2,0 Prozent der mit BCG geimpften Senioren (n=78) an einer Atemwegsinfektion, aber 42,3 Prozent in der Placebogruppe (n=72).
Evangelos J. Giamarellos-Bourboulis et al., "Activate: Randomized Clinical Trial of BCG Vaccination against Infection in the Elderly", Cell, Published:August 31, 2020, DOI:https://doi.org/10.1016/j.cell.2020.08.051
15. September 2020
------------------------------------------
SARS-CoV-2 kann Gehirnzellen befallen
Dass sich SARS-CoV-2 nicht nur auf den Befall der Lunge beschränkt, sondern auch Zellen von Gefäßen und Organen, wie die Leber, das Herz und die Nieren, angreift, ist bereits erwiesen. Nun veröffentlichten Forscher die Ergebnisse zu Experimenten, die zeigen, dass das Virus auch die Zellen im Gehirn angreifen kann. Zuvor wurde es durch die Ermittlung von Antikörpern im Gewebe des Cortex bei drei verstorbenen COVID-19-Patienten nachgewiesen. An der Yale School of Medicine in New Haven/Connecticut zeigen nun Versuche mit Mäusen und Zellkulturen aus Stammzellen zur Hirnzelluntersuchung im Labor, dass eben auch diese angegriffen werden.
Demnach scheinen die Coronaviren in der Lage, Nervenzellen zu identifizieren und dabei vor allem die kortikalen Neuronen der Großhirnrinde zu bevorzugen. Allerdings stellten die Forscher fest, dass die Infektion nicht zum Tod der Neuronen führt, jedoch ein Zelltod in der Umgebung stattfand. Das könnte auf die Unterversorgung der Zellen mit Sauerstoff aufgrund der Infektion zurück zu führen sein. Eindeutig nachweisen konnten die Forscher die Bildung der ACE2- Rezeptor in den Hirnzellen, die für den Eintritt in diese und somit für die Infektion Voraussetzung sind. Unklar bleibt bislang, wie die Viren ins Gehirn gelangten - eventuell über die Blutgefäße. Möglich wäre aber auch der direkte Weg von der Nasenschleimhaut über die Geruchsnerven ins Gehirn.
Beim Mäuseversuch gelang die Infektion des Gehirns. Die Tiere nahmen stark an Gewicht ab und starben. Während andere Versuchstiere, deren Lungen infiziert waren, eher leicht erkrankten und kein Gewicht verloren.
Iwasaki, A. et al; "Neuroinvasion of SARS-CoV-2 in human and mouse brain" published on September 08, 2020 doi: https://doi.org/10.1101/2020.06.25.169946
14. September 2020
------------------------------------------
Theorie zur Immunität: Weiterer Vorteil des Maskentragens?
US-Forscher veröffentlichten vergangene Woche die Hypothese, dass durch die geringe Virenkonfrontation beim Tragen von Masken eventuell eine Immunantwort ohne schlimmere Infektion gebildet werden könnte.
Masken und Mund-Nase-Schutz schützen vor allem andere Personen vor einer möglichen Infektion durch Tröpfchen und Aerosole. Wenn jeder in den geschlossenen Bereichen des öffentlichen Lebens eine trägt, ist ein großer Teil für den Infektionsschutz getan - soweit sind sich Wissenschaftler und Mediziner einig. Zwei Wissenschaftler aus den USA gehen jetzt noch einen Schritt weiter und veröffentlichen eine Theorie, die Maske einen weiteren nützlichen Effekt zuspricht. Ihrer Auffassung nach kann das Tragen des Mund-Nasen-Schutzes helfen, immun gegen SARS-CoV-2 zu werden.
Ihren Ansatz erklären Monica Ghandi und George Rutherford von der University of California in San Francisco in einem Meinungsbeitrag im New England Journal of Medicine so: Die meisten Masken halten zwar den Großteil der Töpfchen zurück, ein geringer Teil gelangt jedoch mit der Atemluft durch das Material in die Umgebungsluft. Diese Virenmenge ist idealerweise so gering, dass sich andere Personen, zumal sie auch eine Maske tragen, nicht infizieren. Das Immunsystem kann die geringe Dosis an Erregern abwehren. Eine mögliche, leichte Infektion bleibt unbemerkt. Durch die geringe Virusanzahl kommt es zudem zu weniger stark ausgeprägten Symptomen.
Dennoch, und das ist der Kern der Hypothese, könnte es durch den Kontakt mit den Viren zu einer Immunreaktion kommen und sich daraus eine Immunität entwickeln. Diese kann dann als Schutz vor weiteren Infektionen dienen. Diesen Ansatz führen die Forscher auf die sogenannte Variolation bei früheren Versuchen der Pockenimpfung zurück, bei denen Patienten eine Sekret mit einer geringen Menge Viren über das Einreiben der Haut verabreicht wurden. Die Hoffnung dabei war, dass die Menge reicht, um eine Immunantwort zu bilden, nicht aber um eine Infektion auszulösen.
Belegt ist aber noch nicht, ob auch leichte und asymptomatische Infektionen zur einer anhaltenden Immunität führen können und ob eine kleine Virendosis nicht auch einen stärkeren Effekt auslösen kann.
Monica Gandhi, George W. Rutherford; "Facial Masking for Covid-19 - Potential for 'Variolation'" as We Await a Vaccine", published on September 8, 2020, at NEJM.org; DOI: 10.1056/NEJMp2026913
++++++++++
Unerklärte klinische Probleme könnten Ursache in unerkannter COVID-19-Erkrankung haben
In einem Pariser Klinikum gab es bei der Überprüfung der analytischen Leistungsfähigkeit des Antikörpertests "Abbott SARS-CoV-2 IgG-Assay" einen interessanten Zufallsbefund. Der Test von 259 Probanden, bei dem zusätzlich die SARS-CoV-2-IgG-Positivitätsraten in COVID-19-positiven und COVID-19-freien Bereichen des Krankenhauses verglichen wurden, bescheinigte dem Verfahren eine Sensitivität von 94 Prozent und eine Spezifität von 100 Prozent.
Dabei fiel jedoch auf, dass mehrere stationäre Patienten, die in vermeintlich COVID-19-freien Bereichen stationiert waren und eine Vielzahl ungeklärter klinischer Merkmale aufwiesen - einschließlich Herz-, Gefäß-, Nieren-, Stoffwechsel- und Infektionsstörungen - unerwartet als seropositiv getestet wurden. Die Autoren leiten daraus ab, dass die SARS-CoV-2-Serologie auch ein nützliches Instrument zur retrospektiven Diagnose von COVID-19-Infektionen sein kann.
Hélène Péré et al.; "Unexpected diagnosis of COVID-19-associated disorders by SARS-CoV-2-specific serology", Journal of Clinical Virology, Volume 132, November 2020, 104568, https://doi.org/10.1016/j.jcv.2020.104568
11. September 2020
------------------------------------------
Unterschiedliche Kopfschmerz-Formen bei SARS-CoV-2
Das Spektrum der Kopfschmerzen bei einer SARS-Cov-2-Infektion ist vielfältig. Für eine Studie mit 112 Patienten, die selbst im Gesundheitswesen als medizinische Fachkräfte tätig sind, befragten und untersuchten die Wissenschaftler um Jesús Porta‐Etessam der neurologischen Fakultät der Universidad Complutense de Madrid die Charakteristika der Kopfschmerzen. Diese traten unabhängig vom Fieber auf und werden unterschiedlich beschrieben. Das Symptom trat am dritten oder vierten Tag der Infektion auf.
Dabei berichteten 46 Prozent der Patienten von hemicranialen, halbseitigen Kopfschmerzen, 42,5 Prozent von Schmerzen mit dumpf-drückendem holocraniellen Charakter und 17,7 Prozent von okzipitalen Kopfschmerzen. Mit 80 Prozent der Befragten beschriebt die große Mehrheit die Schmerzen in jedem Fall als drückend. 17 Prozent der Patienten hatten bereits vorher regelmäßige Kopfschmerzen in Form von Migräne. Sie beschrieben den Kopfschmerz während der Erkrankung am häufigsten als pulsierend. Einige Patienten litten zudem an Übelkeit und Lichtempfindlichkeit. Die Studienbetreiber führen die heterogene Erscheinung der Schmerzen auf verschiedene pathophysiologische Mechanismen zurück.
Porta‐Etessam J. et al. Spectrum of Headaches Associated With SARS‐CoV‐2 Infection: Study of Healthcare Professionals. Headache J Head Face Pain. 2020 :1697-1704. doi:10.1111/head.13774
10. September 2020
------------------------------------------
Corona-Hygienemaßnahmen verhindern auch andere Infektionen
Im Krankenhaus erworbene Infektionen ( Hospital-Acquired Infections, kurz: HAI) sind häufige Komplikationen bei akuten Patienten, die in neurologischen Einheiten stationiert sind, insbesondere bei Schlaganfallpatienten. Eine italienische Studie untersuchte nun, ob die durch die Pandemie verbesserten Hygienemaßnahmen eine Abnahme der HAI in "COVID-freien" neurologischen Einheiten zur Folge hatten. Dazu wurden 319 Patienten, die ab dem 8. März 2020 in Neurologie- und Schlaganfallabteilungen des Policlinico Umberto I-Krankenhauses in Rom hospitalisiert und vor dem 31. Mai 2020 entlassen wurden (n = 103), in die Studie aufgenommen und mit Patienten verglichen, die im gleichen Zeitraum 2019 ins Krankenhaus eingeliefert wurden (n = 216).
Ergebnis: Bei Patienten, die 2019 eingeliefert wurden, lag die Inzidenz von HAIs bei 31,5% (95% -Konfidenzintervall (CI): 0,25-0,38), verglichen mit 23,3% (95% -Konfidenzintervall: 0,15-0,32) im Jahr 2020 ( p = 0,12). Dabei war der Krankenhausaufenthalt 2020 unabhängig mit einem geringeren HAI-Risiko verbunden und mit einer geringeren Anzahl von HAIs sowie einer geringeren Anzahl von verschriebenen Antibiotika pro Patient verbunden. Die Autoren sehen darin Belege für die Auswirkungen strengerer Hygienemaßnahmen auf HAIs.
Emanuele Irelli et al., "The potential impact of enhanced hygienic measures during the COVID-19 outbreak on hospital-acquired infections: A pragmatic study in neurological units", Journal of the Neurological Sciences Volume 418, 15 November 2020, 117111, https://doi.org/10.1016/j.jns.2020.117111
++++++++++
COVID-19 kann offenbar Insulinmangel-Diabetes verursachen
Wissenschaftler des Uniklinikums Schleswig-Holstein (UKSH) berichten von einem Fall, in dem die Manifestationen von insulinabhängigem Diabetes nach einer SARS-CoV-2-Infektion bei einem 19-Jährigen auftraten, die für Typ-1-Diabetes mellitus typisch sind. Die Anamnese des Patienten ergab eine wahrscheinliche COVID-19-Infektion 5-7 Wochen vor der Aufnahme.
Interessanterweise trug der Patient einen menschlichen Leukozyten-Antigen-Genotyp, von dem angenommen wurde, dass er nur ein geringfügig erhöhtes Risiko für die Entwicklung eines Autoimmun-Typ-1-Diabetes mellitus bietet. Obwohl der Bericht die Kausalität zwischen COVID-19 und der Entwicklung von Diabetes bei diesem Patienten nicht vollständig feststellen kann, so die Autoren, sei davon auszugehen, dass SARS-CoV-2 hier selbst die Betazellen im Pankreas angegriffen hat.
Hollstein, T. et al. "Autoantibody-negative insulin-dependent diabetes mellitus after SARS-CoV-2 infection: a case report. Nat Metab (2020). https://doi.org/10.1038/s42255-020-00281-8
------------------------------------------
An dieser Stelle gibt die zm-Redaktion regelmäßig einen kurzen Überblick über ausgewählte Studien zu SARS-CoV-2.