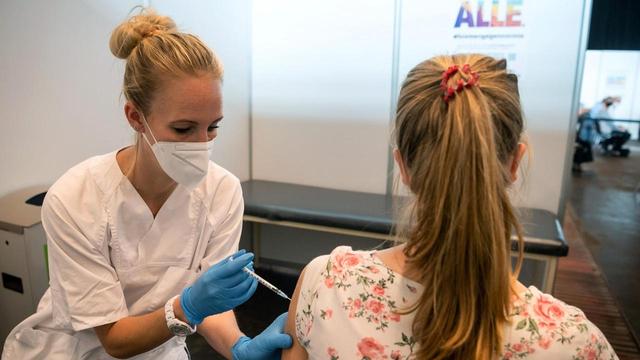
von Constanze Kindel
Emmanuelle Charpentier und Jennifer Doudna ist der wohl bedeutendste Schritt der vergangenen Jahre in der Genforschung gelungen. Sie enträtselten einen Mechanismus, mit dem sich das Erbgut so gezielt wie nie zuvor verändern lässt, und entwickelten daraus eine hochwirksame Genschere. Dafür sind die beiden Forscherinnen nun mit dem Nobelpreis für Chemie ausgezeichnet worden. Wie funktioniert Crispr/Cas9? Und welche Möglichkeiten bietet das Verfahren?
Entdeckung, das klingt zu sehr nach Zufall. So schicksalhaft, so absichtslos. Nicht nach dem, was Forschung wie ihre wirklich ausmacht: ausprobieren, abarbeiten – zähe, methodische Jagd mit ungewissem Ausgang, einem Verdacht auf der Spur. Ein Herantasten, das Schritt für Schritt die Grenzen des Wissens verschiebt. Entdeckung also: Der Begriff passt nicht richtig, findet Emmanuelle Charpentier. „Man sucht ja nicht nach etwas und findet es plötzlich“, erklärt sie, „sondern man entschlüsselt über Monate und Jahre einen Mechanismus.“
Über den von ihr entschlüsselten Mechanismus hat die französische Mikrobiologin in den letzten Monaten viel gesprochen, auf Konferenzen in Chicago, Rom, Heidelberg. Sie nennt das Ergebnis ihrer Forschung einen „game changer“.
Game Changer: die Wende im Spiel, der große, alles verändernde Wurf. Ein Durchbruch, der Emmanuelle Charpentier, das gilt als sicher, früher oder später den Nobelpreis bringen wird.
GEOkompakt Nr. 54
Unser Erbe, unsere Gene
01.10.2020
GEOkompakt über unsere Gene und die Frage, warum wir sind, wie wir sind
Ihrer Forschung ist es zu verdanken, dass Wissenschaftler weltweit heute in der Lage sind, wie nie zuvor gezielt in den Bauplan des Lebens einzugreifen, das Erbgut zu manipulieren, es umzuschreiben – und zwar mit einem Verfahren, das vergleichsweise kostengünstig ist und in der Regel verblüffend schnell funktioniert.
Die 49-jährige Französin, seit 2015 Direktorin des Berliner Max-Planck-Instituts für Infektionsbiologie, ist in weniger als fünf Jahren aufgestiegen zum Weltstar der Wissenschaft.
Im August 2012, damals forscht sie noch an der Universität im schwedischen Umeå, veröffentlicht sie in einer Fachzeitschrift einen Aufsatz, nur etwas mehr als fünf Seiten lang: „A Programmable Dual-RNA-Guided DNA Endonuclease in Adaptive Bacterial Immunity“. Gemeinsam mit der amerikanischen Forscherin Jennifer Doudna und anderen Kollegen beschreibt sie darin, wie sich das Bakterium Streptococcus pyogenes vor Viren schützt. Dieser Krankheitserreger kann etwa Scharlach auslösen oder eitrige Mandelentzündungen. Aber Streptococcus pyogenes ist auch selbst angreifbar: durch Viren.
Das System, mit dem das Bakterium diese Infektionen abwehrt, besteht quasi aus zwei Bereichen: Archiv und Schneidwerkzeug. In seinem eigenen Erbgut legt der Einzeller wie als Erinnerungshilfe Proben nahezu aller Viren ab, mit denen er – und seine Vorfahren – je in Berührung gekommen sind. Im Falle einer erneuten Infektion wird dann das Abwehrsystem der Mikrobe aktiviert: Es prüft das Virus anhand der archivierten Proben.
Die Arbeit über Streptococcus pyogenes ist der Auftakt zu einer Revolution
Erkennt es den Eindringling, kommt das Schneidwerkzeug zum Einsatz: Ein bestimmtes Enzym, eine Art molekulares Werkzeug, durch trennt die virale DNS. Damit macht das Abwehrsystem (das die beiden Forscherinnen CRISPR-Cas9 nennen, nach den archivierten DNS-Sequenzen, CRISPR, und der DNS-Schere, Cas9) den Erreger unschädlich.
Aber die Wissenschaftlerinnen erklären in ihrem Aufsatz nicht nur, wie der Mechanismus arbeitet: Sie zeigen auch, wie sich der Abwehrschild umfunktionieren lässt zur Allzweckwaffe. Denn sie haben entdeckt, dass CRISPR-Cas9 (heute meist nur noch CRISPR genannt) eine Art Universalwerkzeug zum Umschreiben von Erbsubstanz sein kann. Mehr noch – eine Technik, mit der sich Gene gezielt verändern lassen, bei Bakterien, Pflanzen, Tieren, Menschen.
Kurz: Die Arbeit über Streptococcus pyogenes ist der Auftakt zu einer Revolution.
Noch vor wenig mehr als zehn Jahren wusste niemand in der Wissenschaft etwas über die Rolle dieses Systems bei Bakterien. Heute erscheinen fast täglich neue Studien, in denen Forscher die Ergebnisse ihrer Experimente mit CRISPR präsentieren. In denen sie etwa von Versuchen berichten, Erdnüsse ohne Allergene hervorzubringen – oder Mücken, die keine Malaria übertragen können. Es wird bereits daran gearbeitet, ausgestorbene Tiere wieder zum Leben zu erwecken. Oder Krankheiten zu heilen, bei denen es bislang wenig Hoffnung gab.
„Man startet mit einer Idee und denkt, das dauert 30 Jahre, bis daraus etwas Nützliches entsteht“, sagt Charpentier. Und dann, plötzlich, geht alles schnell.
Forscher nutzen CRISPR bereits, um das Erbgut des Menschen zu verändern
Wohl keine andere Entwicklung hat die Gentechnik in so kurzer Zeit so weit vorangebracht. Vereinfacht kann man sich das gezielte Verändern von Erbgutsequenzen mit CRISPR wie das Redigieren einer Textdatei am Computer vorstellen: Die Software findet in dem Dokument jede beliebige Buchstabenkombination, auf einer Seite, in einer Zeile. Wenn die jeweilige Stelle gefunden ist, können Tippfehler korrigiert, Buchstaben oder ganze Wörter gelöscht, ausgetauscht oder eingefügt werden.
Beim CRISPR-Verfahren setzt sich die gesuchte Buchstabenkombination zusammen aus den DNS-Molekülen Adenin (A), Guanin (G), Cytosin (C) und Thymin (T) – und zwar so aneinandergereiht, dass ihre Abfolge dem Abschnitt in der DNS-Sequenz entspricht, der verändert werden soll.
Das Enzym, die eigentliche Genschere im CRISPR-System, wird mit der entsprechenden Buchstabenkombination präpariert – gewissermaßen gleicht es damit der Suchmaske im Textverarbeitungsprogramm. Es steuert nun in der Regel genau jene Stelle im Erbgut an, die es finden soll. Dann bindet es sich an den ausgewählten Abschnitt und verursacht einen Bruch in den beiden Strängen der DNS-Doppelhelix.
Nun kann dort – wie in einem Textverarbeitungsprogramm – eine Passage gelöscht oder ein neues Wort (ein fremdes Gen) eingeschleust werden.
Molekularbiologen sind bereits seit mehr als 20 Jahren prinzipiell in der Lage, mithilfe von Enzymen bestimmte Gene zu eliminieren oder zu ersetzen. Aber die Verfahren waren teuer und langwierig. Wie CRISPR arbeiten diese frühen Genscheren mit speziellen Schneide-Proteinen, die sich an eine ausgewählte Stelle der DNS-Sequenz binden und dort den Doppelstrang der DNS durchtrennen.
Doch diese Proteine mussten für jeden Einsatz aufwendig neu verändert werden. Es brauchte eine lange Reihe von Versuch und Irrtum, bis das Protein tatsächlich die gewünschte Stelle fand. Jeder Erfolg kostete oft Hunderte gescheiterte Versuche. Mal landete das Schneidwerkzeug einen Zufallstreffer, häufig wurden DNS-Abschnitte an falscher Stelle eliminiert. Erst mit CRISPR hat das Textverarbeitungsprogramm – um im Bild zu bleiben – eine präziser arbeitende Suchmaske erhalten: Meist sehr zielgenau kann sie die gewünschte Stelle im Buch ansteuern.
Mit CRISPR ist die Technik keine hochspezialisierte Anwendung mehr, sondern weitgehend ein Standardverfahren. Was früher die Arbeit von Monaten oder gar Jahren war, dauert heute in der Regel nur noch Tage. Beinahe jedes kleine Labor kann die Methode anwenden.
CRISPR hat das Basteln am Erbgut, die Genchirurgie, schneller, billiger, effizienter gemacht als je zuvor. Ein Biologiestudent mit einer Labor-Standardausstattung wäre imstande, mit diesem System ein Gen auszuschalten, sagt Charpentier. Ein paar Tage Arbeit, Materialkosten von kaum ein paar Hundert Euro.
Mit der CRISPR-Technik lassen sich fremde Gene zielgenau ins Erbgut schleusen.
© Soleil Nordic / shutterstock
Bildbeschreibung: Um fehlerhafte Gene auszutauschen oder Organismen mit neuen Eigenschaften zu erschaffen, fügen Forscher mithilfe der CRISPR-Technik fremdes Erbgut (grün) in einen DNS-Abschnitt (blau) ein. Damit das fremde Gen an die richtige Position im DNS-Strang gelangt, wird die mit einem Erkennungsmolekül markiert. Das besteht aus der präzisen genetischen Buchstaben folge der gesuchten Stelle und lagert sich entsprechend an. Im nächsten Schritt durchtrennt ein Enzym, eine Art molekulares Werkzeug (ovale Struktur), den DNS-Strang an ebenjener Stelle, an der sich das Erkennungsmolekül angelagert hat. Auf diese Weise entsteht eine Lücke in der DNS. Die körpereigenen Reparaturmechanismen sorgen dafür, dass der Strangbruch sich wieder schließt. Das fremde Gen ist so präpariert, dass es dabei automatisch in die Lücke eingebaut wird. Das fremde Gen befindet sich schließlich in der ursprünglichen DNS und kann dort seine Funktion aufnehmen.
US-Firmen verkaufen bereits CRISPR-Baukästen, mit denen sich selbst Laien an der Technik versuchen können. Das kalifornische Unternehmen „The Odin“ bietet beispielsweise Sets an, mit denen man in bestimmten Bakterien ein Gen austauschen kann, sodass sie anschließend auf speziellen Nährböden wachsen.
Das Start-up will Menschen sogar Eingriffe ins eigene Erbgut ermöglichen. Auf einer Biotechnologie-Konferenz in San Francisco im Oktober 2017 setzte sich Odins Gründer Josiah Zayner, promovierter Biophysiker, eine Spritze in den Unterarm. Der Inhalt, verkündete Zayner, ziele auf sein Myostatin-Gen, das im Körper das Muskelwachstum hemmt. Als erster Mensch werde er versuchen, auf diese Weise sein eigenes Genom zu verändern. CRISPR im Selbstversuch: größere Muskeln mit Genchirurgie.
Schon warnt die US-Lebens- und Arzneimittelaufsichtsbehörde FDA, der Verkauf von Produkten zur Gentherapie verstoße gegen das Gesetz, man sei beunruhigt über die damit verbundenen Sicherheitsrisiken.
Viele große Probleme der Medizin scheinen mit CRISPR lösbar

Doch CRISPR hat auch die etablierte Wissenschaft elektrisiert. Forschungseinrichtungen, Universitäten und Firmen treiben den Einsatz der Methode voran. Schon jetzt lassen sich mit CRISPR sehr effektiv Nutztiere und Nutzpflanzen Bedingungen und Bedürfnissen anpassen, Schweine mit geringerem Körperfettanteil züchten oder Maniokpflanzen und Weizen, die gegen verbreitete Viren und Pilze immun sind.
Mediziner wollen mithilfe von CRISPR unter anderem bessere Tiermodelle für menschliche Leiden erzeugen. Selbst komplizierte psychische Störungen wie Autismus und Schizophrenie, an denen eine Vielzahl von Genmutationen in unterschiedlichen Kombinationen beteiligt sind, könnten so begreifbarer werden, Behandlungseffekte sich einfacher simulieren lassen.
Viele große Probleme der Medizin scheinen mit CRISPR plötzlich lösbar. So ließen sich beispielsweise Antibiotikaresistenzen eliminieren, indem man Viren so verändert, dass sie Bakterien abtöten: Das Immunsystem der Einzeller wendet sich gegen sie selbst.
Oder der Mangel an Spenderorganen für Transplantationen: Vielleicht lassen sich Herzen, Lungen, Nieren dank der Genschere bald in Schweinen züchten. In deren Erbsubstanz finden sich bislang viele Krankheitserreger, die von Elterntieren an ihre Nachkommen vererbt werden. US-Forschern gelang es mit der neuen Technik erstmals, diese Viren unschädlich zu machen.
In China gibt es bereits erste CRISPR-Studien zur Krebstherapie. An der Sichuan-Universität in Chengdu injizierten Forscher Ende 2016 erstmals einem Patienten, der an einem aggressiven Lungenkrebs litt, mit CRISPR genchirurgisch bearbeitete Immunzellen.
Einem anderen chinesischen Team gelang es mit der Technik erstmals, ein komplettes Chromosom zu entfernen: die dritte, überzählige Kopie des 21. Chromosoms aus im Labor gezüchteten Zellen eines Menschen mit Trisomie 21, also dem Downsyndrom. Könnte man Embryonen, bei denen dieser Defekt noch im Mutterleib entdeckt wird, in Zukunft per Genschere heilen? Vieles scheint möglich.
Auf mehr als 10.000 schätzt die Weltgesundheitsorganisation die Zahl der erblichen Erkrankungen, die von einem einzigen fehlerhaften Gen verursacht werden. Leiden wie die Nervenkrankheit Chorea Huntington, bei der das Gehirn fortschreitend erkrankt und beispielsweise Bewegungsstörungen verursacht. Oder die Duchenne-Muskeldystrophie, die den Körper lähmt. Oder die Sichelzellanämie, die etwa Herz, Augen, Nieren schädigt. Diese monogenen Erbkrankheiten sind in nächster Zeit das naheliegende Ziel für den Einsatz von CRISPR.
Gentechnik
Wie Genforscher die Medikamente der Zukunft entwickeln
Wissenschaftler forschen an der DNS, um maßgeschneiderte Arzneien zu entwickeln
Manche Forscher aber wollen mehr, als diese Krankheiten aufzuhalten: Sie wollen sie ausschalten, lange bevor sie ausbrechen können – und zwar bereits in der Keimbahn, also auf dem Weg von der befruchteten Eizelle zu den Keimzellen des neuen Lebewesens.
Die genchirurgische Manipulation von Ei- und Spermazellen soll Embryonen von Erbkrankheiten befreien. Ebendiese Interventionen aber würden auch auf das Erbgut künftiger Generationen wirken: Werden Gene in diesem frühesten Stadium der menschlichen Entwicklung manipuliert, vererben sich diese Veränderungen später weiter – ein Eingriff in die menschliche Evolution.
Ethisch sind diese Eingriffe höchst umstritten. Dauerhaft verhindern aber lassen sie sich kaum – zumal es keinen weltweiten Konsens über den Einsatz der Gentechnik und seine Grenzen gibt.
So hat zum Beispiel eine US-Forschergruppe bereits mit dem Einsatz der Technik an menschlichen Embryonen im frühen Entwicklungsstadium experimentiert. Mithilfe der Genschere korrigierte das Team eine Mutation im Gen MYBPC3, die eine Verdickung des Herzmuskels auslöst – eine sogenannte hypertrophe Kardiomyopathie, die eine Hauptursache für plötzliche Todesfälle bei jungen Sportlern ist.
Emmanuelle Charpentier sagt, sie sei strikt gegen solche Eingriffe: Niemand dürfe die Keimbahn antasten.
Jennifer Doudna, ihre Kollegin bei der CRISPR-Entschlüsselung, ist sich in dieser Frage dagegen nicht so sicher. Wenn es einen Weg gebe, Menschen zu helfen, die von Erbkrankheiten betroffen sind: Wäre es erlaubt, dies nicht zu tun? Auch wenn nicht auszuschließen ist, dass die Technik, die Wünsche irgendwann über medizinische Notwendigkeiten weit hinausgehen? Dass Eltern beginnen, womöglich ihre ungeborenen Kinder bezüglich Größe, Augenfarbe, Intelligenz nach ihren Vorstellungen zu formen?
Noch ist das eine ferne Möglichkeit. Neben den ethischen Erwägungen stehen der Anwendung der Genschere am Menschen bislang auch noch etliche mögliche Risiken im Weg. Es gibt Zweifel daran, wie sicher die Technik ist. Und Bedenken, welche Folgen ihr Einsatz hätte.
Zu den technischen Schwierigkeiten zählt zurzeit noch der Transportweg: Um das Schneide-Enzym an seinen Einsatzort zu bringen, brauchen die Biologen sogenannte Gen-Fähren – ungefährliche oder künstlich inaktivierte Viren, die CRISPR-Moleküle durch die Blutbahn ins Zellinnere befördern. Aber diese viralen Genfähren erreichen schnell ihre Ballastgrenzen. Eine Alternative wären womöglich Liposomen: winzige Fettpartikel, die an Zellen andocken und ihre Ladung ins Innere der Zelle abgeben können.
Schwer wiegt auch das Problem möglicher Kollateralschäden der CRISPR-Methode – etwa wenn die Genschere ihr Ziel verfehlt und die DNS in einem anderen Abschnitt durchtrennt. Die Folgen dieser ungeplanten DNS-Brüche sind nicht abzusehen. Im schlimmsten Fall könnten die Veränderungen Krebs auslösen.
Auf einen Blick
Die VorlageBakterien nutzen den CRISPR-Mechanismus als Verteidigung, um das Erbgut von Viren zu zerschneiden.
Die TechnikDie Forscherinnen Emmanuelle Charpentier und Jennifer Doudna haben daraus eine Genschere für die Wissenschaft entwickelt.
Die AnwendungDank ihrer Erfindung ist es nun einfacher denn je, genveränderte Organismen zu erzeugen oder Erbkrankheiten zu therapieren.
US-Mediziner, die mithilfe von CRISPR den Gendefekt von Mäusen mit angeborener Blindheit korrigiert hatten, fanden nach dem Eingriff im Erbgut der nun sehenden Mäuse gut 100 größere Veränderungen und mehr als 1000 Punktmutationen, bei denen nur ein einzelnes Basenpaar der DNS verändert war.
Ob die Mutationen eine Folge der CRISPR-Behandlung waren, wie die Wissenschaftler befürchteten, oder bereits vor dem Experiment im Erbgut der Mäuse zu finden gewesen wären, ist allerdings umstritten: Die Studie hatte auf den Vergleich mit Kontrollmäusen verzichtet.
Trotzdem warnte wenig später auch eine Gruppe von Wissenschaftlern in einer Studie, dass CRISPR-Werkzeuge sorgfältig an das Genom des jeweiligen Patienten angepasst werden müssten, um sicherzustellen, dass die Technik nicht von Variationen im Genom des Patienten fehlgeleitet würde.
Längst suchen Forscher nach Wegen, auf denen sich diese Risiken umgehen lassen. Ein Team des Salk Institute in San Diego etwa hat eine neue Variante der CRISPR-Technik geschaffen, die Brüche in der DNS vermeidet. Auch an der Harvard University ist ein neues, besser zu kontrollierendes Verfahren entwickelt worden. Schon jetzt haben erste klinische Studien zur Gentherapie mit CRISPR begonnen.
Das Unternehmen „CRISPR Therapeutics“, an dem Emmanuelle Charpentier beteiligt ist, will versuchen, die Erbkrankheiten Beta-Thalassämie und Sichelzellenanämie zu heilen.
Beide Leiden werden meist von Mutationen in einem Gen ausgelöst, das an der Erzeugung von Hämoglobin beteiligt ist: einem Proteinkomplex, der Sauerstoff im Blut transportiert. Die Behandlung soll eine Form von Hämoglobin reaktivieren, die bei Säuglingen vorkommt. Die Zulassung ist beantragt.
Dass bereits erste klinische Studien gestartet sind, ist nach den Maßstäben der medizinischen Forschung rekordverdächtig schnell – noch nicht einmal sechs Jahre, nachdem zum ersten Mal die Rede war von einem neuartigen, unkomplizierten und günstigen Genschere-Verfahren.
Die Revolution in der Gentherapie hat gerade erst begonnen.
Dieser Beitrag erschien erstmals im März 2018 in "GEO kompakt Nr. 54 - Unser Erbe, unsere Gene".
#Themen
Chemie
Forschung