Fundo:
A triagem neonatal é usada para a detecção precoce de distúrbios metabólicos e endócrinos congênitos que, se não forem tratados, podem levar a crises fatais ou danos a longo prazo. Na Alemanha, a triagem neonatal é regulamentada nas diretrizes infantis do Federal Joint Committee (G-BA). Os relatórios de qualidade são criados e publicados anualmente pela Sociedade Alemã de Triagem Neonatal (DGNS Report). Os dados dos relatórios DGNS 2006-2018 são a base deste trabalho.
Método:
Para os anos 2006-2018, as prevalências foram calculadas e os dados sobre a qualidade do processo avaliados.
Resultado:
Dentre 9.218.538 nascimentos, 6.917 recém-nascidos foram identificados com uma doença-alvo. A prevalência geral é de 75 por 100.000 recém-nascidos, sendo o hipotireoidismo congênito o mais comum em 30 por 100.000, seguido por fenilcetonúria (PKU) e deficiência de acil-CoA desidrogenase de cadeia média (MCAD) em 10 por 100.000 cada um. Dos 272.205 check-ups solicitados, 80% foram atendidos. A taxa de resultados de triagem positivos (recall) caiu de 0,90% em 2006 para 0,37% em 2018. Cada quinto resultado de triagem positivo confirmou uma doença-alvo. O tratamento foi iniciado em 79% das crianças com indicação de terapia em até duas semanas.
Conclusão:
A baixa taxa de reconvocação e o início precoce do tratamento em 79% das crianças afetadas comprovam a eficácia do programa. A integração de estruturas de rastreamento e a introdução de um cadastro poderiam melhorar ainda mais a qualidade do programa.
A triagem neonatal para distúrbios metabólicos e endócrinos congênitos é uma das medidas de prevenção secundária mais bem-sucedidas na infância. Os recém-nascidos têm sido rastreados para fenilcetonúria (PKU) desde o final da década de 1960 e, desde a década de 1980, também para hipotireoidismo e galactosemia. Em 2004, o Federal Joint Committee (G-BA) incluiu a chamada "triagem neonatal estendida" (ENS) para doze doenças-alvo na diretriz infantil e, portanto, no tratamento padrão e acrescentou a tirosinemia tipo I em 2018 e grave combinada em 2019 Imunodeficiências (SCID) (1). A triagem de fibrose cística foi introduzida em 2016 com regulamentos separados (2).
Algumas doenças-alvo podem levar a crises metabólicas com risco de vida ou danos permanentes em um estágio inicial. Assim, o objetivo da ENS é identificar o maior número de crianças afetadas o mais cedo possível, mas ao mesmo tempo alertar apenas algumas famílias de crianças saudáveis com um resultado falso-positivo (conspícuo) (3). Isso requer um processo padronizado com responsabilidades definidas; esse processo é especificado pelas orientações das crianças para informação e consentimento, implementação e conteúdo da triagem e serviços laboratoriais (1, 2). No entanto, o registo dos diagnósticos de confirmação, a avaliação do rastreio e o rastreio não estão regulamentados. Este último destina-se a garantir que achados notáveis ou achados que precisam ser repetidos sejam verificados.
Métodos
O prestador de serviço que foi responsável pelo nascimento da criança é responsável pela realização do teste do pezinho. Antes da coleta de sangue, os pais devem ser informados sobre a triagem neonatal, geralmente por um médico, de acordo com as especificações da Lei de Diagnóstico Genético (4) e dar seu consentimento por escrito. O sangue nativo deve ser coletado entre 36 e 72 horas de vida, pingado em um papel de filtro especial, seco e enviado para um laboratório de triagem. Se a criança receber alta antes de 36 horas de vida, deve-se fazer uma triagem precoce na casa de parto. Para estas crianças e para os prematuros, cuja primeira amostra foi colhida antes das 32 semanas de gestação (GW), é obrigatório o check-up após as 36 horas de vida ou às 32 semanas de gestação.
Um resultado de triagem positivo (recall) representa uma suspeita diagnóstica e deve ser esclarecida imediatamente. Dependendo da gravidade do achado positivo e da suspeita diagnóstica, recomenda-se repetir a triagem ou esclarecimento direto (diagnóstico de confirmação) em um centro especializado.
De acordo com a diretriz infantil, os laboratórios devem apresentar um relatório de qualidade todos os anos, que é publicado para todos os laboratórios de triagem alemães como um relatório de triagem nacional pela Sociedade Alemã de Triagem Neonatal e. V. (DGNS) e publicado em www.screening-dgns.de/reports.php (5). Os laboratórios relatam dados cumulativos sobre a qualidade do processo e dados individuais pseudonimizados sobre diagnósticos de confirmação ao DGNS. Os dados são verificados quanto à plausibilidade e os casos são validados usando critérios definidos. Os casos validados positivamente e os casos sem informação sobre a confirmação diagnóstica, em que os valores repetidos de triagem (“limpeza de triagem neonatal”) falam com uma probabilidade muito alta para o acerto do diagnóstico suspeito, estão relacionados aos nascimentos relatados na Alemanha para o cálculo da prevalência.
Os dados dos relatórios DGNS 2006–2018 (5) foram usados e processados para esta publicação. Os dados sobre rastreio de fibrose quística só estão disponíveis a partir de 2016. Eles serão publicados separadamente, uma vez que aqui é utilizado um algoritmo de triagem complexo, cuja apresentação e os problemas resultantes iriam além do escopo desta publicação. A avaliação estatística foi realizada com SPSS 25.
Resultados
Na Alemanha, onze laboratórios estão atualmente autorizados a fornecer e cobrar pela triagem neonatal. Na Baviera, um centro de triagem independente dos laboratórios também está incluído no Escritório Estatal de Saúde e Segurança Alimentar da Baviera para garantir a alta qualidade do processo e avaliar a triagem (6, 7, 8, 9) (eBox 1). Salvo indicação em contrário, todos os dados e cálculos nesta publicação referem-se a todo o período de 2006 a 2018.
caixa
Parâmetros de qualidade na triagem neonatal
Ampliar imagemTodas as imagens
eBox 1
Organização estrutural da triagem neonatal alemã
Ampliar imagemTodas as imagens
Totais
Numa triagem populacional, o sucesso depende essencialmente de uma alta taxa de participação, que foi alcançada com 9.244.411 exames de triagem documentados em 9.218.538 nascimentos (10) na Alemanha. O maior número de exames pode ser explicado, entre outras coisas, por amostras de crianças não registradas na Alemanha. Um total de 8.471 recusas de toda a ENS (1 em 1.000 recém-nascidos) foi documentado.
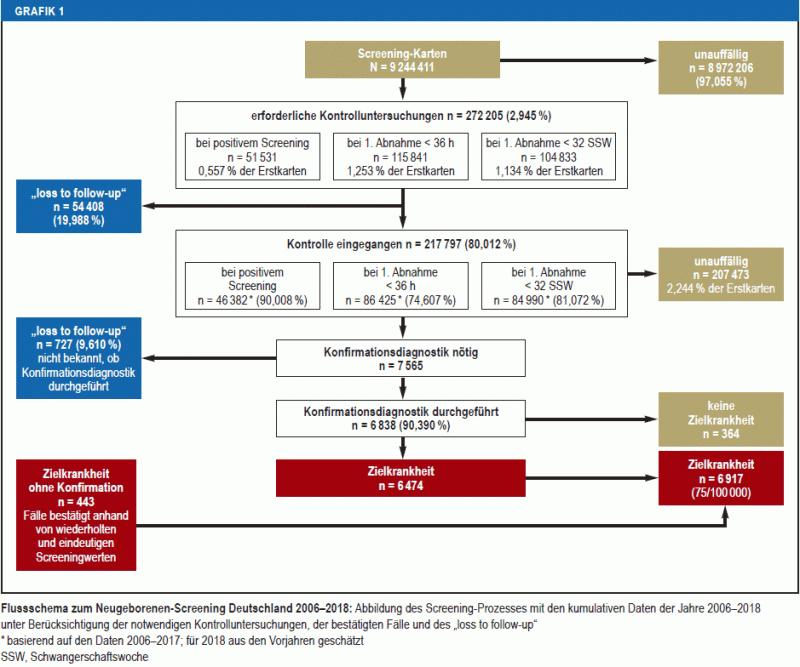
Os laboratórios solicitaram exames de acompanhamento (cartões duplicados) para 30 crianças em 1.000 (n=272.205); a maioria por coleta de sangue antes de 36 horas de vida (13 em 1.000; n = 115.841) ou antes de 32 semanas de gestação (11 em 1.000; n = 104.833). O acompanhamento após um resultado de triagem positivo (rechamada) foi necessário em 51.531 recém-nascidos (6 em 1.000) e foi realizado em 90,01% das crianças. Foram realizados 80,01% (n = 217.797) dos exames solicitados (Figura 1).
Gráfico 1
Fluxograma para triagem neonatal Alemanha 2006-2018
Ampliar imagemTodas as imagens
Tempos de processo
Os tempos de processo curtos são decisivos para a eficácia da triagem neonatal, a fim de alcançar o tratamento mais precoce possível das crianças afetadas (3). A coleta de sangue antes de 72 horas de vida tem uma contribuição significativa e foi realizada em 96,22% dos recém-nascidos em 2018 (eFigura 1, eBox 2). Isso representa um aumento de 13,85% em relação a 2006. Em contrapartida, a proporção de amostras de sangue com mais de dois dias entre a coleta e o recebimento no laboratório aumentou de 42,08% em 2006 para 51,64% em 2018 (eFiguras 2 e 3).
eGráfico 1
Idade na coleta de sangue 2006-2018
Ampliar imagemTodas as imagens
eGráfico 2
Tempo desde a coleta de sangue até o recebimento no laboratório
Ampliar imagemTodas as imagens
eGráfico 3
Tempo desde o recebimento do laboratório até a notificação dos resultados
Ampliar imagemTodas as imagens
eBox 2
Evolução em tempos de processo 2006-2018 no que diz respeito ao diagnóstico precoce
Ampliar imagemTodas as imagens
6.014 das 6.917 crianças com diagnóstico confirmado necessitaram de tratamento, que foi iniciado na primeira semana de vida para 3.127 recém-nascidos (51,95%) e na segunda semana de vida para mais 1.627 crianças (27,05%). Isso significa que 79,05% dos recém-nascidos afetados foram tratados em até duas semanas após o nascimento (mediana de início da terapia = 7 dias de vida). 778 crianças foram tratadas posteriormente, incluindo 342 (43,96%) crianças com hipotireoidismo, 124 (15,94%) com deficiência de acil-CoA desidrogenase de cadeia média (MCAD) e 145 (18, 64%) com deficiência de biotinidase (parcialmente parcial). A proporção de crianças que iniciou o tratamento tardiamente permanece constante ao longo dos anos, assim como a proporção de crianças cujo início do tratamento é desconhecido (n = 482; 8,02%). Em 901 crianças com hiperfenilalaninemia leve, não houve indicação de terapia; dois bebês muito prematuros morreram antes do início da terapia (eFigura 4).
eGráfico 4
Idade no início da terapia
Ampliar imagemTodas as imagens
Prevalência
A prevalência de doenças congênitas raras depende da composição étnica da população de triagem e só pode ser calculada de forma válida quando o número de casos é alto. No presente conjunto de dados, uma doença-alvo foi documentada para 6.917 recém-nascidos, ou seja, para 75 em 100.000 (Tabela 1).
Tabela 1
Doenças-alvo na triagem neonatal alemã 2006-2018; Comparação da prevalência com estimativas de 2004
Ampliar imagemTodas as imagens
Em 37 crianças com resultados de triagem normais (falsos negativos), uma doença-alvo foi diagnosticada com base nos sintomas clínicos e os achados foram relatados ao laboratório de triagem (8 crianças com síndrome adrenogenital, 29 crianças com hipotireoidismo). Estes são relatórios individuais, pois não há registro na Alemanha em que todos os casos de doença sejam documentados.
Qualidade analítica
A qualidade de um procedimento de teste (caixa) é determinada usando sensibilidade, especificidade e valor preditivo positivo (VPP). O VPP descreve a probabilidade com que o diagnóstico será confirmado se o resultado da triagem for positivo e depende da taxa de reconvocação (taxa de resultados positivos da triagem) e da prevalência. A taxa de reconvocação melhorou ao longo dos anos de 0,90% para 0,37%, com variação significativa entre as doenças (Tabela 2, Gráfico 2). Atualmente (dados de 2018), são esperados 370 achados positivos em 100.000 exames de triagem, dos quais 78 são confirmados (VPP = 21,1%). Isso significa que cada quinta criança com resultado de triagem positivo é confirmada como portadora da doença; isso geralmente ocorre com achados altamente patológicos (91,434% confirmados no diagnóstico de confirmação). A sensibilidade não pode ser calculada porque o número de crianças perdidas na triagem não é registrado sistematicamente.
Gráfico 2
Taxas de recordação de doenças-alvo selecionadas na triagem neonatal alemã
Ampliar imagemTodas as imagens
Tabela 2
Taxa de achados de triagem patológica (taxa de reconvocação) e valor preditivo positivo (VPP)
Ampliar imagemTodas as imagens
"Perda de seguimento"
Dos 272.205 check-ups solicitados, incluindo 5.149 após rastreio positivo, 54.408 (19,99%) não foram realizados ("perda de seguimento"). Não há dados diagnósticos de confirmação disponíveis para outras 727 crianças dos 7.565 recém-nascidos (9,61%) com alto grau de suspeição de uma doença-alvo (Figura 1), incluindo um terço com suspeita de hipotireoidismo. Em 443 dessas crianças, os achados da triagem também estavam claros no cartão de controle, para que pudessem ser incluídos no cálculo da prevalência. Em 284 casos (3,75%) isso não foi possível.
No geral, 11,40% dos 51.531 resultados de triagem positivos não foram esclarecidos ou não eram claros (Figura 1). Com 1,14–37,28% de informações ausentes nos diagnósticos de confirmação, há grandes discrepâncias entre os laboratórios.
Discussão
Pela primeira vez, o processo de triagem e os resultados da "triagem neonatal estendida" para toda a Alemanha de 13 coortes de nascimento com um total de 9,2 milhões de crianças são apresentados em uma seção longitudinal. Os resultados mostram que a triagem neonatal também pode ser implementada com muito sucesso em uma estrutura federal com onze laboratórios (eBox 1) se as responsabilidades e os processos forem claramente definidos. Pode-se supor que quase todos os recém-nascidos são rastreados, mesmo que uma comparação pessoal entre crianças nascidas e rastreadas seja realizada apenas em algumas regiões (3). Da mesma forma, metade das crianças afetadas (mediana) pode iniciar o tratamento precocemente em sete dias e 79,05% em duas semanas. Isso corresponde aproximadamente aos dados relatados da Noruega (mediana = 6 dias) e é significativamente anterior a 2012 para a Europa por Burgard et al. (11) publicaram mediana de 14,9 dias e clarificação de 75% dos resultados positivos da triagem em 20 dias. Odenwald et al., mostraram como o diagnóstico precoce e a terapia podem ser importantes. para crianças com síndrome adrenogenital (SAG). Se o tratamento começou após três dias, 23,5% das crianças apresentaram desequilíbrio eletrolítico, e se o tratamento começou por doze dias ou mais, 50% sofreram uma crise de perda de sal (desequilíbrio eletrolítico: 94,4%) (12). No caso de outras doenças, o início precoce do tratamento também pode ser decisivo em relação às crises ou possíveis consequências a longo prazo (13, 14, 15). No geral, o ENS permite que as crianças mais afetadas se desenvolvam normalmente graças à terapia precoce (13, 16, 17).
O efeito positivo de regulamentações claras em exames seriados fica claro quando os componentes não regulamentados são considerados. Por um lado, não há regulamentação sobre rastreamento, por outro lado, os portadores não são sistematicamente registrados para muitas doenças-alvo. Este último é certamente possível se a proteção de dados for rigorosamente observada, seja em registros ou por meio de consultas sistemáticas nos centros de tratamento, como foi publicado para algumas doenças raras na Alemanha (18, 19, 20, 21) e é exigido internacionalmente (22, 23, 24, 25, 26). Declarações válidas sobre a sensibilidade da triagem só podem ser feitas se os dados de todas as crianças afetadas forem combinados. Um alto nível de sensibilidade pode ser assumido para doenças metabólicas, uma vez que essas doenças raras geralmente são tratadas em poucos centros metabólicos. Apenas alguns resultados de triagem falso-negativos foram relatados aqui. Isso é menos claro no caso de doenças endócrinas, uma vez que crianças com hipotireoidismo também são tratadas nos consultórios de médicos de clínica geral. Em princípio, se houver suspeita clínica de uma das doenças-alvo, um diagnóstico específico deve ser feito mesmo que os achados de triagem sejam normais.
Para mais de 55.000 crianças, incluindo 5.876 com resultado de triagem positivo, não está documentado se o resultado foi verificado e esclarecido ("perda de acompanhamento"). Não se sabe se os pais não foram informados ou contatados pelo remetente responsável pela triagem ou se não apresentaram o recém-nascido para o segundo exame de sangue. Também não está claro com que frequência o resultado positivo não foi esclarecido ou se o centro de tratamento ou o pediatra não informou ao laboratório de triagem o resultado do diagnóstico de confirmação. Para resolver este problema, é necessário um sistema de lembrete estruturado, como foi estabelecido na Baviera, por exemplo, com um centro de rastreamento desde 1999 (6, 7, 8, 9). Em outros estados da federação, o rastreamento é feito em parte pelos laboratórios, mas sem financiamento depende dos possíveis recursos locais. Conhecer os resultados dos diagnósticos de confirmação também é importante para o laboratório para garantia de qualidade e otimização da análise.
A taxa de "perda de acompanhamento" e o esforço envolvido no rastreamento continuam a aumentar a cada nova doença-alvo incluída no painel de triagem. Há uma necessidade urgente de ação aqui. Ao incluir o rastreamento nas diretrizes das crianças e fornecer o financiamento adequado, essa tarefa pode ser transferida para os laboratórios de triagem, além de centros independentes.
Um fator decisivo para a alta eficácia da ENS é também a baixa taxa de resultados positivos de triagem (recall), pois todo resultado falso positivo gera preocupação desnecessária para as famílias e custos no sistema de saúde. Entretanto, os critérios de qualidade da ENS, com uma taxa de reconvocações de 0,37% (2018) e um VPP de 21%, são muito melhores do que outros métodos de rastreio que também podem ser considerados eficazes (rastreamento mamográfico: taxa de reconvocação 3ª -14%, PPV 2-22% [27]; triagem auditiva: taxa de reconvocação 5,3%, PPV 6,2% [28]). Uma melhoria adicional seria possível através do uso de métodos de análise adicionais em uma segunda etapa de exame da mesma amostra de sangue no caso de um valor de triagem anormal (“second tier”), sem negligenciar crianças doentes. Isso é mostrado de forma impressionante na triagem de AGS (Figura 2) (29, 30) e é concebível para outras doenças. No entanto, isso aumenta o custo da triagem. Em alguns países, como Noruega ou Suécia, análises de segundo nível também são usadas para doenças metabólicas no painel de triagem (31, 32), na Alemanha como parte de estudos (33, 34).
Com o grande número de aproximadamente 9,2 milhões de crianças rastreadas, a prevalência de doenças congênitas raras na Alemanha pode ser calculada de forma válida, mesmo que algumas prevalências nos dados disponíveis sejam devidas a "perda de acompanhamento" e falta de feedback de casos não detectados na triagem pode estar subestimado. As prevalências não podem necessariamente ser extrapoladas de outras populações e, em alguns casos, apresentam desvios significativos dos valores anteriormente adotados e publicados com base em números de casos muito menores e muitas vezes de outros países (Tabela 1) (16).
Fundação de dados
Neste trabalho são apresentados e interpretados os resultados mais importantes dos relatórios de triagem 2006-2018 (5). Os relatórios elaborados pela DGNS correspondem em muitos aspectos aos critérios de qualidade estabelecidos por Cornel et al. (24) e Ojodu et al. (35) são propostas ou necessárias para a avaliação de um programa de triagem. As limitações desses dados são, por um lado, que nenhum resultado analítico individual está disponível e os dados do processo são fornecidos apenas cumulativamente; por outro lado, falta retorno dos médicos assistentes sobre a confirmação diagnóstica aos laboratórios, necessários para a validação dos casos suspeitos. Para este último, regulamentos obrigatórios que levem em consideração os requisitos de proteção de dados na diretiva de crianças seriam muito úteis.
Em contraste com os relatórios organizados e financiados pelo Estado na Holanda, Grã-Bretanha e Noruega (32, 36, 37), o relatório alemão foi criado por iniciativa da sociedade especializada (DGNS) e dos laboratórios e tem sido o único por mais de dez anos Relatório de qualidade sobre triagem neonatal na Alemanha publicado (5). A fim de garantir uma alta qualidade da triagem neonatal e reconhecer e comunicar prontamente os desenvolvimentos e tendências - também no que diz respeito a novas doenças-alvo - e para otimizar ainda mais a triagem, mais regulamentos sobre garantia de qualidade e avaliação devem ser buscados nas diretrizes para crianças.
Conclusão
A triagem neonatal está sendo implementada em todo o país na Alemanha com grande sucesso e é um exemplo impressionante de uma medida preventiva eficaz em pediatria que está sendo continuamente otimizada. Em sua totalidade, a triagem é um processo complexo no qual estão envolvidos diversos atores de diferentes áreas. A garantia permanente da alta qualidade da triagem neonatal só é garantida se todos os componentes da triagem estiverem sujeitos a um processo de melhoria contínua. O estabelecimento de estruturas de rastreamento, um registro e garantia de qualidade contínua, bem como a avaliação de testes de triagem novos ou modificados são necessários para isso.
Obrigado
Nosso agradecimento especial ao Prof. Dr. médico Heiko Krude e Erwin Lankes (Charité Berlin) pelo apoio na validação das doenças endócrinas e ao Prof. Dr. médico Esther Maier (Dr. von Haunersches Children's Hospital LMU Munich) validando doenças metabólicas.
Contribuintes
Laboratórios de Triagem Alemanha:Dr. médico Oliver Blankenstein, Laboratório de Triagem Neonatal Charité, Universitätsmedizin Berlin; Prof. Dr. ré. claro Uta Ceglarek, laboratório de triagem de Leipzig, Instituto de Medicina Laboratorial, Química Clínica e Diagnóstico Molecular (ILM), Hospital Universitário de Leipzig; dr ré. claro Marina Stopsack, Instituto de Química Clínica e Medicina Laboratorial, Hospital Universitário Carl Gustav Carus na TU Dresden; PD dr médico Martin Lindner, Hesse Screening Center, Hospital Universitário de Frankfurt; dr ré. claro Cornelia Müller, Centro de Triagem Neonatal Mecklenburg-West Pomerania, University Medicine Greifswald; Prof. Dr. médico René Santer, laboratório de triagem de Hamburgo, Hospital Infantil da Universidade de Hamburgo; dr médico dr ré. claro Nils Janzen, Laboratório de Triagem de Hanover; Prof. Dr. médico Gwendolyn Gramer, Triagem Neonatal de Heidelberg, Hospital Universitário de Heidelberg; dr médico Katrin Borucki, Instituto de Química Clínica e Patobioquímica, University Hospital Magdeburg; PD dr médico Wulf Röschinger, Laboratório Becker & Colegas, triagem neonatal, Munique; dr médico dr ré. claro Hans-Wolfgang Schultis, laboratório de triagem, SYNLAB Medical Care Center em Weiden
Conflito de interesse
Dra. Nennstiel recebeu reembolso de despesas de viagem e taxas de palestras da Biogen.
Os demais autores declaram não haver conflito de interesses.
Dados do manuscrito
Enviado: 31/10/2019, versão revisada aceita: 15/09/2020
Endereço dos autores
Dra. médico Uta Nennstiel, MPHBavarian State Office for Health and Food SafetyVeterinärstraße 2, 85764 OberschleißheimUta.Nennstiel@lgl.bayern.de
Estilo de citação
Lüders A, Blankenstein O, Brockow I, Ensenauer R, Lindner M, Schulze A, Nennstiel U, em nome dos laboratórios de triagem na Alemanha: triagem neonatal para distúrbios metabólicos e endócrinos congênitos - resultados da Alemanha para os anos de 2006– 2018 Dtsch Ärzteebl Int 2021; 118:101-8.
DOI: 10.3238/arztebl.m2021.0009
►A versão em inglês do artigo está disponível online em: www.aerzteblatt-international.de
Material adicional
eGraphics, eBoxes: www.aerzteblatt.de/m2021.0009 ou via código QR
1.Diretriz do Federal Joint Committee on the Early Detection of Diseases in Children (Children Guideline), 2020; Seções 13-28. www.g-ba.de/downloads/62-492-2156/Kinder-RL_2020-05-14_iK-2020-03-25.pdf (último acesso em 15 de julho de 2020).
2.Diretriz do Federal Joint Committee on the Early Detection of Diseases in Children (Children Guideline), 2020; Seções 29-42. www.g-ba.de/downloads/62-492-2156/Kinder-RL_2020-05-14_iK-2020-03-25.pdf (último acesso em 15 de julho de 2020).
3.Nennstiel-Ratzel U, Lüders A, Blankenstein O: Triagem neonatal: um excelente exemplo de prevenção secundária eficaz. Diário Federal de Saúde Pesquisa em Saúde Proteção à Saúde 2015; 58:139-45 CrossRef MEDLINE
4.Lei sobre testes genéticos em humanos (Gene Diagnostics Act - GenDG), data de edição 31/07/2009. www.gesetze-im-internet.de/gendg/BJNR252900009.html (último acesso em 15 de julho de 2020).
5.Nennstiel U, Lüders A, Blankenstein O, et al.: DGNS Screening Reports. www.screening-dgns.de/reports.php (último acesso em 15 de julho de 2020).
6.Nennstiel-Ratzel U, Liebl B, Zapf A: Projeto modelo para a reorganização da triagem neonatal na Baviera. Saúde 2003; 65: S31-5 Referência cruzada MEDLINE
7.Liebl B, Nennstiel-Ratzel U, von Kries R, et al.: Triagem neonatal expandida na Baviera: rastreamento para obter a repetição do teste solicitado. PrevMed 2002; 34:132-7 CrossRef MEDLINE
8.Liebl B, Nennstiel-Ratzel U, von Kries R, et al.: Conformidade muito alta em um programa expandido de triagem neonatal baseado em MS-MS, apesar do consentimento por escrito dos pais. PrevMed 2002; 34:127-31 CrossRef MEDLINE
9.Liebl B, von Kries R, Nennstiel-Ratzel U, et al.: Aspectos ético-legais da triagem neonatal. Carta mensal para medicina infantil 2001; 149:1326-35 Referência Cruzada
10.Statistisches Bundesamt Deutschland – GENESIS-Online: Result 12612-0001 (destatis.de) (último acesso em 15 de julho de 2020).
11.Burgard P, Rupp K, Lindner M, et al.: Programas de triagem neonatal na Europa; argumentos e esforços de harmonização. Parte 2. Da triagem dos resultados laboratoriais ao tratamento, acompanhamento e garantia de qualidade. J Herdar Metab Dis 2012; 35:613-25 CrossRef MEDLINE
12.Odenwald B, Dörr HG, Bonfig W, et al.: Hiperplasia adrenal congênita clássica devido à deficiência de 21-hidroxilase: 13 anos de triagem neonatal e acompanhamento na Baviera. Klin Padiatr 2015; 227:278-83 CrossRef MEDLINE
13.Mütze U, Garbade S, Gramer G, et al.: Resultados de longo prazo de indivíduos com doenças metabólicas identificadas por meio da triagem neonatal. Pediatria 2020; DOI: 10.1542/peds.2020-0444 (epub antes da impressão) CrossRef MEDLINE
14.Schweitzer-Krantz S: Diagnóstico precoce de distúrbios metabólicos hereditários para melhorar o resultado: a questão controversa da galactosemia. Eur J Pediatr 2003; 162: S50-3 CrossRef MEDLINE
15.Leger J, Olivieri A, Donaldson M, et al.: Diretrizes de consenso da European Society for Pediatric Endocrinology sobre triagem, diagnóstico e tratamento do hipotireoidismo congênito. Horm Res Paediatr 2014; 81: 80-103 CrossRef MEDLINE
16.Schlune A, Riederer A, Mayatepek E, Ensenauer R: Aspectos da triagem neonatal na acidemia isovalerica. Triagem Neonatal Int J 2018; DOI: 10.3390/ijns4010007 CrossRef MEDLINE PubMed Central
17.Nennstiel-Ratzel U, Arenz S, Maier EM, et al.: Incidência reduzida de crise metabólica grave ou morte em crianças com deficiência de acil-CoA desidrogenase de cadeia média homozigótica para c.985A>Gidentificada por triagem neonatal. Mol Genet Metab 2005; 85:157-9 CrossRef MEDLINE
18.El-Helou SM, Biegner AK, Bode S, et al.: Registro Nacional Alemão de Imunodeficiências Primárias (2012-2017). Front Immunol 2019; 10; DOI: 10.3389/fimmu.2019.01272 CrossRef MEDLINE PubMed Central
19.Nährlich L (ed.), Burkhard J, Wosniok J: Relatório de Registro Alemão de Fibrose Cística, Volume 2018. julho de 2020).
20.Ebrahimi-Fakhari D, Zemlin M, Sauer H, Poryo M, Graf N, Meyer S: Unidade de pesquisa para doenças pediátricas raras na Alemanha (ESPED) - 25 anos de epidemiologia pediátrica: um inventário. Klin Padiatr 2018; 230:215-24 CrossRef MEDLINE
21.Shai S, Perez-Becker R, Andres O, et al.: Incidência de SCID na Alemanha de 2014 a 2015. Uma pesquisa ESPED em nome da API German Pediatric Surveillance Unit. J Clin Immunol 2020; 40:708-17 CrossRef MEDLINE
22.Hoffmann GF, Lindner M, Loeber JG: 50 anos de triagem neonatal. J Herdar Metab Dis 2014; 37:163-4 CrossRef MEDLINE
23.Starkweather A, Coleman B, Barcelona de Mendoza V, et al.: Resumo da política: melhorar a cobertura da triagem genética neonatal para incluir o Painel de Triagem Uniforme Recomendado e o registro de triagem neonatal. Somente Outlook 2017; 65:480-4 CrossRef MEDLINE PubMed Central
24.Cornel MC, Rigter T, Weinreich SS, et al.: Uma estrutura para iniciar o debate sobre as políticas de triagem neonatal na UE: um documento de opinião de especialistas. Eur J Hum Genet 2014; 22:12-7 CrossRef MEDLINE PubMed Central
25.Kanungo S, Patel DR, Neelakantan M, Ryali B: Triagem neonatal e mudança na face dos erros inatos do metabolismo nos Estados Unidos. Ann Transl Med 2018; 6:468 CrossRefMEDLINE PubMed Central
26.Lund AM, Hougaard DM, Simonsen H, et al.: Triagem bioquímica de 504.049 recém-nascidos na Dinamarca, Ilhas Faroé e Groenlândia - experiência e desenvolvimento de um programa de rotina para triagem neonatal expandida. Mol Genet Metab 2012; 107:281-93 CrossRef MEDLINE
27.Mandrik O, Zielonke N, Meheus F, et al.: Revisões sistemáticas como uma 'lente de evidência': determinantes dos benefícios e danos do rastreamento do câncer de mama. Int J Câncer 2019; 145: 994-1006 CrossRef MEDLINE PubMed Central
28.Nennstiel U, Brockow I, Söhl K, et al.: Relatório final sobre a avaliação da triagem auditiva neonatal 2011/2012, a partir de 15 de janeiro de 2017. www.g-ba.de/downloads/17-98-4329/2017-05-18_Kinder-RL_Annahme_Endbericht_NHS-bericht.pdf (último acesso em 15 de julho de 2020).
29.Janzen N, Sander S, Terhardt M, Peter M, Sander J: Quantificação rápida e direta de esteróides adrenais por espectrometria de massa em tandem em soro e manchas de sangue seco. J Chromatogr B Analyt Technol Biomed Life Sci 2008; 861:117-22 CrossRef MEDLINE
30.Janzen N, Peter M, Sander S, et al.: Triagem neonatal para hiperplasia adrenal congênita: perfil adicional de esteróides usando cromatografia líquida-espectrometria de massa em tandem. J Clin Endocrinol Metab 2007; 92:2581-9 CrossRef MEDLINE
31.Sörensen L, von Döbeln U, Ahlmann H, et al.: Triagem expandida de um milhão de bebês suecos com R4S e CLIR para avaliação pós-analítica de dados. Triagem Neonatal Int J 2020; 6:42 CrossRef PubMed Central
32.Tangeraas T, Sæves I, Klingenberg C, et al.: Desempenho da triagem neonatal expandida na Noruega apoiada por ferramentas de bioinformática pós-analítica e análises rápidas de DNA de segundo nível. Triagem Neonatal Int J 2020; 6:51 CrossRef MEDLINE PubMed Central
33.Röschinger W, Sonnenschein S, Schumann E, Nennstiel-Ratzel U, Roscher AA, Olgemöller B: Novas doenças-alvo na triagem neonatal Recomendações de um projeto piloto. Carta mensal para crianças 2015; 2:142-9 Referência Cruzada
34.Gramer G, Hauk F, Lobitz S, Sommerburg O, Speckmann C, Hoffmann GF: Triagem neonatal 2020. Monatsschr Kinderheilkd 2017; 165:216-25 Ref. Cruzada
35.Ojodu J, Singh S, Kellar-Guenther Y, et al.: NewSTEPs: o estabelecimento de um centro nacional de recursos de assistência técnica para triagem neonatal. Triagem Neonatal Int J 2018; 4:1 CrossRef MEDLINE PubMed Central
36.van der Ploeg K, Vitórias S, Verkerk PH. A triagem de sangue em recém-nascidos na Holanda monitora 2018. www.rivm.nl/sites/default/files/2020-01/HielprikMon2018-Engelstalig.pdf (último acesso em 15 de julho de 2020).
37.Begum F: Programa de triagem de manchas de sangue em recém-nascidos no Reino Unido. Relatório de coleta de dados e análise de desempenho de 2016 a 2017. Publicado em maio de 2018. https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/709367/Newborn_blood_spot_screening_data_collection_and_performance_analysis_report_2016_to_2017.pdf (último acesso em 15 julho de 2020).
38.Lobitz S, Frömmel C, Brose A, Klein J, Blankenstein O: Incidência da doença falciforme em uma coorte não selecionada de neonatos nascidos em Berlim, Alemanha. Eur J Hum Genet 2014; 22:1051-3 CrossRef MEDLINE PubMed Central
39.Frömmel C, Brose A, Klein J, Blankenstein O, Lobitz S: Triagem neonatal para doença falciforme: aspectos técnicos e legais de um estudo piloto alemão com 38.220 participantes. Biomed Res Int 2014; 2014: 695828 CrossRef MEDLINE PubMed Central
40.Vill K, Kölbel H, Schwartz O, et al.: Um ano de triagem neonatal para SMA – resultados de um projeto piloto alemão. J Neuromuscul Dis 2019; 6:503-1 CrossRef MEDLINE PubMed Central